Students can go through AP Board 9th Class Physical Science Notes 3rd Lesson మన చుట్టూ ఉన్న పదార్థం శుద్ధమేనా? to understand and remember the concept easily.
AP Board 9th Class Physical Science Notes 3rd Lesson మన చుట్టూ ఉన్న పదార్థం శుద్ధమేనా?
→ మన దైనందిన భాషలో శుద్ధ పదార్థం అనగా ఎటువంటి కత్తీ లేని పదార్థం.
→ సాధారణంగా రెండు లేదా అంతకన్నా ఎక్కువ రకాల అనుఘటకాల కలయిక ద్వారా ఏర్పడిన దానిని మిశ్రమం అంటారు.
→ మిశ్రమాలు రెండు రకాలు. అవి : సజాతీయ మిశ్రమాలు, విజాతీయ మిశ్రమాలు.
→ మిశ్రమంలో ఉండే అనుఘటకాలు ఆ మిశ్రమం అంతటా ఏకరీతిగా విస్తరించి ఉంటే ఆ మిశ్రమాన్ని సజాతీయ మిశ్రమం అంటాం.
→ ఒక మిశ్రమంలో భిన్న పదార్థాలు లేక భిన్న స్థితులలో ఉండే ఒకే పదార్ధ భాగాలు కలిసినట్లయితే ఆ మిశ్రమాన్ని ‘విజాతీయ మిశ్రమం’ అంటారు.
![]()
→ రెండు లేదా అంతకంటే ఎక్కువ పదార్థాల సజాతీయ మిశ్రమాన్ని ‘ద్రావణం’ అంటాం.
→ ద్రావణంలో ఎక్కువ పరిమాణంలో ఉండి, కరిగించుకొనే పదార్థంను ద్రావణి అంటారు.
→ ద్రావణంలో తక్కువ పరిమాణంలో ఉండి, కరిగియున్న పదార్థంను ద్రావితం అంటారు.
→ నిర్దిష్ట ఉష్ణోగ్రత వద్ద ఒక సంతృప్త ద్రావణంలో కరిగియున్న ద్రావిత పరిమాణంను ఆ ఉష్ణోగ్రత వద్ద దాని ద్రావణీయత’ అంటారు.
→ ఒక నిర్దిష్ట ఉష్ణోగ్రత వద్ద ద్రావణంలో ఎంత ద్రావితం కరగగలదో అంతే ద్రావితం కలిగియున్న ద్రావణాన్ని “సంతృప్త ద్రావణం” అంటారు.
→ ఒక ద్రావణంలో గరిష్ఠంగా కరగగలిగే ద్రావిత పరిమాణం కంటే తక్కువ ద్రావితం కరిగియుంటే ఆ ద్రావణాన్ని అసంతృప్త ద్రావణం అంటారు.
→ ఒక ద్రావణంలో ద్రావిత పరిమాణం తక్కువగా ఉంటే ఆ ద్రావణంను ‘విలీన ద్రావణం’ అంటారు. అలా కాకుండా ద్రావిత పరిమాణం ఎక్కువ ఉంటే ఆ ద్రావణంను ‘గాఢ ద్రావణం’ అంటారు.
→ నిర్దిష్ట ఘనపరిమాణం గల ద్రావణంలో కరిగియున్న ద్రావిత పరిమాణం లేదా నిర్దిష్ట పరిమాణం గల ఒక ద్రావణి కలిగియున్న ద్రావిత పరిమాణంను ఆ ‘ద్రావణ గాఢత’ అంటారు.
→ ద్రావణిలో కరగకుండా ఉండి, మన కంటితో చూడగలిగే పదార్థాల కణాలతో అవలంబనాలు ఏర్పడుతాయి. ఇవి ‘విజాతీయ’ మిశ్రమాలు.
![]()
→ కొలాయిడ్ లేదా కాంజికాభకణ ద్రావణాలు విజాతీయ మిశ్రమాలు. వీటి కణాల పరిమాణం చాలా తక్కువగా ఉన్నప్పటికీ కాంతిపుంజాలను పరిక్షేపించగలిగేంతగా ఉంటాయి.
→ పరస్పరం కలవని రెండు ద్రవాలను కలిగియుండి, మిశ్రమాన్ని కదలకుండా ఒక చోట ఉంచినప్పుడు ఆ ద్రవాలు రెండు పొరలుగా నిలిచిపోతాయి. పరస్పరం కలవని రెండు ద్రవాలు గల ఇలాంటి మిశ్రమాలనే ‘ఎమర్జెన్’ లు అంటారు.
→ కొలాయిడల్ ద్రావణాలు రెండు ప్రావస్థలు కలిగియుంటాయి. అవి : 1. విక్షేపణ ప్రావస్థ, 2. విక్షేపణ యానకం.
→ కాంతిపుంజం వివర్తనం చెందించడాన్ని “టిండాల్ ప్రభావము” అంటారు.
→ సాధారణంగా మనం మిశ్రమాలను జల్లెడ పట్టడం, వడపోయడం, తేర్చడం, స్పటికీకరణం, క్రొమటోగ్రఫీ, స్వేదనము, అంశిక స్వేదనము, అపకేంద్ర యంత్రం వంటి కొన్ని పద్ధతుల ద్వారా వేరుచేస్తారు.
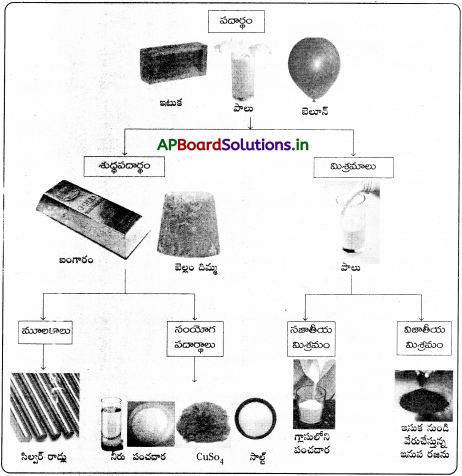
→ శుద్ధ పదార్థం రెండు రకాలు. అవి : 1. మూలకం, 2. సంయోగ పదార్థం.
→ మూలకం అనేది పదార్ధం యొక్క మూలరూపం. ఇది రసాయన చర్యలలో మరికొన్ని కణాలుగా విడిపోదు.
→ సంయోగ పదార్థాలను “శుద్ధ పదార్థాలు”గా చెప్పవచ్చు. వీటిని రసాయనిక చర్య ద్వారా మాత్రమే రెండు లేదా అంతకన్నా ఎక్కువ అనుఘటకాలుగా విడగొట్టగలుగుతాం.
→ సంయోగపదార్ధ ధర్మాలు దాని అనుఘటక మూలకాల ధర్మాలకు భిన్నంగా ఉంటాయి. కాని ఒక మిశ్రమం, దాని అనుఘటక పదార్థాల ధర్మాలను ప్రదర్శిస్తుంది.
→ శుద్ధపదార్థం : ఒక పదార్థం శుద్ధమైనది అంటే అది సజాతీయమైనది. ఆ పదార్థం యొక్క ఏ భాగం నుండి తీసుకున్న నమూనాలోనైనా సంఘటనంలో మార్పు ఉండదు.
→ మిశ్రమం : సాధారణంగా రెండు లేదా అంతకంటే ఎక్కువ రకాల అనుఘటకాల కలయిక (సంయోగం) ద్వారా ఏర్పడిన దానిని ‘మిశ్రమం’ అంటారు. ఒక మిశ్రమంలోని పదార్థాల కలయిక భౌతిక కలయికే కాని, రసాయన కలయిక కాదు.
![]()
→ సజాతీయ మిశ్రమం : మిశ్రమంలో ఉండే అనుఘటకాలు. ఆ మిశ్రమం అంతటా ఏకరీతిగా విస్తరించి ఉంటే ఆ మిశ్రమాన్ని సజాతీయ మిశ్రమం’ అంటారు.
→ విజాతీయ మిశ్రమం : ఒక మిశ్రమంలో భిన్న పదార్థాలు లేక భిన్న స్థితులలో ఉండే ఒకే పదార్ధ భాగాలు కలిసినట్లయితే ఆ మిశ్రమాన్ని ‘విజాతీయ మిశ్రమం’ అంటారు.
→ ద్రావణం : రెండు లేదా అంతకంటే ఎక్కువ పదార్థాల సజాతీయ మిశ్రమాన్ని ‘ద్రావణం’ అంటారు.
→ ఆవలంబనం : ఒక ద్రావణిలో కరగకుండా ఉండి మన కంటితో చూడగలిగే పదార్థాల అవలంబనాలు ఏర్పడుతాయి. ఇవి విజాతీయ’ మిశ్రమాలు.
→ కొలాయిడ్ ద్రావణాలు : కొలాయిడ్ లేదా కాంజికాభకణ ద్రావణాలు విజాతీయ మిశ్రమా , ఎల కణాల పరిమాణం చాలా తక్కువగా ఉన్నప్పటికీ కాంతి పుంజాలను పరిక్షేపించగలిగేంతగా ఉంటాయి.
→ కొలాయిడ్ విక్షేపణం : కొలాయిడ్ ద్రావణాలు కనీసం రెండు ప్రావస్థలను కలిగి ఉంటాయి.
1) విక్షేపణ ప్రావస్త :
ఇది కొలాయిడ్ యానకంలో తక్కువ నిష్పత్తిలో కలిసి ఉన్న పదార్థం మరియు ఇందులో ఉండే కొలాయిడ్ కణాల పరిమాణాలు 1 nm నుండి 10 nm వరకు ఉంటాయి.
2) విక్షేపణ యానకం :
ఇది కొలాయిడ్ కణాలు విస్తరించి ఉన్న ఒక యానకం. యానకంలో కొలాయిడ్ కణాల ఏకరీతి విస్తరణను విక్షేపణం అంటారు.
→ ఎమల్షన్ : పరస్పరం కలవని రెండు ద్రవాలను కలిగియుండి, మిశ్రమాన్ని కదలకుండా ఒక చోట ఉంచినప్పుడు ఆ ద్రవాలు రెండు పొరలుగా నిలిచిపోతాయి. పరస్పరం కలవని రెండు ద్రవాలు గల ఇలాంటి మిశ్రమాలనే ఎమలన్’ లు అంటారు.
![]()
→ ద్రావణి : ద్రావణంలో ఎక్కువ పరిమాణంలో ఉండి, కరిగించుకొనే పదార్థంను ద్రావణి అంటారు.
→ ద్రావితం : ద్రావణంలో తక్కువ పరిమాణంలో ఉండి, కరిగియున్న పదార్థంను ద్రావితం అంటారు.
→ ద్రావణీయత : నిర్దిష్ట ఉష్ణోగ్రత వద్ద, ఒక సంతృప్త ద్రావణంలో కరిగియున్న ద్రావిత పరిమాణంను ఆ ఉష్ణోగ్రత వద్ద దాని ద్రావణీయత’ అంటారు.
→ ద్రావణం గాఢత : నిర్దిష్ట ఘనపరిమాణం గల ద్రావణంలో కరిగియున్న ద్రావిత పరిమాణం లేదా నిర్దిష్ట పరిమాణం గల ఒక ద్రావణి కలిగియున్న ద్రావిత పరిమాణంను ఆ ద్రావణ గాఢత అంటారు.
→ టిండాల్ ప్రభావము : కాంతిపుంజం వివర్తనం చెందించడాన్ని టిండాల్ ప్రభావము అంటారు.
→ బాష్పీభవనము : ద్రవపదార్థాలు వాయు పదార్థాలుగా మారడాన్ని బాష్పీభవనము అంటారు. ఇది ఉప్పు, నీరు వంటి మిశ్రమాలను వేరుచేయుటకు ఉపయోగించు ఒక విధానము.
→ అపకేంద్ర మంత్రం : పాల నుండి వెన్న వంటి మిశ్రమాలను వేరుచేయుటకు వాడే ఒక పరికరమే అపకేంద్ర యంత్రం.
→ అమిశ్రణీయ ద్రావణాలు : ఒక ద్రవం మరొక ద్రావణంలో పూర్తిగా కలవకుండా నీటిలో నూనె మాదిరిగా ఒకదానిపై మరొకటి పొరలుగా ఏర్పడి సులువుగా వేరుచేయగలిగే ద్రవాలను అమిశ్రణీయ ద్రవాలు అంటారు.
![]()
→ మిశ్రణీయ ద్రవాలు : ఒక ద్రవం మరొక ద్రవంలో పూర్తిగా కలిసిపోతే వాటిని మిశ్రణీయ ద్రవాలు అంటారు.
→ కొనుటోగ్రఫీ : క్రొమటోగ్రఫీ అనేది ఒక ప్రయోగశాల ప్రక్రియ. దీని ద్వారా ఒక మిశ్రమంలో గల భిన్న అనుఘటకాలను వేరుచేయవచ్చు. ఈ పద్ధతిని సికాలోగల రంగులోని అనుఘటకాలను వేరుచేయడానికి ఉపయోగిస్తారు.
→ స్వేదనం : రెండు లేదా అంతకంటే ఎక్కువ మిశ్రణీయ ద్రవాల యొక్క బాష్పీభవన స్థానాలలో వ్యత్యాసం 25 C కంటే ఎక్కువగా ఉంటే, ఆ రకమైన ద్రవాలను వేరుచేయడానికి స్వేదన ప్రక్రియను ఉపయోగిస్తారు.
→ అంశిక స్వేదవం : రెండు లేదా అంతకంటే ఎక్కువ మిశ్రణీయ ద్రవాల యొక్క బాష్పీభవన స్థానాలలో వ్యత్యాసం 25°C కంటే తక్కువగా ఉంటే, ఆ రకమైన ద్రవాలను వేరుచేయడానికి అంశిక స్వేదన ప్రక్రియను ఉపయోగిస్తారు.
→ మూలకం : మూలకం అనేది పదార్థం యొక్క మూలరూపం. ఇది రసాయన చర్యలలో మరికొన్ని కణాలుగా విడిపోదు.
![]()
→ సంయోగ పదార్థాలు : సంయోగ పదార్థాలను “శుద్ధ పదార్థాలు”గా చెప్పవచ్చు. వీటిని రసాయనిక చర్య ద్వారా మాత్రమే రెండు లేదా అంతకన్నా ఎక్కువ అనుఘటకాలుగా విడగొట్టగలుగుతాం.
→ విక్షేపణ యానకం : కాంజికాభ కణాలు, విస్తరించి వున్న ఒక యానకం.
→ విక్షేపణ ప్రావస్థ : కాంజికాభ కణ ద్రావణంలో పరస్పరంగా తక్కువ నిష్పత్తిలో గల మరియు 1nm నుండి 100nm ల పరిమాణాలు గల కణాలను కల్గి వున్న ప్రావస్థ.