Andhra Pradesh BIEAP AP Inter 1st Year Chemistry Study Material 1st Lesson పరమాణు నిర్మాణం Textbook Questions and Answers.
AP Inter 1st Year Chemistry Study Material 1st Lesson పరమాణు నిర్మాణం
అతిస్వల్ప సమాధాన ప్రశ్నలు
ప్రశ్న 1.
ఎలక్ట్రాన్ ఆవేశం, ద్రవ్యరాశి ఎంత ఉంటాయి? ఎలక్ట్రాన్ ఆవేశానికి, ద్రవ్యరాశికి గల నిష్పత్తి ఎంత?
జవాబు:

ప్రశ్న 2.
ఒక మోల్ ఎలక్ట్రాన్ల ఆవేశాన్ని గణించండి.
జవాబు:
ఒక ఎలక్ట్రాన్ యొక్క ఆవేశం ఒక మోల్ ఎలక్ట్రాన్ల ఆవేశం
= – 1.602 × 10-19 coloumbs
= 6.023 × 1023 × 1.602 × 10-19
= 96488.5 coloumbs
ప్రశ్న 3.
ఒక మోల్ ఎలక్ట్రాన్ల ద్రవ్యరాశిని గణించండి.
జవాబు:
ఎలక్ట్రాన్ ద్రవ్యరాశి = 9.1 × 10-31 kg
ఒక మోల్ ఎలక్ట్రాన్ల ద్రవ్యరాశి = 6.023 × 1023 × 9.1 × 10-31
= 5.48 × 10-7 kg.
ప్రశ్న 4.
ఒక మోల్ ప్రోటాన్ల ద్రవ్యరాశిని గణించండి.
జవాబు:
ప్రోటాన్ ద్రవ్యరాశి = 1.672 × 10-27 kg
ఒక మోల్ ప్రోటాన్ల ద్రవ్యరాశి = 6.023 × 1023 x 1.672 × 10-27
= 1.00704 × 10-3 kg.
ప్రశ్న 5.
ఒక మోల్ న్యూట్రాన్ల ద్రవ్యరాశిని గణించండి.
జవాబు:
న్యూట్రాన్ ద్రవ్యరాశి 1.675 × 10-27 kg
ఒక మోల్ న్యూట్రాన్ల ద్రవ్యరాశి
= 6.023 × 1023 × 1.675 × 10-27
= 1.0088 × 10-3 kg.
![]()
ప్రశ్న 6.
6C13, 8O16 12Mg24, 26Fe56, 38Sr88 కేంద్రకాలలో ఉండే న్యూట్రాన్ల, ఎలక్ట్రాన్ల సంఖ్య ఎంత?
జవాబు:
| (zxA) | ఎలక్ట్రాన్ల సంఖ్య (Z) | న్యూట్రాన్ల సంఖ్య (A – Z) |
| i) 6 C13 | 6 | 13 – 6 = 7 |
| ii) 8O16 | 8 | 16 – 8 = -8 |
| iii) 12Mg14 | 12 | 24 – 12 = 12 |
| iv) 26 Fe56 | 26 | 56 – 26 = 30 |
| v) 38Sr88 | 38 | 88 – 38 = 50 |
ప్రశ్న 7.
కృష్ణ పదార్థం అంటే ఏమిటి?
జవాబు:
వికిరణాల శక్తిని సంపూర్ణంగా శోషించుకునే పదార్థాన్ని కృష్ణ పదార్థం (లేక) నల్లని పదార్థం అంటారు. కృష్ణ పదార్థం అవసరమైతే శోషించుకున్న మొత్తం శక్తిని వికిరణం కూడా చేస్తుంది.
ప్రశ్న 8.
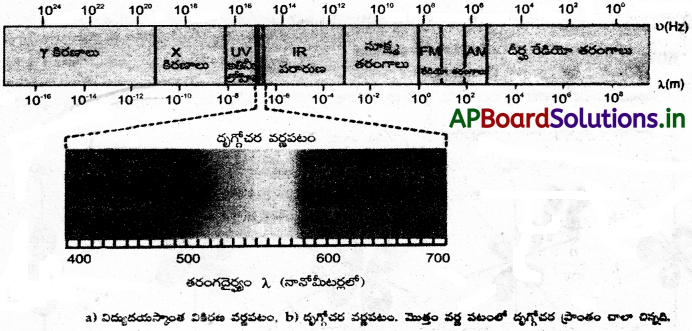
బామర్ శ్రేణి విద్యుదయస్కాంత వర్ణపటంలో ఏ ప్రాంతానికి చెందింది?
జవాబు:
బామర్ శ్రేణి :
హైడ్రోజన్ పరమాణువులో ఉత్తేజితం చెందిన ఎలక్ట్రాన్పై శక్తి స్థాయిల నుండి (n2 = 3, 4, 5, ……) రెండవ శక్తిస్థాయి (n1 = 2) లోకి దూకినపుడు వెలువడే కాంతి వలన బామర్ శ్రేణిలోని గీతలు ఏర్పడతాయి.
బామర్ శ్రేణి విద్యుదయస్కాంత వర్ణపటంలో దృగ్గోచర ప్రాంతంలో ఏర్పడుతుంది.
ప్రశ్న 9.
పరమాణు ఆర్బిటాల్ అంటే ఏమిటి?
జవాబు:
పరమాణు ఆర్బిటాల్ :
పరమాణువులో కేంద్రకం చుట్టూ ఉండే త్రిజామితీయ ప్రదేశంలో ఒక ఎలక్ట్రాన్ను కనుగొనే సంభావ్యత గరిష్ఠంగా (Ψ² = గరిష్ఠం) గల ప్రదేశాన్ని ఎలక్ట్రాన్ పరమాణు ఆర్బిటాల్ అంటారు.
ప్రశ్న 10.
హైడ్రోజన్ పరమాణువులో ఎలక్ట్రాన్ n = 4 కక్ష్య నుంచి n = 5 కక్ష్యకు మార్పు చెందినప్పుడు గ్రహించిన కాంతిరేఖ వర్ణపట శ్రేణిలో దేనికి చెందుతుంది?
జవాబు:
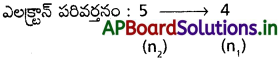
హైడ్రోజన్ పరమాణువులో ఎలక్ట్రాన్ పై శక్తి స్థాయిల నుండి నాల్గవ స్థాయికి (n1 = 4) వచ్చినపుడు వెలువడే కాంతి వలన బ్రాకెట్ శ్రేణిలో గీతలు ఏర్పడతాయి. బ్రాకెట్ శ్రేణి విద్యుదయస్కాంత వర్ణపటంలో పరారుణ ప్రాంతంలో ఏర్పడుతుంది.
ప్రశ్న 11.
సల్ఫర్ పరమాణువులో ఎన్ని p ఎలక్ట్రాన్లు ఉన్నాయి?
జవాబు:
సల్ఫర్ (2 = 16) ఎలక్ట్రాన్ విన్యాసము 1s²2s²2p63s² 3p4
∴ సల్ఫర్ పరమాణువులో మొత్తం ‘p’ ఎలక్ట్రాన్ల సంఖ్య ’10’. (2p6 + 3p4)
ప్రశ్న 12.
3d ఎలక్ట్రాన్ ప్రధాన క్వాంటమ్ సంఖ్య (n), ఎజిముతల్ క్వాంటమ్ సంఖ్య (7) విలువలు ఎంత?
జవాబు:
3d ఎలక్ట్రాన్కు n = 3 మరియు l = 2
![]()
ప్రశ్న 13.
ఇచ్చిన పరమాణు సంఖ్య (Z), పరమాణు ద్రవ్యరాశి (A) గల పరమాణు పూర్తి గుర్తు ఏమిటి?
(I) Z = 4, A = 9 ; (II)Z=17, A = 35 (III) 2 = 92, A =233:
జవాబు:
I) 2 = 4, A = 9 అనగా 4B9
II) Z = 17, A = 35 అనగా 17Cl35
III) Z = 92, A = 233 అనగా 92U233.
ప్రశ్న 14.
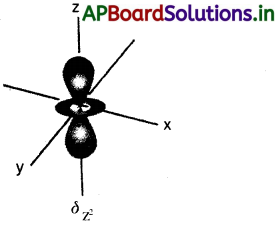
dz² ఆర్బిటాల్ ఆకారాన్ని గీయండి.
జవాబు:
dz² ఆర్బిటాల్ ఆకారం
ప్రశ్న 15.
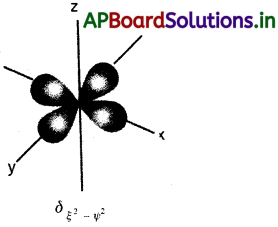
dx²-y² ఆర్బిటాల్ ఆకారాన్ని గీయండి.
జవాబు:
dx²-y² ఆర్బిటాల్ ఆకారం
ప్రశ్న 16.
600 nm తరంగదైర్ఘ్యం గల వికిరణాల పౌనఃపున్యం ఎంత?
జవాబు:

ప్రశ్న 17.
జీమన్ ప్రభావం అంటే ఏమిటి?
జవాబు:
బలమైన అయస్కాంత క్షేత్రంలో పరమాణు వర్ణపటంలో ఒక్కొక్క గీత చిన్న చిన్న గీతలుగా విభజింపబడటాన్ని జీమన్ ఫలితం అంటారు.
ప్రశ్న 18.
స్టార్క్ ప్రభావం అంటే ఏమిటి?
జవాబు:
బలమైన విద్యుత్ క్షేత్రంలో పరమాణు వర్ణ పటంలో ఒక్కొక్క గీత చిన్న చిన్న గీతలుగా విభజింపబడటాన్ని స్టార్క్ ప్రభావం అంటారు.
ప్రశ్న 19.
ఈ కింది ఎలక్ట్రాన్ విన్యాసాలు ఏ మూలకాలకు చెందినవి?
(I) 1s²2s²2p63s² 3p¹ (II) 1s²2s²2p63s²3p6 (III) 1s²2s²2p5 (IV) 1s²2s²2p².
జవాబు:
I) 1s²2s²2p² విన్యాసము కార్బన్ (C) పరమాణువుకి చెందినది.
II) 1s²2s²2p63s² 3p¹ విన్యాసము అల్యూమినియం (AI) పరమాణువుకి చెందినది.
III) 1s²2s²2p63s²3p6 విన్యాసము ఆర్గాన్ (Ar) పరమాణువుకి చెందినది.
IV) 1s²2s²2p5 విన్యాసము ఫ్లోరిన్ (F) పరమాణువుకి చెందినది.
ప్రశ్న 20.
4000 Å తరంగదైర్ఘ్య వికిరణాలను లోహతలంపై పడేటట్లు చేస్తే శూన్యం వేగం గల ఎలక్ట్రాన్లు ఉద్గారమయ్యాయి. ఆరంభ పౌనఃపున్యం (ν0) ఎంత?
జవాబు:

ప్రశ్న 21.
పౌలివర్ణన సూత్రాన్ని వివరించండి.
జవాబు:
పౌలివర్జన నియమము :
ఒక పరమాణువులో ఏ రెండు ఎలక్ట్రాన్లకు నాలుగు క్వాంటం సంఖ్యల విలువలు సమానంగా ఉండవు. (లేక) ఒక ఆర్బిటాల్లో వ్యతిరేక స్పిన్లు గల రెండు ఎలక్ట్రాన్లకే చోటు ఉంటుంది.
![]()
ప్రశ్న 22.
ఆఫ్ నియమం అంటే ఏమిటి?
జవాబు:
ఆఫ్ బౌ నియమం :
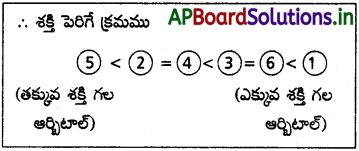
“ఎలక్ట్రాన్లు పరమాణు భూస్థాయిలో అందుబాటులో ఉండే కనిష్ఠ శక్తి ఆర్బిటాల్లోకి ప్రవేశిస్తాయి”. “శక్తి పెరిగే క్రమంలో ఆర్బిటాల్లు వరుసగా ఎలక్ట్రాన్లతో భర్తీ అవుతాయి”.

ప్రశ్న 23.
హుండ్ నియమం అంటే ఏమిటి?
జవాబు:
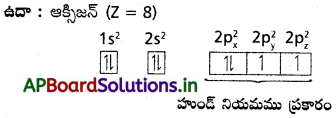
హుండ్ నియమం :
సమాన శక్తి గల (డీ జనరేట్) ఆర్బిటాల్లు ఒకటి కన్నా ఎక్కువగా ఉన్నప్పుడు వీటన్నింటిలో ఒక్కొక్క ఎలక్ట్రాన్ ప్రవేశించిన తర్వాతనే ఎలక్ట్రాన్లు జతగూడడం జరుగుతుంది.
ప్రశ్న 24.
హైసన్బర్గ్ అనిశ్చితత్వ నియమం వివరించండి.
జవాబు:
అనిశ్చితత్వ నియమం :
“అతివేగంగా ప్రయాణించే ఎలక్ట్రాన్ వంటి సూక్ష్మ పరమాణు కణాల స్థానం, ద్రవ్యవేగం రెండింటినీ ఏక కాలంలో ఖచ్చితంగా నిర్ణయించలేం స్థాన నిర్ణయంలో అనిశ్చితత్వం (∆x), ద్రవ్యవేగంలో అనిశ్చితత్వం (∆P) అయితే

హైసన్బర్గ్ అనిశ్చితత్వ నియమ ప్రాముఖ్యత :
- ఈ నియమం ప్రకారం, ఎలక్ట్రానుగానీ, ఎలక్ట్రాన్ లాంటి ఇతర కణాలకుగానీ స్థిరమైన కక్ష్య లేదా ప్రక్షేపమార్గం ఉండే అవకాశం లేదు.
- ఈ నియమం సూక్ష్మాతి సూక్ష్మకణాలకు మాత్రమే ప్రాముఖ్యం ఇస్తుంది. స్థూలకణాలకు వర్తించదు.
- మిల్లీగ్రాము గాని అంతకంటే బరువైన వస్తువులకు అనిశ్చితత్వంతో ఫలితం ఏమీ ఉండదు.
ప్రశ్న 25.
2.0 × 107m/s-1 వేగంతో ప్రయాణించే ఎలక్ట్రాన్ తరంగదైర్ఘ్యం ఎంత?
జవాబు:

ప్రశ్న 26.
పరమాణు ఆర్బిటాల్కు n విలువ 2 అయిన I, m,లకు సాధ్యమైన విలువలేమి ?
జవాబు:
n = 2 అయిన = 0,1
l = 0 అయిన ml = 0
l = 1 అయిన ml = -1, 0, +1
ప్రశ్న 27.
ఇక్కడ ఇచ్చిన ఆర్బిటాల్లో ఏవి సాధ్యం? 2s, 1p, 3f, 2p.
జవాబు:
ఇవ్వబడిన ఆర్బిటాల్లో 2s మరియు 2p లు మాత్రమే సాధ్యమయినవి.
కారణము :
రెండవ శక్తిస్థాయిలో (n = 2) రెండు ఉపశక్తి స్థాయిలుంటాయి. అవి. l = 0(s) మరియు 1(p) వాటిని ‘2s’ మరియు ‘2p’ గా సూచిస్తారు.
ప్రశ్న 28.
నూనె చుక్క మీద ఉన్న స్థిర విద్యుత్ ఆవేశం – 3.2044 × 10-19 C. దానిమీద ఎన్ని ఎలక్ట్రాన్లు ఉన్నాయి?
జవాబు:
నూనె చుక్క స్థిర విద్యుదావేశం = 3.2044 × 10-19 C
ఎలక్ట్రాన్ ఆవేశం = – 1.602 × 10-19 C
![]()
ప్రశ్న 29.
కింద ఇచ్చిన వికిరణాలను పౌనఃపున్యాలు పెరిగే క్రమంలో ఏర్పరచండి.
(a) × – కిరణాలు
(b) దృగ్గోచర వికిరణాలు
(c) సూక్ష్మతరంగ వికిరణాలు
(d) రేడియో తరంగ వికిరణాలు
జవాబు:
రేడియో తరంగాలు < సూక్ష్మతరంగ వికిరణాలు < దృగ్గోచర వికిరణాలు < X – కిరణాలు.
ప్రశ్న 30.
n = 4, ms = + 1/2 తో పరమాణువులో ఉండే ఎలక్ట్రాన్ల సంఖ్య ఎంత?
జవాబు:
n = 4 అయిన విలువలు 0, 1, 2, 3
l = 0 అయిన $ ఆర్బిటాల్లో ఒక ఎలక్ట్రాన్ ms = + 1/2 తో ఉండును
l = 1 అయిన p ఆర్బిటాల్లో 3 ఎలక్ట్రాన్లు ms = + 1/2 తో ఉండును
l = 2 అయిన d ఆర్బిటాల్లో 5 ఎలక్ట్రాన్లు ms = + 1/2 తో ఉండును
l = 3 అయిన f ఆర్బిటాల్లో 7 ఎలక్ట్రాన్లు ms = + 1/2 తో ఉండును
∴ మొత్తం ఎలక్ట్రాన్ల సంఖ్య =1 + 3 + 5 + 7 = 16.
ప్రశ్న 31.
n = 5 లో ఉండే ఉపకర్పరాల సంఖ్య ఎంత?
జవాబు:
n = 5 అయిన 7 విలువలు 0, 1, 2, 3, 4
l = 0 అయిన s – ఆర్బిటాల్
l = 1 అయిన p – ఆర్బిటాల్
l = 2 అయిన d – ఆర్బిటాల్
l = 3 అయిన f – ఆర్బిటాల్
l = 4 అయిన g – ఆర్బిటాల్
∴ n = 5 తో ‘5’ ఉపకర్పరాలు కలవు.
![]()
ప్రశ్న 32.
విద్యుదయస్కాంత వికిరణాల కణస్వభావాన్ని వివరించండి.
జవాబు:
- కాంతి కొన్ని కణాలతో ఏర్పడుతుంది అని న్యూటన్ తన భావనలలో చెప్పడం జరిగింది. న్యూటన్ కణాలను కార్పస్కూల్స్ అని చెప్పాడు.
- కాంతి కణ స్వభావం కృష్ణ వస్తువు వికిరణాలను మరియు కాంతి విద్యుత్ ఫలితాన్ని సంతృప్తికరంగా వివరించినది.
- కాంతి కణ స్వభావం వివర్తనం, వ్యతికరణం వంటి ప్రక్రియలను వివరించలేకపోయింది.
ప్రశ్న 33.
హైసన్బర్గ్ అనిశ్చితత్వ నియమం ప్రాముఖ్యాన్ని వివరించండి.
జవాబు:
హైసన్బర్గ్ అనిశ్చితత్వ నియమ ప్రాముఖ్యత :
- ఈ నియమం ప్రకారం, ఎలక్ట్రాన్ కుగానీ, ఎలక్ట్రాన్ లాంటి ఇతర కణాలకుగానీ స్థిరమైన కక్ష్య లేదా ప్రక్షేపమార్గం ఉండే అవకాశం లేదు.
- ఈ నియమం సూక్ష్మాతి సూక్ష్మకణాలకు మాత్రమే ప్రాముఖ్యం ఇస్తుంది. స్థూలకణాలకు వర్తించదు.
- మిల్లీగ్రాము గాని అంతకంటే బరువైన వస్తువులకు అనిశ్చితత్వంతో ఫలితం ఏమీ ఉండదు.
ప్రశ్న 34.
హైడ్రోజన్ వర్ణపటంలో పరిశీలించిన రేఖ శ్రేణులు ఏమిటి ?
జవాబు:
| n విలువ | శ్రేణి | ప్రాంత |
| 1 | లైమన్ శ్రేణి | UV ప్రాంతం |
| 2 | బామర్ శ్రేణి | దృగ్గోచర ప్రాంతం |
| 3 | పాషన్ శ్రేణి | పరారుణ |
| 4 | బ్రాకెట్ శ్రేణి | పరారుణ |
| 5 | ఫండ్ శ్రేణి | పరారుణ |
స్వల్ప సమాధాన ప్రశ్నలు
ప్రశ్న 1.
హైడ్రోజన్ పరమాణువులో ఎలక్ట్రాన్ n = 5 శక్తి స్థాయి నుంచి n = 3 శక్తి స్థాయికి పరివర్తనం n = చెందినప్పుడు ఉద్గారమయ్యే కాంతి తరంగదైర్ఘ్యం ఎంత?
జవాబు:
R = 1,09,677 cm-1
n1 = 3
n2 = 5
\(\overline{\mathrm{υ}}\) = 7799.25 cm-1

ప్రశ్న 2.
ఒక మూలకపు పరాణువులో 29 ఎలక్ట్రాన్లు, 35 న్యూట్రాన్లు ఉన్నాయి.
i) ప్రోటాన్ల సంఖ్యను,
ii) మూలకం ఎలక్ట్రాన్ విన్యాసాన్ని రాబట్టండి.
జవాబు:
ఎలక్ట్రాన్ల సంఖ్య 29 ఇవ్వబడినది
i) ప్రోటాన్ ల సంఖ్య = 29
ii) 2 = 29, మూలకం ‘Cu’
ఎలక్ట్రాన్ విన్యాసం = 1s² 2s² 2p² 3s² 3p64s¹ 3d10
ప్రశ్న 3.
ఈ కింది క్వాంటమ్ సంఖ్యల సమితులు అసాధ్యమైనవేవి ? కారణాలతో వివరించండి.
(a) n = 0, l = o, ml = 0, ms = +\(\frac{1}{2}\)
(b) n = 1, l = 0, ml = 0, ms = –\(\frac{1}{2}\)
(c) n = 1, l = 1, ml = 0, ms = +\(\frac{1}{2}\)
(d) n = 2, l = 1, ml = 0, ms = +\(\frac{1}{2}\)
(e) n = 3, l = 3, ml = -3, ms = +\(\frac{1}{2}\)
(f) n = 3, l = 1, ml = 0, ms = +\(\frac{1}{2}\)
జవాబు:
ఈ క్రింది క్వాంటమ్ సంఖ్యల సమితులు సాధ్యం కావు.
a) n = 0, 1 = 0, ml = 0, ms = +\(\frac{1}{2}\)
కారణము :
ప్రధాన క్వాంటమ్ సంఖ్య (n) విలువలు 1 నుంచి n వరకు ఉంటాయి ‘n’ కు సున్న విలువ ఉండదు కాని n = 0 అని ఇవ్వబడినది.
c) n = 1, l = 1, ml = 0, ms = +\(\frac{1}{2}\)
కారణము :
‘l’ విలువలు 0 నుండి (n – 1) వరకు ఉంటాయి.
అంటే n = 1 అయితే l = 0 అవుతుంది. కానీ ‘1’ అవ్వదు.
e) n = 3, l = 3, m, = -3, ms = +\(\frac{1}{2}\)
కారణము :
n = 3, కి ‘l’ విలువలు 0, 1, 2, అవుతాయి కాని ‘3’ అవ్వదు.
![]()
ప్రశ్న 4.
హైడ్రోజన్ పరమాణువు బోర్ కక్ష్యలో తిరుగుతున్న ఎలక్ట్రాన్ కక్ష్య చుట్టుకొలత డీబ్రోలీ తరంగదైర్ఘ్యానికి పూర్ణాంక గుణిజంగా ఉంటుందని చూపించండి.
జవాబు:
బోర్ పరమాణు నమూన – డీట్రోలీ భావన :
బోర్ తన నమూనాలో ఎలక్ట్రాన్ కోణీయ ద్రవ్యవేగం క్వాంటీకరణం చేయబడింది అన్నాడేగాని దానికి కారణం చెప్పలేదు. డీబ్రోలీ తన భావనలో, పరమాణు కక్ష్యలో ఎలక్ట్రాన్ స్థావర తరంగం వలె ప్రవర్తిస్తుంది అని చెప్పి కోణీయ ద్రవ్యవేగం యొక్క క్వాంటీకరణాన్ని విశదీకరించాడు. బోర్ ప్రకారం,
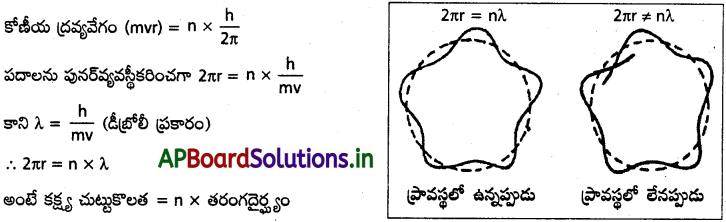
ఈ నిబంధన పరమాణు కక్ష్యలో ఎలక్ట్రాన్ స్థావర తరంగం వలె ప్రవర్తిస్తుందని తెలియజేస్తుంది.
ఎలక్ట్రాన్ తరంగం యొక్క రెండు కొసలు పటంలో చూపినట్లుగా ఒక దానితో ఒకటి కలిసి కక్ష్యలో అవిరళంగా శృంగాలు, ద్రోణులు ఏకాంతర క్రమంలో ఉంటే అట్టి తరంగాన్ని ప్రావస్థలో ఉన్న స్థావర తరంగం అంటారు.
ప్రశ్న 5.
589.0, 589.6 mm లు గరిష్ఠ ద్వంద్వ శోషణ పరివర్తన తరంగదైర్ఘ్యాలుగా పరిశీలించబడ్డాయి. పరివర్తన పౌనఃపున్యాలను, రెండు ఉత్తేజస్థితుల మధ్య శక్తి తేడాలను లెక్కించండి.
జవాబు:

ప్రశ్న 7.
పరమాణువు క్వాంటమ్ యాంత్రిక నమూనా ముఖ్య లక్షణాలు ఏమిటి?
జవాబు:
పరమాణు క్వాంటమ్ యాంత్రిక నమూనా – ముఖ్య లక్షణాలు :
- పరమాణువులోని ఎలక్ట్రాన్ల శక్తి క్వాంటీకృతమయి ఉంటుంది.
- ఎలక్ట్రాన్లు క్వాంటీకృత శక్తి స్థాయిలు ఉండటానికి కారణాలు ఎలక్ట్రానుకు తరంగదైర్ఘ్యాలు ఉండటంతో పాటు ప్రోడింగల్ తరహా సమీకరణానికి ఆమోదయోగ్యమైన విలువలు కూడా ఉండడం.
- పరమాణువులో ఉన్న ఎలక్ట్రాన్ సమాచారం అంతా ఆర్బిటాల్ తరంగ ప్రమేయం ‘Ψ’ లోనే ఉంటుంది. ఆ సమాచార సారాన్ని క్వాంటమ్ యాంత్రిక శాస్త్రం ద్వారా బయటికి తీయడం సాధ్యమవుతుంది.
- ఎలక్ట్రాన్ మార్గాన్ని కచ్చితంగా కనుగొనలేము. కాబట్టి పరమాణువు చుట్టూ ఉన్న త్రిజామితీయ ప్రదేశంలో వేరు వేరు బిందువుల వద్ద ఎలక్ట్రాన్ సంభావ్యతను మాత్రమే కనుగొనవచ్చు.
- పరమాణువులో ఏదైనా ఒక బిందువు వద్ద ఎలక్ట్రాన్ను కనుగొనే సంభావ్యత, ఆర్బిటాల్ తరంగ ప్రమేయ వర్గానికి (Ψ)² అనులోమానుపాతంలో ఉంటుంది. Ψ² ను సంభావ్యతా సాంద్రత అంటారు. ఇది ఎప్పుడు ధన విలువై ఉంటుంది.
పరమాణువులో వేరు వేరు బిందువుల వద్ద సంభావ్యతా సాంద్రత, Ψ² విలువలు తెలిసినట్లయితే కేంద్రకం చుట్టూ ఎలక్ట్రాన్ ఉండే గరిష్ట సంభావ్యత గల ప్రదేశాన్ని గుర్తించవచ్చు.
ప్రశ్న 8.
నోడల్ తలం అంటే ఏమిటి? 2p, 3d – ఆర్బిటాల్లలో ఎన్ని నోడల్ తలాలుంటాయి?
జవాబు:
నోడల్ తలం :
ఎలక్ట్రాను కనుగొనే సంభావ్యత శూన్యమయిన (Ψ² = 0) ఉపరితలాన్ని నోడల్ తలం (లేక) నిర్ణీత తలం అందురు. నోడల్ తలాల సంఖ్య ఆ ఆర్బిటాల్ యొక్క ‘l’ విలువకు సమానం.
ఉదా : 2p – ఆర్బిటాల్కు నోడల్ తలాల సంఖ్య = 1
3d – ఆర్బిటాల్కు నోడల్ తలాల సంఖ్య = 2
ప్రశ్న 9.
91.2 nm నుంచి 121.6 nm ల మధ్య లైమన్ శ్రేణి, 364.7 nm నుంచి 656.5 nm ల మధ్య బామర్శ్రేణి, 820.6 nm నుంచి 1876 pm ల మధ్య పాశ్చన్ శ్రేణి కనబడతాయి. ఈ తరంగదైర్ఘ్యాలు వర్ణపటంలో ఏ ప్రాంతానికి చెందినవో కనుక్కోండి.
జవాబు:
విద్యుదయస్కాంత వర్ణపటంలో
a) 91.2 – 121.6 nm (లైమన్ శ్రేణి) అతినీలలోహిత (Ultraviolet) ప్రాంతానికి చెందినది.
b) 364.7 – 656.5 nm (బామర్ శ్రేణి) దృగ్గోచర (Visible) ప్రాంతానికి చెందినది.
c) 820.6 – 1876 nm (పాశ్చన్ శ్రేణి) పరారుణ (Infrared) ప్రాంతానికి చెందినది.
ప్రశ్న 10.
హైడ్రోజన్ పరమాణువులో n. l, m, క్వాంటమ్ సంఖ్యలు ఎలా వస్తాయి?
జవాబు:
హైడ్రోజన్ ఎలక్ట్రాన్ విన్యాసం 1s¹
1s¹ కు n = 1
1 = 0
ml = 0
ms = + ½
![]()
ప్రశ్న 11.
హైడ్రోజన్ పరమాణువులో లైమన్ శ్రేణిలో ఒక రేఖ తరంగదైర్ఘ్యం 1.03 × 10-7 m అయితే ఎలక్ట్రాన్ తొలి శక్తిస్థాయి ఏది?
జవాబు:
దత్తాంశము, λ = 1.03 × 10-7 m = 1.03 × 10-5 cm
లైమన్ శ్రేణికి, n2 = 1
R = 109677 cm-1
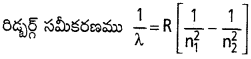

ప్రశ్న 12.
ఎలక్ట్రాన్ స్థితిని ±0.002 nm లోపు కచ్చితంగా కొలవగలిగినట్లైతే ఎలక్ట్రాన్ ద్రవ్యవేగంలో అనిశ్చితత్వం గణించండి.
జవాబు:
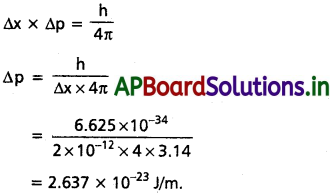
∆x = 0.002 nm ఇవ్వబడినది
సూత్రము
ప్రశ్న 13.
1.6 × 106 m/s-1 ఎలక్ట్రాన్ వేగం ఉన్నట్లయితే దానితో ఉన్న డీబ్రోలీ తరంగదైర్ఘ్యాన్ని గణించండి.
జవాబు:
V = 1.6 × 106 m/sec ఇవ్వబడినది

ప్రశ్న 14.
శోషణ, ఉద్గార వర్ణపటాల మధ్య తేడాలను వివరించండి. [AP.Mar. ’15]
జవాబు:
| ఉద్గార వర్ణపటం | శోషణ వర్ణపటం |
| 1. శక్తి ఉద్గారం వలన ఏర్పడుతుంది. | 1. శక్తి శోషణ వలన ఏర్పడుతుంది. |
| 2. దీనిలో నల్లని పట్టీపై ప్రకాశవంతమైన గీతలు ఏర్పడతాయి. | 2. దీనిలో ప్రకాశవంతమైన పట్టీపై నల్లని గీతలు ఏర్పడతాయి. |
| 3. ఎలక్ట్రాన్లు పై శక్తి స్థాయి నుండి క్రింది శక్తి స్థాయి లోనికి దూకినపుడు ఈ వర్ణపటం ఏర్పడుతుంది. | 3. ఎలక్ట్రాన్లు క్రింది శక్తి స్థాయి నుండి పై శక్తి స్థాయి లోనికి దూకినపుడు ఈ వర్ణపటం ఏర్పడుతుంది. |
ప్రశ్న 15.
ఎలక్ట్రాన్ల క్వాంటమ్ సంఖ్యలు కింద ఇవ్వడమైంది. వాటిని శక్తిపరంగా ఆరోహణ క్రమంలో రాయండి.
(a) n = 4, l = 2, ml = -2, ms = +\(\frac{1}{2}\)
(b) n = 3, l = 2, ml = -1, ms = –\(\frac{1}{2}\)
(c) n = 4, l = 1, ml = 0, ms = +\(\frac{1}{2}\)
(d) n = 3, l = 2, ml = -1, ms = –\(\frac{1}{2}\)
జవాబు:
ఆర్బిటాల్ యొక్క శక్తికి ఫార్ములా (n + 1)
∴ ఇవ్వబడిన ప్రతి సంయోగానికి (n + 1) విలువలు
(1) కి n + l = 4 + 2 = 6
(2) కి n + l = 3 + 2 = 5
(3) కి n + l = 4 + 1 = 5
(4) కి n + l = 3 + 2 = 5
(5) కి n + l = 3+1 = 4
(6) కి n + 1 = 4+1 = 5
- (n + 1) విలువ తక్కువ ఉంటే, ఆ స్థాయి శక్తి తక్కువ.
- (n + l) విలువలు సమానంగా ఉన్నప్పుడు, దేనికైతే తక్కువ ‘n’ విలువ ఉంటుందో ఆ ఆర్బిటాల్ యొక్క శక్తి తక్కువ.
ప్రశ్న 16.
సీజియం పరమాణువు పని ప్రమేయం 1.9 eV. ఆరంభ వికిరణాల పౌనఃపున్యాన్ని గణించండి. సీజియం మూలకాన్ని 500 nm ల తరంగదైర్ఘ్యం గల వికిరణాలతో ఉద్యోతనం (irradiation) చేస్తే వెలువడే ఫోటో ఎలక్ట్రాన్ గతిజశక్తి గణించండి.
జవాబు:
Case – I
కాంతి విద్యుత్ ఫలిత సమీకరణం
hυ = hυ0 + ½mv²
w = hυ0

ప్రశ్న 17.
1.3225 nm వ్యాసార్థం గల కక్ష్యలో మొదలై 211.6 pm వ్యాసార్థం గల కక్ష్యలో చేరినట్లయితే ఉద్గార పరివర్తన తరంగదైర్ఘ్యాన్ని గణించండి. ఈ పరివర్తన ఏ శ్రేణికి చెందుతుంది ? అది వర్ణపటంలో “ఏ ప్రాంతానికి చెందుతుంది?
జవాబు:
ఏ కక్ష్య నుండి మొదలైనదో ఆ కక్ష్య వ్యాసార్థం 1.35225pm గా ఇవ్వబడినది.
∴ r = 1.35225 × 10-9 m = 13.225 Å
r = 0.529 × n²
n² = \(\frac{13.225}{0.529}\) = 25
n = 5
పరివర్తనం ముగిసిన కక్ష్య వ్యాసార్ధం = 211.6 pm = 2.116 Å
∴ n² = \(\frac{2.116}{0.529}\) = 4
n² = 4 ⇒n= 2
పరివర్తనం n = 5 నుండి n = 2 కు జరిగినది.
కావున వర్ణపట రేఖలు బామర్ శ్రేణిలో ఏర్పడును. (దృగ్గోచర ప్రాంతం)
![]()
ప్రశ్న 18.
కక్ష్య (ఆర్బిట్)కు, ఆర్బిటాల్కు గల భేదాన్ని వివరించండి.
జవాబు:
| కక్ష్య | ఆర్బిటాల్ |
| 1. కేంద్రకం చుట్టూ ఎలక్ట్రాన్లు తిరిగేటటువంటి వృత్తాకార మార్గాలను కక్ష్య అంటారు. | 1. ఎలక్ట్రాన్ కనుగొను సంభావ్యత అధికంగా గల త్రిజామితీయ ప్రదేశంను ఆర్బిటాల్ అంటారు. |
| 2. ఇవి దిశారహితమైనది. | 2. వీటికి నిర్దిష్టమైన ఆకృతి కలిగి ఉంటాయి. వీటికి దిశ ఉంటుంది. (s – ఆర్బిటాల్ తప్ప) |
| 3. ఇవ్వబడిన ‘n’ విలువ (కక్ష్య)కు మొత్తం ఎలక్ట్రాన్ల సంఖ్య 2n². | 3. ప్రతి ఆర్బిటాల్ రెండు ఎలక్ట్రాన్లతో నింపబడును. |
ప్రశ్న 19.
కాంతి విద్యుత్ ప్రభావాన్ని వివరించండి.
జవాబు:
కాంతికిరణం పౌనఃపున్యంపై కాంతి విద్యుత్ ప్రభావం ఆధారపడి ఉండటానికి గల కారణాన్ని ఐన్స్టీన్ తన సాధారణీకృత క్వాంటమ్ సిద్ధాంతం ద్వారా వివరించాడు. కాంతిని కణాల సముదాయంగా భావిస్తే, కాంతి కణం లేదా ఫోటాను శక్తి (E) పౌనః పున్యానికి (υ) అనులోమానుపాతంలో ఉంటుందని, ఆ సంబంధం E = hυ గా ఉంటుందని గుర్తించారు. లోహం నుంచి ఎలక్ట్రాను బయటకు తొలగించడానికి అవసరమైన శక్తి ఫోటాన్కు ఉంటే లోహంతో ఈ ఫోటాన్ ఢీకొన్నప్పుడు లోహం నుంచి ఎలక్ట్రాన్ బహిర్గతమవుతుందని ఐన్స్టీన్ భావించాడు.
ఊదారంగు కాంతి ఫోటాన్కు శక్తి క్వాంటమ్ విలువ, ఎరుపు కాంతి ఫోటాన్ల శక్తి క్వాంటమ్ విలువ కంటే ఎక్కువ. కాబట్టి పొటాషియమ్ లోహం నుంచి ఎలక్ట్రాన్ బహిర్గతం చేయడానికి అవసరమయ్యే శక్తి, ఎరుపు కాంతి ఫోటాన్కు లేదని ఊదాకాంతి ఫోటాను ఉన్నదని తెలుస్తుంది. ఒక ఫోటాన్ లోహపు ఉపరితలాన్ని ఢీకొన్నప్పుడు, ఫోటాన్ శక్తిని ఎలక్ట్రాన్ గ్రహిస్తుంది. ఈ శక్తిలో కొంత భాగం, విడుదలైన ఎలక్ట్రాన్ గతిజశక్తిగా మారుతుంది. కాబట్టి
hυ = W + KE ⇒ hυ = hυ0 + \(\frac{1}{2}\)mev²
hυ = ఫోటాన్ శక్తి
υ0= ఆరంభ పౌనఃపున్యము
v = విడుదలైన ఎలక్ట్రాన్ వేగం
me = ఎలక్ట్రాన్ ద్రవ్యరాశి
W = లోహంలో, ఎలక్ట్రాన్ల మీద గల ఆకర్షణ బలాలను అధిగమించే శక్తి K.E. = విడుదలైన ఎలక్ట్రాన్ గతిజశక్తి
ఈ విధంగా కాంతి విద్యుత్ ప్రభావానికి సరైన వివరణ ఐన్స్టీన్ ఇచ్చాడు.
దీర్ఘ సమాధాన ప్రశ్నలు
ప్రశ్న 1.
రూథర్ ఫర్డ్ పరమాణువు కేంద్రక నమూనాను వివరించండి. దానిలోని లోపాలు ఏమిటి?
జవాబు:
బంగారు రేకు ప్రయోగం (Gold foil experiment) నుంచి వచ్చిన ఫలితాల ఆధారంగా రూథర్ఫర్డ్ క్రింది విషయాలను గమనించడం జరిగింది.
- చాలా వరకు α – కణాలు అపవర్తనం చెందకుండానే బంగారు రేకు నుంచి వెళ్ళిపోయాయి.
- తక్కువ భాగం α – కణాలు కొద్దికోణంలో అపవర్తనం చెందాయి.
- అత్యల్ప భాగం α – కణాలు 180° కోణంలో అపవర్తనం చెంది వెనుతిరగడం గమనించారు.
పై పరిశీలనలో ఆధారంగా రూథర్ఫర్డ్ పరమాణు నిర్మాణం గురించి క్రింది నిర్ణయాలు తీసుకున్నాడు.
అవి
1. పరమాణువులో ఎక్కువ ప్రదేశం ఖాళీగానే వుంటుంది. 2. తక్కువ ధనావేశ α – కణాలు అపవర్తనం చెందాయి. ఇది వికర్షణ వల్ల జరుగుతుంది. ధనావేశం చాలా కొద్ది ఘనపరిమాణంలో సాంద్రీకృతమై ఉండడం వల్ల నేరుగా ధనావేశం మీదికి వెళ్లే α – కణాలను వచ్చిన దిశగానే అపవర్తనం చెందించగలిగింది.
పై పరిశీలనల ఆధారంగా రూథర్ఫర్డ్ కేంద్రక నమూనాను ప్రతిపాదించాడు.
రూథర్ ఫర్డ్ సౌరకుటుంబ పరమాణు నమూనా – ప్రతిపాదనలు :
- పరమాణువులో ధనావేశం అంతా కొద్ది ప్రాంతంలో సాంద్రీకృతమై ఉంటుంది. దానిని కేంద్రకం అంటారు.
- కేంద్రకం చుట్టూ ఎలక్ట్రాన్లు గుండ్రంగా తిరుగుతుంటాయి. ఎలక్ట్రాన్లు తిరిగే ఈ మార్గానే కక్ష్యలు అంటారు. ఈ విధంగా, రూథర్ ఫర్డ్ నమూనా సౌరకుటుంబాన్ని పోలి ఉంటుంది.
- ఎలక్ట్రాన్లు, కేంద్రకమూ స్థిరవిద్యుత్ బలాల ఆకర్షణ వల్ల దగ్గరగా ఉంటాయి.
రూథర్ ఫర్డ్ నమూనాలో లోపాలు :
- విద్యుత్ గతిశాస్త్ర నియమాల ప్రకారం ఎలక్ట్రాన్ వంటి ఆవేశపూరిత కణం వృత్తాకార మార్గాలలో తిరుగుతూ కేంద్రక ఆకర్షణ వలన శక్తిని క్రమంగా కోల్పోయి కేంద్రకంలో పడిపోవాలి. కానీ ఆవిధంగా జరగక పరమాణువు విద్యుత్ తటస్థం కలిగి స్థిరంగా ఉంది. ఆ విధంగా రూథర్ఫర్డ్ నమూనా పరమాణు స్థిరత్వాన్ని విశదీకరించలేకపోయింది.
- ఒకవేళ ఎలక్ట్రాన్ కేంద్రకం చుట్టూ స్థిరంగా ఉన్నట్లయితే, ఎలక్ట్రాన్ కూ కేంద్రానికీ మధ్య ఉన్న స్థిర విద్యుదాకర్షణ వల్ల, ఎలక్ట్రాన్ కేంద్రకం వైపు లోబడాలి. కానీ ఈ విధంగా జరగడం లేదు.
- ఈ నమూనా, పరమాణువులో ఎలక్ట్రాన్ నిర్మాణాన్ని విశదీకరించలేదు. అంటే శక్తి స్థాయిల్లో ఎలక్ట్రాన్ పంపిణీ గురించి తెలుపలేదు.
ప్రశ్న 2.
ప్లాంక్స్ క్వాంటమ్ సిద్ధాంతాన్ని సంక్షిప్తంగా వివరించండి.
జవాబు:
ప్లాంక్ సిద్ధాంతంలోని ప్రతిపాదనలు :
1. ఎలక్ట్రాన్ వంటి ఆవేశపూరిత కణాలు, కంపనాలు చేయటం వలన శక్తి ఉద్గారం జరుగుతుంది.
2. ఉద్గారించబడిన శక్తి, అవిచ్ఛిన్నంగా కాక కొంత శక్తి ప్యాకెట్ల రూపంలో ఉంటుంది. ఈ శక్తి ప్యాకెట్నే క్వాంటం అంటారు.
3. ఉద్గారించబడిన శక్తి తరంగాల రూపంలో విస్తరిస్తుంది.
4. ఒక్కొక్క క్వాంటంలో ఇమిడి ఉన్న శక్తిని ఈ క్రింది సమీకరణంతో సూచిస్తారు.
E = hυ (లేక) E nhυ
ఇచ్చట h = ప్లాంక్ స్థిరాంకం (6.625 × 10-27 ఎర్గ్ – సెకన్), n = పూర్ణాంకం, υ = కణం పౌనఃపున్యము.
5. శక్తి ఉద్గారం లేక శోషణం, ఒక క్వాంటం లేక క్వాంటం యొక్క సరళపూర్ణ గుణిజాలుగా మాత్రమే జరుగుతుంది. దీనినే శక్తి క్వాంటీకరణం అంటారు.
ప్లాంక్ స్థిరాంకానికి వివిధ ప్రమాణాలు :
- 6.625 × 10-27 ఎర్గ్ – సెకన్
- 6.625 × 10-34 జౌల్ – సెకన్
- 1.58 × 10-34 కాలరీ – సెకన్
ప్లాంక్ క్వాంటం సిద్ధాంతం యొక్క విజయము :
కృష్ణ పదార్థం నుంచి ఉద్గారమయ్యే వికిరణాలను విజయవంతంగా ప్లాంక్ సిద్ధాంతం వివరించింది. వికిరణాల శక్తిని సంపూర్ణంగా శోషించుకొనే (లేదా) వికిరణాల శక్తిని సంపూర్ణంగా ఉద్గారించే పదార్థాన్ని కృష్ణ పదార్థం అంటారు.
ప్రశ్న 3.
హైడ్రోజన్ పరమాణువు బోర్ నమూనా ప్రతిపాదనలు ఏమిటి? [A.P. Mar. 15 Mar. 13]
జవాబు:
- బోర్ తన సిద్ధాంతం ద్వారా హైడ్రోజన్ పరమాణు నిర్మాణం మరియు వర్ణపటంలోని ముఖ్యాంశాలను వివరించాడు.
- బోర్ సిద్ధాంతం పరమాణు నిర్మాణం, వర్ణపటాలలోని చాలా విషయాలు హేతుబద్ధకంగా వివరిస్తుంది.
ముఖ్యాంశాలు :
- హైడ్రోజన్ పరమాణువులోని ఎలక్ట్రాన్ కేంద్రకం నుండి స్థిర వ్యాసార్థాలు గల వృత్తాకార మార్గాలతో నిర్ణీత శక్తులతో తిరుగుతూ ఉండును. ఈ వృత్తాకార మార్గాలను స్థిర స్థితులు (లేక) కక్ష్యలు (లేక) అనుమతించదగ్గ శక్తిస్థాయిలు అంటారు.
- కక్ష్యలో తిరిగే ఎలక్ట్రాన్ శక్తి స్థిరంగా ఉంటుంది. కాలంతో మారదు.
- ఎలక్ట్రాన్ ఒక కక్ష్య నుండి మరియొక కక్ష్యకు పోయినపుడు శక్తి మార్పు వస్తుంది.
a) ఎలక్ట్రాన్ కింది స్థిర స్థితి నుండి పై స్థిర స్థితికి పోయినపుడు శక్తిని శోషించుకొనును.
b) ఎలక్ట్రాన్పై స్థిర స్థితి నుండి క్రింది స్థిర స్థితికి పోయినపుడు శక్తిని ఉద్గారించుకొనును.
ఆ రెండు స్థిర స్థితులు శక్తి భేదం ∆E = E2 – E1 = hυ
పౌనఃపున్యం υ = \(\frac{E_2-E_1}{h}\)
E1 మరియు E2 లు కింది మరియు పై స్థితుల శక్తులు - ఎలక్ట్రాన్ యొక్క కోణీయ ద్రవ్యవేగం mvr = \(\frac{nh}{2 \pi}\)
ఎలక్ట్రాన్ కోణీయ ద్రవ్యవేగం \(\frac{h}{2 \pi}\) విలువకు పూర్ణాంక గుణిజంగా ఉండే కక్ష్యలలో మాత్రమే తిరుగుతుంది.
బోర్ సిద్ధాంతం ద్వారా హైడ్రోజన్ వర్ణపట రేఖల వివరణ :
→ హైడ్రోజన్ పరమాణువునందు వర్ణపట రేఖలు బోర్ సిద్ధాంతం ద్వారా వివరించబడ్డాయి.
→ బోర్ సిద్ధాంతం ప్రకారం రెండు స్థిర స్థాయిల మధ్య ఎలక్ట్రాన్ పరివర్తనం జరిగినపుడు

- శోషణ వర్ణపటం nf > n1 (శక్తి శోషించబడును (+Ve))
- ఉద్గార వర్ణపటం ni > nf (శక్తి ఉద్గారించబడును (- Ve))
- శోషణలో గాని, ఉద్గారంలో గాని ప్రతి రేఖ కూడా హైడ్రోజన్ పరమాణువులో ఒక ప్రత్యేకమైన పరివర్తన ద్వారానే వస్తుంది.
- హైడ్రోజన్ పరమాణువులు ఎక్కువ సంఖ్యలో ఉన్నట్లయితే ఎక్కువ సంఖ్యలో వర్ణపట రేఖలు ఏర్పడతాయి.
![]()
ప్రశ్న 4.
హైడ్రోజన్ పరమాణువుకు బోర్ సిద్ధాంత విజయాలను వివరించండి.
జవాబు:
హైడ్రోజన్ పరమాణువుకు బోర్ సిద్ధాంత విజయాలు :
→ బోర్ సిద్ధాంతం ప్రధాన క్వాంటం సంఖ్య గురించి వివరణ ఇచ్చినది. ఎలక్ట్రాన్ స్థిర కక్ష్యల సంఖ్యలు n = 1,2,3,…..లు ప్రధాన క్వాంటం సంఖ్యలు.
→ బోర్ సిద్ధాంతం ద్వారా కక్ష్య పరిమాణం, కక్ష్య వ్యాసార్ధంలు గురించి వివరించబడ్డాయి.
r = 0.529 × n² Å
r = 52.9 × n² pm
→ బోర్ సిద్ధాంతం ద్వారా ఎలక్ట్రాన్ శక్తి గురించి తెలపటం జరిగింది.
En = – RH(\(\frac{1}{n^2}\)) n = 1, 2, 3, …….
RH = రిడ్ బర్గ్ స్థిరాంకం
= 1,09,677 cm-1
→ ఈ సిద్ధాంతం హైడ్రోజన్ యొక్క రేఖా వర్ణపటం వివరించినది.
→ ఈ సిద్ధాంతం He+, Li+2, Be+3 వంటి అయాన్లకు కూడా అనువర్తింపబడుతుంది.
→ కక్ష్యలలో తిరుగు ఎలక్ట్రాన్ల వేగం గురించి వివరణ ఇచ్చినది.
ప్రశ్న 5.
పరమాణువు క్వాంటమ్ యాంత్రిక నమూనా సిద్ధాంతానికి దారితీసిన కారణాలను వివరించండి.
జవాబు:
- సంప్రదాయ యాంత్రిక శాస్త్రం స్థూల వస్తువుల చలనాన్ని విజయవంతంగా వివరించినది. ఉదా : కిందపడే రాయి, గ్రహాలు.
- సంప్రదాయ యాంత్రిక శాస్త్రం ద్వారా ఎలక్ట్రాన్, పరమాణువుల వంటి సూక్ష్మమైన కణాల చలనాన్ని వివరించలేకపోయినది.
- ఈ శాస్త్రం పదార్థ ద్వంద్వ స్వభావాన్ని వివరించలేకపోయినది.
క్వాంటమ్ యాంత్రిక శాస్త్రం :
- పదార్థాల ద్వంద్వ స్వభావాన్ని పరిగణనలోనికి తీసుకొనే శాస్త్రాన్ని క్వాంటమ్ యాంత్రిక శాస్త్రం అంటారు.
- ఇది ఎలక్ట్రాన్ వంటి సూక్ష్మమైన కణాల చలనాన్ని వివరిస్తుంది.
పరమాణు క్వాంటమ్ యాంత్రిక నమూనా – ముఖ్య లక్షణాలు :
- పరమాణువులోని ఎలక్ట్రాన్ల శక్తి క్వాంటీకృతమయి ఉంటుంది.
- ఎలక్ట్రాను క్వాంటీకృత శక్తి స్థాయిలు ఉండటానికి కారణాలు ఎలక్ట్రానుకు తరంగదైర్ఘ్యాలు ఉండటంతో పాటు ప్రోడింగల్ తరహా సమీకరణానికి ఆమోదయోగ్యమైన విలువలు కూడా ఉండడం.
- పరమాణువులో ఉన్న ఎలక్ట్రాన్ సమాచారం అంతా ఆర్బిటాల్ తరంగ ప్రమేయం ‘Ψ’ లోనే ఉంటుంది. ఆ సమాచార సారాన్ని క్వాంటమ్ యాంత్రిక శాస్త్రం ద్వారా బయటికి తీయడం సాధ్యమవుతుంది.
- ఎలక్ట్రాన్ మార్గాన్ని కచ్చితంగా కనుగొనలేము. కాబట్టి పరమాణువు చుట్టూ ఉన్న త్రిజామితీయ ప్రదేశంలో వేరు వేరు బిందువుల వద్ద ఎలక్ట్రాన్ సంభావ్యతను మాత్రమే కనుగొనవచ్చు.
- పరమాణువులో ఏదైనా ఒక బిందువు వద్ద ఎలక్ట్రాను కనుగొనే సంభావ్యత, ఆర్బిటాల్ తరంగ ప్రమేయ వర్గానికి (Ψ)² అనులోమానుపాతంలో ఉంటుంది. Ψ² ను సంభావ్యతా సాంద్రత అంటారు. ఇది ఎప్పుడు ధన విలువై ఉంటుంది.
పరమాణువులో వేరు వేరు బిందువుల వద్ద సంభావ్యతా సాంద్రత, Ψ² విలువలు తెలిసినట్లయితే కేంద్రకం చుట్టూ ఎలక్ట్రాన్ ఉండే గరిష్ట సంభావ్యత గల ప్రదేశాన్ని గుర్తించవచ్చు.
ప్రశ్న 6.
పరమాణు క్వాంటమ్ యాంత్రిక నమూనా ముఖ్య లక్షణాలను వివరించండి.
జవాబు:
పరమాణు క్వాంటమ్ యాంత్రిక నమూనా – ముఖ్య లక్షణాలు :
- పరమాణువులోని ఎలక్ట్రాన్ల శక్తి క్వాంటీకృతమయి ఉంటుంది.
- ఎలక్ట్రాను క్వాంటీకృత శక్తి స్థాయిలు ఉండటానికి కారణాలు ఎలక్ట్రానుకు తరంగదైర్ఘ్యాలు ఉండటంతో పాటు ప్రోడింగల్ తరహా సమీకరణానికి ఆమోదయోగ్యమైన విలువలు కూడా ఉండడం.
- పరమాణువులో ఉన్న ఎలక్ట్రాన్ సమాచారం అంతా ఆర్బిటాల్ తరంగ ప్రమేయం ‘Ψ’ లోనే ఉంటుంది. ఆ సమాచార సారాన్ని క్వాంటమ్ యాంత్రిక శాస్త్రం ద్వారా బయటికి తీయడం సాధ్యమవుతుంది.
- ఎలక్ట్రాన్ మార్గాన్ని కచ్చితంగా కనుగొనలేము. కాబట్టి పరమాణువు చుట్టూ ఉన్న త్రిజామితీయ ప్రదేశంలో వేరు వేరు బిందువుల వద్ద ఎలక్ట్రాన్ సంభావ్యతను మాత్రమే కనుగొనవచ్చు.
- పరమాణువులో ఏదైనా ఒక బిందువు వద్ద ఎలక్ట్రాన్ను కనుగొనే సంభావ్యత, ఆర్బిటాల్ తరంగ ప్రమేయ వర్గానికి (Ψ)² అనులోమానుపాతంలో ఉంటుంది. Ψ² ను సంభావ్యతా సాంద్రత అంటారు. ఇది ఎప్పుడు ధన విలువై ఉంటుంది.
పరమాణువులో వేరు వేరు బిందువుల వద్ద సంభావ్యతా సాంద్రత, Ψ² విలువలు తెలిసినట్లయితే కేంద్రకం చుట్టూ ఎలక్ట్రాన్ ఉండే గరిష్ఠ సంభావ్యత గల ప్రదేశాన్ని గుర్తించవచ్చు.
ప్రశ్న 7.
బోర్ పరమాణు నమూనాలోని లోపాలు ఏమిటి? [A.P. Mar. ’15 Mar. ’13]
జవాబు:
బోర్ పరమాణు నమూనా – లోపాలు :
- ఒకటి కన్నా ఎక్కువ ఎలక్ట్రాన్లు గల పరమాణువు లేదా అయాన్ వర్ణపటాన్ని బోర్ నమూనా వివరించలేదు.
- బోర్ నమూనా హైడ్రోజన్ సూక్ష్మ వర్ణపటాన్ని వివరించలేదు (రేఖా వర్ణపటంలో ఒక గీత అనేక గీతల సంపుటి. ఇదే సూక్ష్మ వర్గపటం)
- జీమన్ ఫలితాన్ని మరియు స్టార్క్ ఫలితాన్ని వివరించలేదు.
- ఎలక్ట్రాన్ యొక్క ద్వంద్వ స్వభావాన్ని వివరించలేదు.
- ఎలక్ట్రాన్ యొక్క కోణీయ ద్రవ్యవేగం \(\frac{h}{2 \pi}\)కు సరళ పూర్ణాంక గుణిజాలుగా ఉండవలెనని బోర్ ప్రతిపాదించాడు. కాని దీనికి కారణం సరిగా వివరించలేదు.
- ఈ నమూనా పరమాణువులు, వాటిలోని కక్ష్యలు సమతలంలో ఉన్నాయనే భావనను ఇస్తుంది. ఇది తప్పు.
- రసాయన బంధాల ద్వారా అణువులను ఏర్పరిచే పరమాణువుల సామర్థ్యాన్ని కూడా బోర్ నమూనా వివరించలేదు.
గమనిక :
ఎ) జీమన్ ఫలితము :
హైడ్రోజన్ వాయువును బాహ్య అయస్కాంత క్షేత్ర ప్రభావానికి గురిచేసి, హైడ్రోజన్ వర్ణపటాన్ని నమోదు చేసినపుడు వర్ణపటంలోని ప్రతి గీత సున్నితపు గీతల సంపుటిగా చీలడం కనిపించింది. దీనినే జీమన్ ఫలితం అంటారు.
బి) స్టార్క్ ఫలితము :
విద్యుత్ క్షేత్ర ప్రభావంతో హైడ్రోజన్ వాయువు వర్ణపటం నమోదు చేసినపుడు ప్రతిగీత, సున్నితపు గీతల సంపుటిగా చీలడం కనిపించింది. దీనిని స్టార్క్ ప్రభావం అంటారు.
ప్రశ్న 8.
ఎలక్ట్రాన్ ద్వంద్వ స్వభావానికి రుజువులు ఏమిటి?
జవాబు:
- కాంతి యొక్క కణ స్వభావం కృష్ణ వస్తువు యొక్క వికిరణాలను మరియు కాంతి విద్యుత్ ఫలితాన్ని విజయవంతంగా వివరించినది.
- కాంతి తరంగ స్వభావం వివర్తనం, వ్యతికరణం వంటి ప్రక్రియలను వివరించినది.
- కావున కాంతికి ద్వంద్వ స్వభావం కలదు అనగా తరంగంవలె (లేదా) కణాల ప్రవాహంగా ఉండును.
- డీబ్రోలీ సిద్ధాంతం ప్రకారం కాంతికి ద్వంద్వ స్వభావం ఉండును అనగా కణ మరియు తరంగ స్వభావం.
డీబ్రోలీ సమీకరణం

- హైసన్ బర్గ్ అనిశ్చితత్వ నియమం కూడా ద్వంద్వ స్వభావ ఫలితమే.
అనిశ్చితత్వ నియమం :
“అతివేగంగా ప్రయాణించే ఎలక్ట్రాన్ వంటి సూక్ష్మ పరమాణు కణాల స్థానం, ద్రవ్యవేగం రెండింటినీ ఏక కాలంలో ఖచ్చితంగా నిర్ణయించలేం. స్థాన నిర్ణయంలో అనిశ్చితత్వం (∆x), ద్రవ్యవేగంలో అనిశ్చితత్వం (∆P) అయితే
(∆x) (∆P) ≥ \(\frac{h}{2 \pi}\) (n = 1, 2, 3, 4 ………………..)
హైస్బర్గ్ అనిశ్చితత్వ నియమ ప్రాముఖ్యత :
- ఈ నియమం ప్రకారం, ఎలక్ట్రాన్కగానీ, ఎలక్ట్రాన్ లాంటి ఇతర కణాలకుగానీ స్థిరమైన కక్ష్య లేదా ప్రక్షేపమార్గం ఉండే అవకాశం లేదు.
- ఈ నియమం సూక్ష్మాతి సూక్ష్మకణాలకు మాత్రమే ప్రాముఖ్యం ఇస్తుంది. స్థూలకణాలకు వర్తించదు.
- మిల్లీగ్రాము గాని అంతకంటే బరువైన వస్తువులకు అనిశ్చితత్వంతో ఫలితం ఏమీ ఉండదు.
ప్రశ్న 9.
n, l, ml క్వాంటమ్ సంఖ్యలు ఎలా వచ్చాయి? వాటి ప్రాముఖ్యాన్ని వివరించండి. [T.S. Mar. ’15 Mar. ’14]
జవాబు:
- సాధారణంగా ఎక్కువ సంఖ్యలో పరమాణు ఆర్బిటాళ్లు సాధ్యపడతాయి. ఇవి వాటి పరిమాణం, ఆకృతి మొదలైనవాటి లో విభిన్నత కలిగి యుండును.
- పరమాణు ఆర్బిటాళ్లు క్వాంటం సంఖ్యల ద్వారా భేదపరుస్తారు.
క్వాంటమ్ సంఖ్యలు :
పరమాణువులో ఎలక్ట్రాన్ స్థానాన్ని మరియు శక్తిని పూర్తిగా వివరించుటకు సహాయపడే వాటిని “క్వాంటమ్ సంఖ్యలు” అంటారు. 1. ప్రధాన క్వాంటం సంఖ్య, 2. ఎజిమ్యుథల్ క్వాంటం సంఖ్య, 3. అయస్కాంత క్వాంటం సంఖ్య.
1. ప్రధాన క్వాంటం సంఖ్య (n) :
i) దీనిని ‘నీల్స్ బోర్’ ప్రవేశపెట్టాడు.
ii) ‘n’ అన్నీ పూర్ణాంక విలువలే ఉంటాయి. n = 1, 2, 3,…….. (లేక) K, L, M, N
iii) ప్రాముఖ్యత : ఈ క్వాంటమ్ సంఖ్య కక్ష్య పరిమాణాన్ని దాదాపుగా శక్తిని తెలుపుతుంది. ‘n’ విలువ పెరిగేకొలదీ కక్ష్య పరిమాణము మరియు శక్తి కూడా పెరుగుతాయి.
ఈ క్వాంటమ్ సంఖ్య ఎలక్ట్రాన్ ఏ ప్రధానస్థాయికి చెందినదో తెలుపుతుంది.
2. ఎజిమ్యుథల్ (లేక) కోణీయ ద్రవ్యవేగం (లేక) ఉప క్వాంటమ్ సంఖ్య (l) :
i) దీనిని సోమర్ ఫెల్డ్ ప్రవేశపెట్టాడు.
ii) ‘l’ విలువ ‘n’ పై ఆధారపడి ఉంటుంది. దీని విలువలు ‘0’ నుండి (n – 1) వరకు ఉండును.
ఉదా : n = 4 అయినపుడు ‘l’ విలువలు
l = 0 (s – ఉపస్థాయి)
l = 1 (p – ఉపస్థాయి)
l = 2 (d – ఉపస్థాయి)
l = 3 (f – ఉపస్థాయి)
iii) ప్రాముఖ్యత :
- ఆర్బిటాల్ల త్రిమితీయ ఆకృతిని వివరించును.
- సూక్ష్మ వర్ణ పటాన్ని వివరించును.
3. అయస్కాంత క్వాంటమ్ సంఖ్య (m) :
i) దీనిని ‘లాండే’ ప్రవేశపెట్టాడు.
ii) ‘m’ విలువలు ‘0’ తో కలిపి – l నుండి +l వరకు ఉంటాయి. మొత్తం (2l + 1) విలువలుంటాయి.
ఉదా : 1 = 0 అయితే m = 0
l = 1 అయితే m = -1, 0, + 1
| ఉప కర్పరము | 1 విలువ | m విలువ |
| s | 0 | 0 |
| p | 1 | – 1, 0, +1 |
| d | 2 | -2, -1, 0, +1, +2 |
| F | 3 | −3, −2, −1, 0, +1, +2, +3 |
iii) ప్రాముఖ్యత :
- ఈ క్వాంటమ్ సంఖ్య ఆర్బిటాల్ల ప్రాదేశిక దిగ్విన్యాసాలను తెలుపుతుంది.
- జీమన్ మరియు స్టార్క్ ఫలితాలను వివరించును.
ప్రశ్న 62.
పదార్థం ద్వంద్వ స్వభావాన్ని వివరించండి. ఎలక్ట్రాన్లాంటి సూక్ష్మ కణాలకు దీని ప్రాముఖ్యాన్ని చర్చించండి.
జవాబు:
- కాంతి యొక్క కణ స్వభావం కృష్ణ వస్తువు యొక్క వికిరణాలను మరియు కాంతి విద్యుత్ ఫలితాన్ని విజయవంతంగా వివరించినది.
- కాంతి తరంగ స్వభావం వివర్తనం, వ్యతికరణం వంటి ప్రక్రియలను వివరించినది.
- కావున కాంతికి ద్వంద్వ స్వభావం కలదు అనగా తరంగం వలె (లేదా) కణాల ప్రవాహంగా ఉండును.
- డీబ్రోలీ సిద్ధాంతం ప్రకారం కాంతికి ద్వంద్వ స్వభావం ఉండును అనగా కణ మరియు తరంగ స్వభావం.
డీబ్రోలీ సమీకరణం

- హైసన్బర్గ్ అనిశ్చితత్వ నియమం కూడా ద్వంద్వ స్వభావ ఫలితమే.
అనిశ్చితత్వ నియమం :
“అతివేగంగా ప్రయాణించే ఎలక్ట్రాన్ వంటి సూక్ష్మ పరమాణు కణాల స్థానం, ద్రవ్యవేగం రెండింటినీ ఏక కాలంలో ఖచ్చితంగా నిర్ణయించలేం. స్థాన నిర్ణయంలో అనిశ్చితత్వం (∆x), ద్రవ్యవేగంలో అనిశ్చితత్వం (∆P) అయితే
(∆x) (∆P) ≥ \(\frac{h}{n \pi}\) (n = 1, 2, 3, 4 ………………..)
హైసన్బర్గ్ అనిశ్చితత్వ నియమ ప్రాముఖ్యత:
- ఈ నియమం ప్రకారం, ఎలక్ట్రానుగానీ, ఎలక్ట్రాన్ లాంటి ఇతర కణాలకుగానీ స్థిరమైన కక్ష్య లేదా ప్రక్షేపమార్గం ఉండే అవకాశం లేదు.
- ఈ నియమం సూక్ష్మాతి సూక్ష్మకణాలకు మాత్రమే ప్రాముఖ్యం ఇస్తుంది. స్థూలకణాలకు వర్తించదు.
- మిల్లీగ్రాము గాని అంతకంటే బరువైన వస్తువులకు అనిశ్చితత్వంతో ఫలితం ఏమీ ఉండదు.
![]()
ప్రశ్న 10.
విద్యుదయస్కాంత వికిరణాలలో వేర్వేరు అవధులు ఏమిటి ? విద్యుదయస్కాంత వికిరణాల లక్షణాలు వివరించండి.
జవాబు:
విద్యుదయస్కాంత వికిరణాల అభిలాక్షణిక ధర్మాలు :
1. పదార్థంలో డోలాయమానం చెందే ఆవేశిత కణాలు విద్యుదయస్కాంత వికిరణాలను ఉత్పత్తి చేస్తాయి.
2. ఈ తరంగాల వ్యాపనానికి యానకం అవసరం లేదు. అవి శూన్యంలో కూడా ప్రయాణిస్తాయి.
3. వేగము (c) :
ఒక సెకను కాలంలో ఒక తరంగం ప్రయాణించిన రేఖీయ దూరాన్ని వేగము అంటారు. ప్రయాణాలు : సెం.మీ / సెకను, మీటరు / సెకను
4. తరంగదైర్ఘ్యము (λ) :
తరంగంలో అనుక్రమ (లేదా) వరుసగా ఉన్న రెండు శృంగముల (లేక) ద్రోణుల మధ్య దూరాన్ని తరంగదైర్ఘ్యము అంటారు.
ప్రమాణాలు : Å, మీటరు, సెం.మీ, నానోమీటరు (nm) మరియు పికో మీటరు (pm).
5. పౌనఃపున్యము (v) :
ఒక సెకనులో ఒక నిర్ణీత బిందువును దాటే తరంగాల సంఖ్యను పౌనఃపున్యము అందురు. ప్రమాణాలు: హెర్ట్ సెకను, సైకిల్/సెకను (cps).
6. తరంగ సంఖ్య (v) :
ఒక సెం.మీ. దూరంలో వ్యాపించి ఉన్న తరంగాల సంఖ్యను తరంగసంఖ్య అందురు. (లేక)
తరంగ దైర్ఘ్యానికి వ్యుత్రమ విలువ (\(\frac{1}{\pi}\)) ను తరంగ సంఖ్య అందురు.
ప్రమాణాలు : మీటరు-1, సెం.మీ.-1.
7. క్షేత్రంలో ఒక బిందువు వద్ద విద్యుత్ క్షేత్రబలాన్ని డోలన పరిమితి (లేదా) తీక్షణత (A) అందురు.
ప్రశ్న 11.
పరమాణు ఆర్బిటాల్ను నిర్వచించండి. s, p, d ఆర్బిటాల్ల ఆకారాలను పటాల ద్వారా వివరించండి.
జవాబు:
పరమాణు ఆర్బిటాల్ :
పరమాణువులో కేంద్రకం చుట్టూ ఉండే త్రిజామితీయ ప్రదేశంలో ఒక ఎలక్ట్రాన్ను కనుగొనే సంభావ్యత గరిష్ఠంగా గల ప్రదేశాన్ని పరమాణు ఆర్బిటాల్ అంటారు.
ఆర్బిటాల్ ఆకారం :
ఒక ఎలక్ట్రాన్ను కనుగొనే సంభావ్యత గల ప్రదేశాన్ని గుర్తించడానికి వీలుగా గీచిన త్రిజామితీయ ఉపరితలాన్ని పరమాణు ఆర్బిటాల్ ఆకారం అంటారు.
పరమాణు ఆర్బిటాల్ల ఆకారాలు :
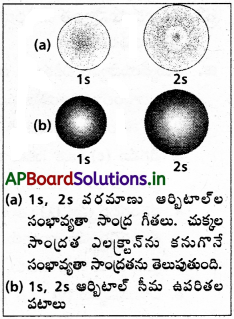
i) s – ఆర్బిటాల్ ఆకారం :
s – ఆర్బిటాల్ గోళాకారంలో ఉంటుంది. వీటికి ఎలక్ట్రాను కనుగొనే సంభావ్యత త్రిజామితీయ ప్రదేశంలో అన్నిదిశలలోను సమానంగా ఉంటుంది.
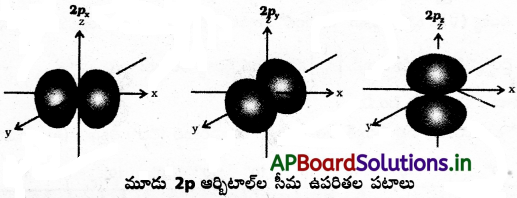
ii) p – ఆర్బిటాల్ ఆకారాలు :
p – ఆర్బిటాల్లో రెండు భాగాలు ఉంటాయి. వాటినే ‘లోబ్’లు అంటారు. కేంద్రకం నుంచి పోయే తలానికి రెండువైపులా ఈ గోళాకార ‘లోబ్ ‘ లు ఉంటాయి. మూడు p- ఆర్బిటాల్ల పరిమాణం, ఆకారం, శక్తి సమానంగా ఉంటుంది. మూడు p- ఆర్బిటాల్లు ఒకదానికొకటి పరస్పరం లంబంగా ఉంటాయి. ప్రతి p – ఆర్బిటాల్ ‘డంబెల్’ ఆకారంలో ఉంటుంది.
iii) d – ఆర్బిటాల్ ఆకారాలు :
ఇవి అయిదు వీటిని dxy, dyz, dzx, dx²-y² మరియు dz² అంటారు. మొదటి నాలుగు డబుల్ డంబెల్ ఆకారాల్లో ఉంటాయి. ప్రతి దానికి నాలుగు లోన్లు ఉంటాయి. dz² ఆర్బిటాల్ ‘Z’ అక్షం చుట్టూ డంబెల్ ఆకారంలో వ్యాప్తి చెంది ఉంటుంది.
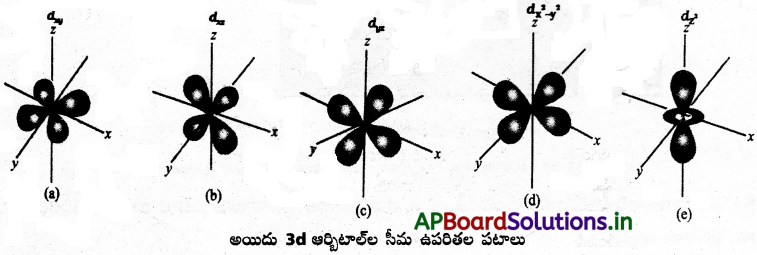
ప్రశ్న 12.
మూడు p – ఆర్బిటాల్ల, అయిదు d ఆర్బిటాల్ల సీమతలాలను రేఖాపటాల ద్వారా వివరించండి.
జవాబు:
‘p’ ఆర్బిటాల్స్ ముద్గరాకృతిలో ఉంటాయి.
i) p – ఆర్బిటాల్ ఆకారాలు :
p – ఆర్బిటాల్లో రెండు భాగాలు ఉంటాయి. వాటినే ‘లోబ్ ‘ లు అంటారు. కేంద్రకం నుంచి పోయే తలానికి రెండువైపులా ఈ గోళాకార ‘లోబ్ ‘లు ఉంటాయి. మూడు p- ఆర్బిటాల్ల పరిమాణం, ఆకారం, శక్తి సమానంగా ఉంటుంది. మూడు p – ఆర్బిటాల్లు ఒకదానికొకటి పరస్పరం లంబంగా ఉంటాయి. ప్రతి p – ఆర్బిటాల్ ‘డంబెల్’ ఆకారంలో ఉంటుంది.
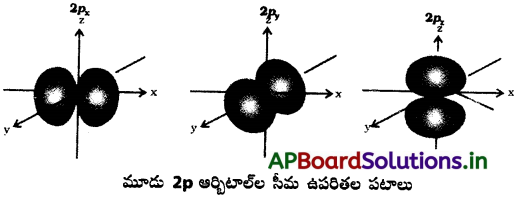
ii) d – ఆర్బిటాల్ ఆకారాలు :
ఇవి అయిదు వీటిని dyz, dzx, dx²-y² మరియు dz² మొదటి నాలుగు డబుల్ డంబెల్ ఆకారాల్లో ఉంటాయి. ప్రతి దానికి నాలుగు లోబ్ లు ఉంటాయి. dz² ఆర్బిటాల్ ‘Z’ అక్షం చుట్టూ డంబెల్ ఆకారంలో వ్యాప్తి చెంది ఉంటుంది.
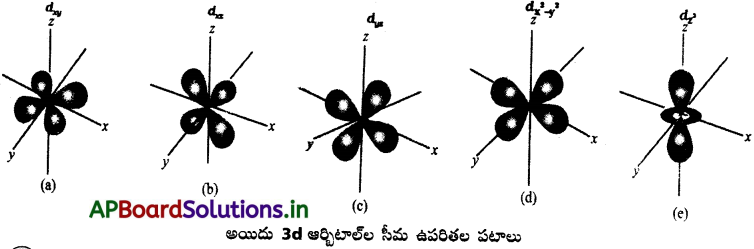
ప్రశ్న 13.
పూర్తిగా నిండిన, సగం నిండిన ఉపకర్పరాల స్థిరత్వానికి కారణాలను విశదీకరించండి.
జవాబు:
Cr మరియు Cu ప్రత్యేకమైన ఎలక్ట్రాన్ విన్యాసాలను కలిగి ఉంటాయి.
Cr – [Ar] 4s¹ 3d5, Cu – [Ar] 4s¹ 3d10
- Cr సగం నిండిన 3d- ఆర్బిటాల్ విన్యాసాన్ని కలిగియుండును.
- Cu పూర్తిగా నిండిన 3d – ఆర్బిటాల్ విన్యాసాన్ని కలిగియుండును.
- మిగతా విన్యాసాల కన్నా సగం నిండిన పూర్తిగా నిండిన ఆర్బిటాళ్లు ఎక్కువ స్థిరత్వాన్ని కలిగియుంటాయి.
సగం లేదా పూర్తిగా నిండిన ఉపకర్పరాల స్థిరత్వానికి కారణాలు
పూర్తిగా నిండిన, సగం నిండిన ఉపకర్పరాలు కింది కారణాల వల్ల స్థిరంగా ఉంటాయి.
1. ఎలక్ట్రాన్ల సౌష్ఠవ పంపిణీ :
సౌష్ఠవం స్థిరత్వానికి దారితీస్తుందని అందరికీ తెలిసిందే. పూర్తిగాగాని, సగం గాని నిండిన ఉపకర్పరాలలో ఎలక్ట్రాన్లు సౌష్ఠవంగా పంపిణీ జరగడం వల్ల అధిక స్థిరత్వం ఉంటుంది. ఒకే ఉపకర్పరంలోని (3d) ఎలక్ట్రాన్లన్నిటికీ ఒకే శక్తి ఉండి ప్రాదేశిక పంపిణీ మాత్రం వేరువేరుగా ఉంటుంది. కాబట్టి, అవి ఒకదానికి మరొకటి కవచంగా ఏర్పడటం సాపేక్షంగా తక్కువ కనుక ఎలక్ట్రాన్లు కేంద్రకంతో అధికంగా ఆకర్షించబడతాయి.
2. మార్చుకొనే శక్తి :
డీజనరేట్ ఆర్బిటాళ్ళలో రెండుగాని అంతకంటే ఎక్కువ సమాంతర స్పిన్లు గల ఎలక్ట్రాన్లు ఉన్నట్లయితే స్థిరత్వ ప్రభావం సంభవిస్తుంది. ఈ ఎలక్ట్రాన్లు ఒకదాని స్థానాన్ని మరొక దానితో మార్చుకొంటాయి. ఈ మార్పు వల్ల ఎలక్ట్రాన్ శక్తి తగ్గుతుంది. దీనినే మార్చుకొనే శక్తి (exchange energy) అంటారు. పూర్తిగా లేదా సగం నిండిన ఉపకర్పరాలలో మార్చుకొనే ఎలక్ట్రాన్ల సంఖ్య గరిష్ఠంగా ఉంటుంది తత్ఫలితంగా మార్చుకొనే శక్తి గరిష్ఠంగా ఉండి అధిక స్థిరత్వం వస్తుంది.
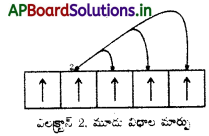
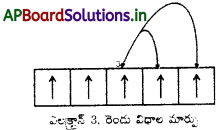
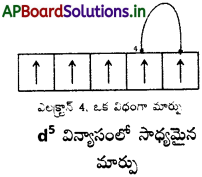
సమాస శక్తిగల ఆర్బిటాల్లోకి సాధ్యమైనంత వరకు ఎలక్ట్రాన్లు సమాంతర స్పిన్తో ప్రవేశించాలనే హుండు నియమం వల్ల మార్చుకొనే శక్తికి ఆధారమనేది గుర్తించాలి. ఇంకొక విధంగా చెప్పాలంటే సగం నిండిన, పూర్తిగా నిండిన ఉపకర్పరాలకు అధిక స్థిరత్వం ఎందుకంటే : (i) సాపేక్షంగా తక్కువ కవచం ఉండటం, (ii) కూలంబిక్ వికర్షణ శక్తి స్వల్పంగా ఉండటం, (iii) మార్చుకొనే శక్తి (echange energy) అధికంగా ఉండటం, పై తరగతులలో మార్చుకొనే శక్తి వివరాలు విపులంగా తెలుసుకొంటారు.
ప్రశ్న 14.
శోషణ, ఉద్గార వర్ణపటాలను వివరించండి. హైడ్రోజన్ పరమాణువులో రేఖా వర్ణపటాల సాధారణ వర్ణనపై చర్చించండి.
జవాబు:
ఉద్గార వర్ణపటము :
ఒక పదార్థాన్ని వేడిచేసినా (లేదా) విద్యుత్ ఉత్సర్గానికి గురిచేసినా దానిలోని పరమాణువులు (లేదా) అణువులు శక్తిని గ్రహిస్తాయి మరియు దానిలోని ఎలక్ట్రాన్లు ఉత్తేజం చెందుతాయి. ఈ ఉత్తేజిత ఎలక్ట్రాన్లు తిరిగి భూస్థితికి వచ్చేటప్పుడు వికిరణాలను ఉద్గారిస్తుంది. ఉద్గారమైన ఈ వికిరణాలను పట్టకం ద్వారా పంపినపుడు ఏర్పడే వర్ణపటాన్ని ఉద్గార వర్ణపటం అంటారు. ఇది రెండు రకములు. అవి ఎ) అవిచ్ఛిన్న వర్ణపటము బి) విచ్ఛిన్న వర్ణపటము. ఉద్గార వర్ణపటంలో నల్లని ప్లేటుపై ప్రకాశవంతమైన గీతలు ఏర్పడతాయి.
శోషణ వర్ణపటము :
శ్వేత కాంతి వంటి వికిరణాన్ని సోడియం జ్వాల ద్వారా పంపి తరువాత బహిర్గతమయ్యే కాంతిని పట్టకం గుండా పంపినట్లయితే రెండు నల్లని రేఖలు ఉన్న అవిచ్ఛిన్న వర్ణపటము ఏర్పడుతుంది. ఇక్కడ సోడియం పసుపు రంగు ప్రాంతంలో రెండు తరంగదైర్ఘ్యాలను తెల్లని కాంతి నుండి శోషించుకుంటుంది. ఈ వర్ణపటాన్ని శోషణ వర్ణపటం అంటారు.
ఈ వర్ణపటంలో ప్రకాశవంతమైన ప్లేటుపై నల్లని గీతలు ఏర్పడతాయి.
- బోర్ తన సిద్ధాంతం ద్వారా హైడ్రోజన్ పరమాణు నిర్మాణం మరియు వర్ణపటంలోని ముఖ్యాంశాలను వివరించాడు.
- బోర్ సిద్ధాంతం పరమాణు నిర్మాణం, వర్ణపటాలలోని చాలా విషయాలు హేతుబద్ధకంగా వివరిస్తుంది.
ముఖ్యాంశాలు :
- హైడ్రోజన్ పరమాణువులోని ఎలక్ట్రాన్ కేంద్రకం నుండి స్థిర వ్యాసార్థాలు గల వృత్తాకార మార్గాలతో నిర్ణీత శక్తులతో తిరుగుతూ ఉండును. ఈ వృత్తాకార మార్గాలను స్థిర స్థితులు (లేక) కక్ష్యలు (లేక) అనుమతించ దగ్గ శక్తిస్థాయిలు అంటారు.
- కక్ష్యలో తిరిగే ఎలక్ట్రాన్ శక్తి స్థిరంగా ఉంటుంది. కాలంతో మారదు.
- ఎలక్ట్రాన్ ఒక కక్ష్య నుండి మరియొక కక్ష్యకు పోయినపుడు శక్తి మార్పు వస్తుంది.
a) ఎలక్ట్రాన్ కింది స్థిర స్థితి నుండి పై స్థిర స్థితికి పోయినపుడు శక్తిని శోషించుకొనును.
b) ఎలక్ట్రాన్ పై స్థిర స్థితి నుండి క్రింది స్థిర స్థితికి పోయినపుడు శక్తిని ఉద్గారించుకొనును.
ఆ రెండు స్థిర స్థితులు శక్తి భేదం ∆E = E2 – E1 = hυ
పౌనఃపున్యం υ = \(\frac{E_2E_1}{h}\)
E1 మరియు E2 లు కింది మరియు పై స్థితుల శక్తులు
→ ఎలక్ట్రాన్ యొక్క కోణీయ ద్రవ్యవేగం mvr = \(\frac{nh}{2 \pi}\)
ఎలక్ట్రాన్ కోణీయ ద్రవ్యవేగం \(\frac{h}{2 \pi}\) విలువకు పూర్ణాంక గుణిజంగా ఉండే కక్ష్యలలో మాత్రమే తిరుగుతుంది.
బోర్ సిద్ధాంతం ద్వారా హైడ్రోజన్ వర్ణపట రేఖల వివరణ :
- హైడ్రోజన్ పరమాణువునందు వర్ణపట రేఖలు బోర్ సిద్ధాంతం ద్వారా వివరించబడ్డాయి.
- బోర్ సిద్ధాంతం ప్రకారం రెండు స్థిర స్థాయిల మధ్య ఎలక్ట్రాన్ పరివర్తనం జరిగినపుడు

- శోషణ వర్ణపటం nf > ni (శక్తి శోషించబడును (+Ve))
- ఉద్గార వర్ణపటం ni > nf (శక్తి ఉద్గారించబడును (- Ve))
- శోషణలో గాని, ఉద్గారంలో గాని ప్రతి రేఖ కూడా హైడ్రోజన్ పరమాణువులో ఒక ప్రత్యేకమైన పరివర్తన ద్వారానే వస్తుంది.
- హైడ్రోజన్ పరమాణువులు ఎక్కువ సంఖ్యలో ఉన్నట్లయితే ఎక్కువ సంఖ్యలో వర్ణపట రేఖలు ఏర్పడతాయి.
సాధించిన సమస్యలు (Solved Problems)
ప్రశ్న 1.
35Br30 లోని ప్రోటాన్లు, న్యూట్రాన్ల సంఖ్యను లెక్కించండి.
సాధన:
35Br30 లోZ = 35, A = 80 ఇది తటస్థ పరమాణువు.
ప్రోటాన్ ల సంఖ్య = ఎలక్ట్రాన్ల సంఖ్య Z = 35
న్యూట్రాన్ల సంఖ్య = 80 – 35 = 45
![]()
ప్రశ్న 2.
ఒక కణంలో ఎలక్ట్రాన్లు, ప్రోటాన్లు, సాధన. సమీకరణం V = న్యూట్రాన్ల సంఖ్య 18, 16, 16 వరసగా కలవు. ఆ కణానికి సరైన గుర్తును ఇవ్వండి.
సాధన:
పరమాణు సంఖ్య, ప్రోటాన్ల సంఖ్యకు సమానం = 16.
మూలకం గంధకం (S) పరమాణు ద్రవ్యరాశి సంఖ్య = ప్రోటాన్ల సంఖ్య + న్యూట్రాన్లసంఖ్య
= 16 + 16 = 32
ప్రోటాన్ల సంఖ్య ఎలక్ట్రాన్ల సంఖ్యకు సమానం కాదు కనుక ఆ కణం తటస్థమైంది కాదు. అది ఆనయాన్ (రుణావేశం కలది) దానిమీద ఆవేశం ఎలక్ట్రాన్లు ఎన్ని ఎక్కువ ఉన్నవో అంత, ఎక్కువ ఉన్న ఎలక్ట్రాన్లు = 18 -16 = గుర్తు 3216S2-.
గమనిక :
సంకేతంAZX వాడేముందు ఆ కణం తటస్థమైందా, కాటయానా, ఆనయానా తెలుసుకోవాలి. తటస్థ పరమాణువు అయితే
ప్రోటాన్ల సంఖ్య = ఎలక్ట్రాన్ల సంఖ్య = పరమాణు సంఖ్య.
ఆ కణం ఒకవేళ అయాన్ అయితే ఎలక్ట్రాన్ల సంఖ్య కంటే ప్రోటాన్ల సంఖ్య ఎక్కువ అయితే కాటయాన్, ధన అయాన్ లేదా తక్కువ అయితే ఆనయాన్, రుణ అయాన్ ఆ కణం తటస్థమైంది అయినా లేదా. అయాన్ అయినా న్యూట్రాన్ల సంఖ్య ఎప్పుడూ (A – Z) కు సమానమవుతుంది.
ప్రశ్న 3.
ఆకాశవాణి ఢిల్లీ, వివిధభారతి స్టేషన్ నుంచి 1,368 kHz (కిలో హెర్ట్స్) పౌనఃపున్యంపై ప్రసారాలు చేస్తుంది. ప్రసారిణి ఉద్గారించే విద్యుదయస్కాంత వికిరణాల తరంగ దైర్ఘ్యం గణించండి. ఇది విద్యుదయస్కాంత వర్ణపటంలో ఏ ప్రాంతానికి చెందుతుంది ?
సాధన:
తరంగదైర్ఘ్యం, λ, C/υ కి సమానం, నిర్వాతంలో విద్యు దయస్కాంత వికిరణాల వేగం, వాటి పౌనఃపుణ్యం. ఈ విలువలను ప్రతిక్షేపించగా, λ, C/υ.
ప్రశ్న 4.
దృగ్గోచర వర్ణపటం ఊదా (violet) (400 nm) నుంచి ఎరుపు (red) (750 nm) వరకు ఉంటుంది. ఈ తరంగదైర్ఘ్యాలను పౌనఃపున్యాల (Hz) లో తెలపండి. (1nm = 10-9 m).
సాధన:
సమీకరణం V = \(\frac{1}{\lambda}\) ఉపయోగించి ఊదా (violet) కాంతి పౌనఃపున్యం
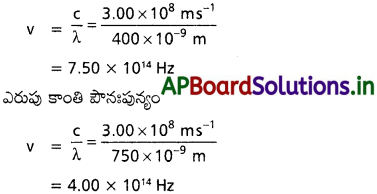
దృగ్గోచర వర్ణపటం 4.0 × 1014 Hz నుండి
7.5 × 1014 Hz పౌనఃపున్యం ప్రమాణాలలో ఉంటుంది.
ప్రశ్న 5.
5000 Å తరంగదైర్ఘ్యం గల పసుపు (yellow) వికిరణాల (a) తరంగ సంఖ్యను (b) పౌనః పున్యాన్ని గణించండి.
సాధన:
(a) తరంగసంఖ్య (\(\overline{\mathrm{υ}}\)) గణించడం
λ = 5800 Å = 5800 × 10-8 cm
= 5800 × 10-10 m

ప్రశ్న 6.
5 × 1014 Hz పౌనఃపున్యం గల ఒక మోల్ ఫోటాన్ల శక్తిని గణించండి.
సాధన:
ఒక ఫోటాన్ శక్తి E = hv
= 6.626 × 10-34 J S
V= 5 × 1014 s-1
E = (6.626 × 10-34Js) × (5 × 1014 s-1)
= 3.313 × 10-19 )
ఒక మోల్ ఫోటాన్ శక్తి
= (3.313 × 10-19 J) × (6.022 × 1023 mol-1)
= 199.51 kJ mol-1.
ప్రశ్న 7.
ఒక 100 వాట్ల బల్బు 400 nm ల ఏకవర్ణ కాంతిని ఉద్గారం చేస్తుంది. ఒక సెకనుకు ఆ బల్బు ఎన్ని ఫోటాన్ లను ఉద్గారం చేస్తుందో లెక్కించండి.
సాధన:
బల్బు సామర్థ్యం = 100 watt
= 100 J s-1
ఒక ఫోటాన్ శక్తి E = hv hc/λ

ప్రశ్న 8.
300 nm తరంగదైర్ఘ్యం గల విద్యుదయస్కాంత వికిరణాలు సోడియం లోహం మీద పడినప్పుడు 1.68 × 105 J mol-1 గతిజశక్తిగల ఎలక్ట్రాన్లు ఉద్గార మయ్యాయి. సోడియం పరమాణువు నుంచి ఎలక్ట్రాను తొలగించడానికి కావలసిన కనిష్ఠ శక్తి ఎంత? ఫోటో ఎలక్ట్రాన్ ఉద్గారం కావడానికి గరిష్ఠ తరంగదైర్ఘ్యం ఎంత?
సాధన:
300 nm ఫోటాన్ శక్తి
hv = hc/λ
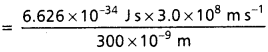
= 6.626 × 10-19 J
ఒక మోల్ ఫోటాన్ల శక్తి
= 6.626 × 10-19 J × 6.022 × 1023 mol-1
= 3.99 × 105 J mol-1
సోడియం నుంచి ఒక మోల్ ఎలక్ట్రాన్లను తీయడానికి కావలసిన కనిష్ఠ శక్తి
= (3.99 – 1.68) 105 J mol-1
= 2.31 × 105 J mol-1
ఒక ఎలక్ట్రాను తీయటానికి కావలసిన కనిష్ఠ శక్తి

= 518 nm ఇది ఆకుపచ్చరంగు కాంతి.
![]()
ప్రశ్న 9.
లోహం ఆరంభ పౌనఃపున్యం (vo) 7.0 × 1014 s-1. v = 1.0 × 1015 s-1 పౌనఃపున్యం గల వికిరణాలు లోహంపై తగిలినప్పుడు బయటకు వెలువడే ఎలక్ట్రాన్ల గతిజశక్తి గణించండి.
సాధన:
ఐన్స్టీన్ సమీకరణం ప్రకారం
గతిజశక్తి = ½ me v² = h(v – vo)
= (6.626 × 10-34 Js) (1.0 × 1015 s-1 – 7.0 × 1014 s-1)
= (6.626 × 10-34 J s) (3.0 × 1014 s-1)
= 1.988 × 10-19 J
ప్రశ్న 10.
హైడ్రోజన్ పరమాణువులో n = 5 స్థాయి నుంచి n = 2 స్థాయికి ఎలక్ట్రాన్ పరివర్తనం చెంది నప్పుడు ఉద్గారమయ్యే ఫోటాన్ పౌనఃపున్యం, తరంగదైర్ఘ్యం ఎంత ?
సాధన:
n1 = 5, nf = 2 కి పరివర్తనం చెందినప్పుడు వర్ణపటం రేఖ దృగ్గోచర ప్రాంతంలో ఉండే బామర్ శ్రేణికి చెందుతుంది.

ఫోటాన్ పౌనఃపున్యం (శక్తి పరిమాణాన్ని మాత్రమే తీసుకొని)

ప్రశ్న 11.
He+ మొదటి కక్ష్య శక్తిని గణించండి. ఆ కక్ష్య వ్యాసార్థం ఎంత?
సాధన:

ప్రశ్న 12.
10 m s-1 వేగంతో చలించే 0.1 kg బంతి తరంగ దైర్ఘ్యం ఎంత?
సాధన:

ప్రశ్న 13.
ఎలక్ట్రాన్ ద్రవ్యరాశి 9.1 × 10-31 kg. దాని గతిజశక్తి 3.0 × 10-25J, దాని తరంగదైర్ఘ్యాన్ని లెక్కించండి.
సాధన:
గతిజశక్తి K.E. = ½ mv²

ప్రశ్న 14.
3.6 Å తరంగదైర్ఘ్యం గల ఫోటాన్ ద్రవ్యరాశిని గణించండి.
సాధన:
λ = 3.6 Å = 3.6 × 10-10 m
ఫోటాన్ వేగం = కాంతి వేగం
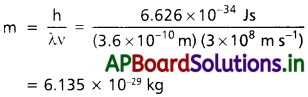
ప్రశ్న 15.
సరియైన ఫోటాన్లను ఉపయోగించి మైక్రోస్కోప్ ద్వారా పరమాణువులో ఉన్న ఎలక్ట్రాన్ ను 0.1 Å దూరంలోపల చూడగలిగారు. దాని వేగం కొలతలో ఉన్న అనిశ్చితత్వం ఎంత?
సాధన:

ప్రశ్న 16.
గల్ఫ్ బంతి ద్రవ్యరాశి 40g దాని వేగం 45 m/s. దాని వేగాన్ని 2% లోపల కొలవగలిగినట్లయితే దాని స్థానంలో అనిశ్చితత్వం ఎంత?
సాధన:
వేగంతో అనిశ్చితత్వం 2% అంటే
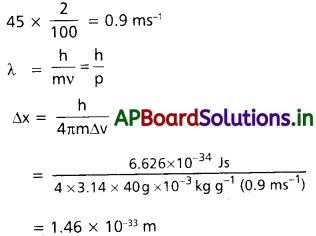
ఈ విలువ పరమాణు కేంద్రకం వ్యాసం కంటే ~ 1018 రెట్లు చిన్నది. ఇంతకుముందు చెప్పినట్లు పెద్ద కణాలకు నిశ్చితత్వ నియమం కచ్చితమైన కొలతలకు అర్థవంతమైన అవధులు పెట్టలేదు.
![]()
ప్రశ్న 17.
ప్రధాన క్వాంటమ్ సంఖ్య n = 3 తో ఉన్న మొత్తం ఆర్బిటాల్ల సంఖ్య ఎంత?
సాధన:
n = 3 కు సాధ్యమైన 7 విలువలు 0, 1, 2. ఆ విధంగా ఒక 3s ఆర్బిటల్ (n = 3, l = 0, ml = 0);
మూడు 3p ఆర్బిటాల్ (n = 3, l = 1, ml = -1, 0, +1); అయిదు 3d ఆర్బిటాల్లు (n = 3 l = 2, ml = -2, -1, 0, +1, +2).
∴ మొత్తం ఆర్బిటాల్ ల సంఖ్య = 1 + 3 + 5 = 9
ఇదే విలువను వేరే విధంగా పొందవచ్చు ;
ఆర్బిటాల్ సంఖ్య = n² = 3² = 9.
ప్రశ్న 18.
s, p, d, f సంకేతాలను ఉపయోగించి కింది క్వాంటమ్ సంఖ్యలతో ఆర్బిటాల్లను వర్ణించండి.
(a) n = 2, l = 1
(b) n = 4, 1 = 0
(c) n = 5, 1 = 3
(d) n = 3, 1 = 2
సాధన: