Andhra Pradesh BIEAP AP Inter 2nd Year Chemistry Study Material 4th Lesson ఉపరితల రసాయనశాస్త్రం Textbook Questions and Answers.
AP Inter 2nd Year Chemistry Study Material 4th Lesson ఉపరితల రసాయనశాస్త్రం
అతిస్వల్ప సమాధాన ప్రశ్నలు
ప్రశ్న 1.
అంతర్ఆలం అంటే ఏమిటి? ఒక ఉదాహరణ తెలపండి.
జవాబు:
అంతర్అలం :
సాధారణంగా కొన్ని అణువుల మందాన్ని అంతర్అలం అంటారు. ఆయతమప్రావస్థలను ఒక అడ్డుగీత (-) లేదా ఒక నిలువు గీత (i) ద్వారా వేరు పరుస్తు అంతర్ తలాన్ని వ్యక్తం చేస్తారు.
ఉదా : ఘనపదార్థం, వాయు పదార్థాల మధ్య అంతర్ తలాన్ని ఘనస్థితి – వాయువు (లేదా) ఘన స్థితి / వాయువు అని వ్యక్తం చేస్తారు.
ప్రశ్న 2.
అధిశోషణం అంటే ఏమిటి? ఒక ఉదాహరణ ఇవ్వండి.
జవాబు:
అధిశోషణం :
“ఒక పదార్థం వేరొక ద్రవం లేదా ఘన పదార్థం ఉపరితలంపై గాఢత చెందడాన్ని ‘అధిశోషణం’ అంటారు. ఇది ఒక ఉపరితల దృగ్విషయము.
ఉదా : i) CO2, SO2, Cl2 లాంటి వాయువులను ఉత్తేజిత బొగ్గు అధిశోషించుకుంటుంది.
ii) Pt లేక Ni లోహం, హైడ్రోజన్ వాయువుతో సంపర్కంలో ఉంటే ఆ వాయువును అధిశోషించుకుంటుంది.
ప్రశ్న 3.
అభిశోషణం అంటే ఏమిటి? ఒక ఉదాహరణ ఇవ్వండి.
జవాబు:
అభిశోషణం :
“ఏదైనా ఒక పదార్థపు అణువులు, ఇతర పదార్థపు ఉపరితలంపై మరియు అంతర్భాగంలో కూడా ఏకరీతిగా వ్యాప్తి చెందడాన్ని ‘అభిశోషణం’ అంటారు.
ఇది ఒక ఆయతన దృగ్విషయం.
ఉదా : i) నీటిలో ముంచిన ‘స్పాంజ్’ నీటిని అభిశోషించుకుంటుంది.
ii) రంగు సిరాలో ఉంచిన సుద్దముక్క సిరాను అభిశోషించుకుంటుంది.
ప్రశ్న 4.
అధిశోషణం, అభిశోషణం వీటిని భేదపరచండి. ప్రతిదానికి ఒక ఉదాహరణ ఇవ్వండి.
జవాబు:
| అధిశోషణం | అభిశోషణం |
| “ఒక పదార్థం వేరొక ద్రవం లేదా ఘన పదార్థం ఉపరితలంపై గాఢత చెందడాన్ని ‘అధిశోషణం’ అంటారు. ఇది ఒక ఉపరితల దృగ్విషయము. | “ఏదైనా ఒక పదార్థపు అణువులు, ఇతర పదార్థపు ఉపరితలంపై మరియు అంతర్భాగంలో కూడా ఏకరీతిగా వ్యాప్తి చెందడాన్ని ‘అభిశోషణం’ అంటారు. ఇది ఒక ఆయతన దృగ్విషయం. |
| ఉదా : i) CO2, SO2, Cl2 లాంటి వాయువులను ఉత్తేజిత బొగ్గు అధిశోషించుకుంటుంది. ii) Pt లేక Ni లోహం, హైడ్రోజన్ వాయువుతో సంపర్కంలో ఉంటే ఆ వాయువును ధిశోషించుకుంటుంది. | ఉదా : i) నీటిలో ముంచిన ‘స్పాంజ్’ నీటిని అభిశోషించుకుంటుంది. ii) రంగు సిరాలో ఉంచిన సుద్దముక్క సిరాను అభిశోషించుకుంటుంది. |
ప్రశ్న 5.
సిలికాజెల్ సమక్షంలో తేమతో కూడిన గాలి, తడి లేకుండా మారుతుంది. దీనికి కారణం ఏమిటి?
జవాబు:
సిలికాజెల్ సమక్షంలో తేమతో కూడిన గాలి, తడి లేకుండా మారుతుంది. దీనికి కారణం నీటి అణువులు జెల్ యొక్క ఉపరితలంపై అధిశోషణం చెందుతాయి.
ప్రశ్న 6.
మిథిలీన్ బ్లూ ద్రావణానికి జాంతవ బొగ్గును కలిపి గిలకరించి ద్రావణాన్ని వడపోస్తే ఏర్పడిన గాలితం రంగును కోల్పోతుంది. కారణం తెలపండి.
జవాబు:
మిథిలీన్ బ్లూ ద్రావణానికి జాంతవ బొగ్గును కలిపి గిలకరించి ద్రావణాన్ని వడపోస్తే ఏర్పడిన కాగితం రంగును కోల్పోతుంది.
కారణం :
జాంతవ బొగ్గుపై మిథిలీన్ బ్లూ అణువులు (అద్దకం) ద్రావణంనుండి అధిశోషణం చెందుతాయి.
![]()
ప్రశ్న 7.
నీటి ఆవిరి గల పాత్రలో రెండు భాగాలలో కొద్ది పరిమాణంలో సిలికాజెల్, అనార్ద్ర కాల్షియమ్ క్లోరైడ్ను వేరుగా ఉంచాం. ఏ ఘటన లేదా దృగ్విషయం జరుగుతుంది?
జవాబు:
నీటి ఆవిరిగల పాత్రలో రెండు భాగాలలో కొద్ది పరిమాణంలో సిలికాజెల్, అనార్ద్ర CaCl2 ను వేరుగా వుంచినపుడు నీటి అణువులు అనార్ద్ర CaCl2 తో అభిశోషణం చెందుతాయి మరియు జెల్పై అధిశోషణం జరుపుతాయి.
ప్రశ్న 8.
డీసార్హాన్ అంటే ఏమిటి?
జవాబు:
ఒక ఉపరితలం నుండి దానిపై అధిశోషణం చెందిన పదార్థాన్ని తొలగించు ప్రక్రియను విశోషణం (డిసార్షన్) అంటారు.
ప్రశ్న 9.
సాల్షన్ అంటే ఏమిటి?
జవాబు:
కొన్ని సందర్భాలలో అధిశోషణం, అభిశోషణం రెండు ఒకేసారి జరుగుతాయి. ఈ ప్రక్రియను శోషణం (సార్షన్) అంటారు.
ప్రశ్న 10.
అధిశోషణం, అభిశోషణం వీటిలో ఉపరితల ఘటన ఏది? ఎందువల్ల?.
జవాబు:
అధిశోషణం అనునది ఉపరితల ఘటన
అధిశోషణం :
“ఒక పదార్థం వేరొక ద్రవం లేదా ఘన పదార్థం ఉపరితలంపై గాఢత చెందడాన్ని ‘అధిశోషణం’ అంటారు. ఇది ఒక ఉపరితల దృగ్విషయము.
అభిశోషణం :
“ఏదైనా ఒక పదార్థపు అణువులు, ఇతర పదార్థపు ఉపరితలంపై మరియు అంతర్భాగంలో కూడా ఏకరీతిగా వ్యాప్తి చెందడాన్ని ‘అభిశోషణం’ అంటారు. ఇది ఒక ఆయతన దృగ్విషయం.
ప్రశ్న 11.
అధిశోషణం, అభిశోషణం రెండూ ఏకకాలంలో జరిగితే ఆ ఘటనను ఏమంటారు?
జవాబు:
కొన్ని సందర్భాలలో అధిశోషణం, అభిశోషణం రెండు ఒకేసారి జరుగుతాయి. ఈ ప్రక్రియను శోషణం (సార్షన్) అంటారు.
ప్రశ్న 12.
సిరాలో ముంచి ఉంచిన సుద్దముక్క కింది వాటిని ప్రదర్శిస్తుంది.
ఎ) ముక్క ఉపరితలంపై సిరా రంగు నిలిచి ఉంటుంది.
బి) సుద్దముక్కను ముక్కలు చేస్తే లోపలి భాగం తెలుపుగానే ఉంటుంది. పై పరిశీలనలను వివరించండి.
జవాబు:
ఎ) సిరాలో ముంచి ఉంచిన సుద్దముక్క ఉపరితలంపై సిరారంగు నిలిచి ఉంటుంది. దీనికి కారణం సిరారంగు అణువుల యొక్క అధిశోషణం.
బి) సిరాలో ముంచి ఉంచిన సుద్దముక్కను ముక్కలు చేస్తే లోపలి భాగం తెలుపుగానే ఉంటుంది. దీనికి కారణం సిరారంగు అణువులు అధిశోషణం చెంది సిరాలోని ద్రావణి అభిశోషణం జరుపుతుంది.
![]()
ప్రశ్న 13.
ఘనపదార్థంపై వాయువు అధిశోషణాన్ని ప్రభావితం చేసే అంశాలను తెలపండి.
జవాబు:
ఘనపదార్థంపై వాయువు అధిశోషకాన్ని ప్రభావితం చేసే అంశాలు
ఎ) అధిశోషకం ఉపరితల వైశాల్యం
బి) వాయు స్వభావం
సి) అధిశోషిత పీడనం
డి) ఉష్ణోగ్రత
ప్రశ్న 14.
అధిశోషణం ఎప్పుడూ ఉష్ణమోచకంగానే ఉంటుంది. కారణం ఏమిటి?
జవాబు:
అధిశోషణం ప్రక్రియలో అధిశోషకం ఉపరితలంపై ఉండే అవశేషబలాల సంఖ్య తగ్గుతుంది. దీనివలన ఉపరితల శక్తి తగ్గి, ఆ తగ్గినశక్తి, ఉష్ణం రూపంలో వెలువడుతుంది. కావున అధిశోషణ ప్రక్రియ ప్రధానంగా ఉష్ణమోచక చర్యగానే ఉంటుంది.
ప్రశ్న 15.
బొగ్గుపై అమోనియా వాయువు అధిశోషణం చెందినప్పుడు ∆H, ∆S విలువల సంజ్ఞలు ఎలా ఉంటాయి.
జవాబు:
బొగ్గుపై అమ్మోనియా వాయువు అధిశోషణం చెందినపుడు ∆H విలువ రుణాత్మకంగాను ∆S విలువ ధనాత్మంగాను ఉండును.
ప్రశ్న 16.
అధిశోషణం ఎన్ని రకాలు? అవి ఏవి?
జవాబు:
అధిశోషణం రెండు రకాలు.
- భౌతిక అధిశోషణం (ఫిజిసార్షన్)
- రసాయన అధిశోషణం (కెమిసాన్)
ప్రశ్న 17.
ఘనపదార్థంపై వాయువు జరిపే ఫిజిసార్డన్లో ఏ రకం బలాలు ఇమిడి ఉన్నాయి?
జవాబు:
ఘనపదార్థంపై వాయువు జరిపే ఫిజిసార్లోన్లో వాండర్ వాల్ బలాలు ఇమిడి ఉన్నాయి.
![]()
ప్రశ్న 18.
ఘనపదార్థంపై వాయువు జరిపే కెమిసారన్కు వాయు అణువులకు ఘనపదార్థం ఉపరితలానికి మధ్య జరిగే ఏ రకం అన్యోన్య చర్య కారణం?
జవాబు:
ఘనపదార్థంపై వాయువు జరిపే కెమిసారన్కు వాయు అణువులకు ఘనపదార్థం ఉపరితలానికి మధ్య రసాయన బంధాలు (లేదా) వేలన్సీ బలాలు కారణం.
ప్రశ్న 19.
కెమిసాల్షన్ను ఎందుకు ఉత్తేజిత అధిశోషణం అంటారు?
జవాబు:
కెమిసార్షన్లో ఉత్తేజితశక్తి అధికం అందువలన దీనిని ఉత్తేజిత అధిశోషణం అంటారు.
ప్రశ్న 20.
ఫిజిసార్షన్కు కెమిసారన్కు మధ్యగల భేదం ఏమిటి?
జవాబు:
- ఫిజిసార్లోన్లో అధిశోషితం, అధిశోషకం మధ్య ఉండు బలాలు వాండర్ వాల్ బలాలు
- కెమిసార్లోన్లో అధిశోషితం, అధిశోషకం మధ్య ఉండు బలాలు రసాయన బంధాలు (లేదా) వేలన్సీ బలాలు.
ప్రశ్న 21.
ఫిజిసార్షన్, కెమిసార్షన్ల మధ్య ఏది ఉత్రమణీయంగా ఉంటుంది?
జవాబు:
ఫిజిస్టార్షన్, కెమిస్టార్షన్లలో ఫిజిస్సార్షన్ ఉత్రణీయమైనది.
ప్రశ్న 22.
వాయువు సందిగ్ధ ఉష్ణోగ్రతతో వాయు అధిశోషణానికి ఎలా సంబంధం ఉంది?
జవాబు:
వాయువు సందిగ్ధ ఉష్ణోగ్రత పెరిగే కొలది వాయువు త్వరగా ద్రవీకరింపబడుతుంది. కావున సందిగ్ధ ఉష్ణోగ్రత పెరిగే కొలది వాయు అధిశోషణ ప్రక్రియ కూడా పెరుగును.
ప్రశ్న 23.
SO2 సందిగ్ధ ఉష్ణోగ్రత 630 K CH4 సందిగ్ధ ఉష్ణోగ్రత 190 K. వీటిలో ఏది బొగ్గుపై సులభంగా అధిశోషణం చెందుతుంది? ఎందుకు?
జవాబు:
SO2 యొక్క సందిగ్ధ ఉష్ణోగ్రత (630 K) CH4 యొక్క సందిగ్ధ ఉష్ణోగ్రత కంటే ఎక్కువగా ఉన్నది. కావున SO2 వాయువు బొగ్గుపై సులభంగా అధిశోషణం చెందును. అధిక సందిగ్ధ ఉష్ణోగ్రత ఉన్న వాయువులు ఎక్కువ అధిశోషణంను కలిగి ఉంటాయి.
ప్రశ్న 24.
సులభంగా ద్రవీకరణం చెందే వాయువులు ఘనపదార్థాలపై సులభంగా అధిశోషించబడతాయి. ఎందుకు?
జవాబు:
సులభంగా ద్రవీకరణం చెందే వాయువులు ఘనపదార్థాలపై సులభంగా అధిశోషించబడతాయి. దీనికి కారణం సందిగ్ధ ఉష్ణోగ్రతకం దగ్గరగా వాండర్ వాల్ బాలాలు బలంగా ఉంటాయి.
![]()
ప్రశ్న 25.
SO2 H2 లలో ఏది బొగ్గుపై సులభంగా అధిశోషణం చెందుతుంది? కారణం ఏమిటి?
జవాబు:
SO2 H2లలో SO2 బొగ్గుపై సులభంగా అధిశోషణం చెందును. దీనికి కారణం SO2 యొక్క సందిగ్ధ ఉష్ణోగ్రత (630 K) H2 యొక్క సంధిగ్ధ ఉష్ణోగ్రత (33K) కంటే ఎక్కువ.
ప్రశ్న 26.
ఫిజిసాల్షన్, కెమిసార్షన్ల ఎంథాల్పీ విలువలను తులనం చేయండి.
జవాబు:
- ఫిజిసార్షన్ యొక్క ఎంథాల్పీ విలువలు తక్కువగా ఉంటాయి (20 – 40 KJ/mole)
- కెమిసార్షన్ యొక్క ఎంథాల్పీ విలువలు ఎక్కువగా ఉంటాయి (80 – 240 KJ/mole)
ప్రశ్న 27.
భౌతిక అధిశోషణం ఎంథాల్పీ విలువ పరిమాణం ఎలా ఉంది? దీనికి కారణం తెలపండి.
జవాబు:
భౌతిక అధిశోషణం ఎంథాల్పీ విలువ పరిమాణం తక్కువ 20 – 40 KJ/mole దానికి కారణం వాండర్ వాల్ బలాలు వాయువుకు ఘనపదార్థంకు మధ్య ఉంటాయి.
ప్రశ్న 28.
కెమిసాన్ ఎంథాల్పీ విలువ పరిమాణం ఏమిటి? ఈ పరిమాణానికి కారణం ఏమిటి?
జవాబు:
రసాయన అధిశోషణం ఎంథాల్పీ విలువ పరిమాణం ఎక్కువ. 80 – 240 KJ/mole దీనికి కారణం రసాయన బలాలు (లేదా) వేలన్సీ బలాలు వాయువుకు ఘనపదార్థానికి మధ్య ఉంటాయి.
ప్రశ్న 29.
అధిశోషణం అనువర్తనాలు రెండింటిని తెలపండి.
జవాబు:
1) అధిక శూన్య స్థితిని ఏర్పరచడం :
ఒక పాత్రలో అధిక శూన్య స్థితిని పొందడానికి ఆ పాత్రలోని గాలిని నిర్వాత పంపుద్వారా తొలగిస్తారు. ఈ ప్రక్రియలో పాత్రలో ఇంకా మిగిలి ఉన్న కొద్దిపాటి గాలిని, బొగ్గును ఉపయోగించి అధిశోషణ ప్రక్రియ ద్వారా తొలగిస్తారు.
2) వాయు ముసుగు (gas mask) :
బొగ్గుగనులలో పనిచేసే కార్మికులు గాలిని పీల్చుకొనేటప్పుడు గాలిలోని విషవాయువులను అధిశోషించుకోవడానికి వాడే సాధనాన్ని వాయు ముసుగు అంటారు. ఇది ఉత్తేజపరిచిన బొగ్గు లేదా ఇతర అధిశోషకాల మిశ్రమంతో నిండి ఉంటుంది.
ప్రశ్న 30.
ఫిజిసారన్కు ఎందుకు విశిష్టత లేదా వరణాత్మకత లేదు?
జవాబు:
వాండర్వాల్ బలాలు సార్వత్రికం కాబట్టి అధిశోషకం ఉపరితలం ఏ వాయువు పైనా ప్రత్యేకంగా ఇష్టతను ప్రదర్శించదు. కావున ఫిజిసారన్కు విశిష్టతలేదు.
![]()
ప్రశ్న 31.
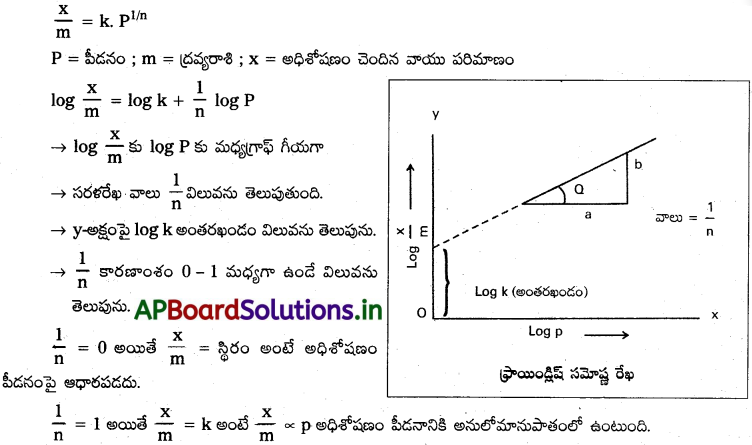
అధిశోషణ సమోష్ణరేఖ అంటే ఏమిటి? ఫ్రాయిండ్లిష్ సమోష్ణరేఖ సమీకరణం వ్రాయండి.
జవాబు:
స్థిర ఉష్ణోగ్రత వద్ద ఏకాంక ద్రవ్యరాశిగల ఘనస్థితిలోని అధిశోషకంపై అధిశోషణం చెందే వాయువు పరిమాణానికి, వాయువు పీడనానికి మధ్యగల అనుభావిక సంబంధాన్ని తెలిపే రేఖలను అధిశోషణ సమోష్ణరేఖలు అంటారు.
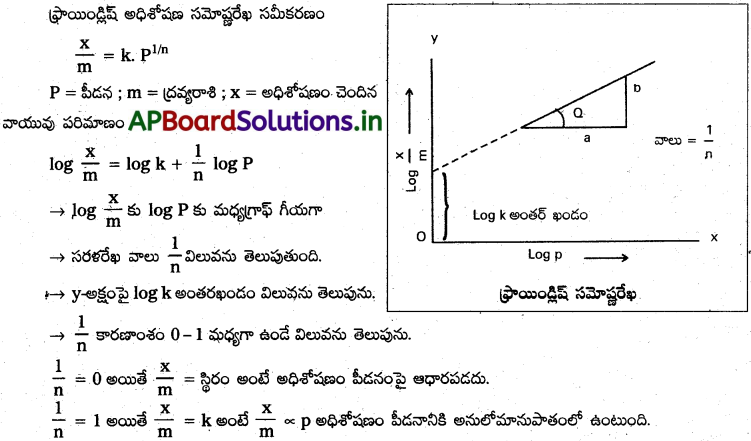
ఫ్రాయిండ్లిష్ సమోష్టరేఖ సమీకరణం \(\frac{x}{m}\) = k × pl/n
x = అధిశోషణం చెందిన వాయు పరిమాణం
P = పీడనం
m = ద్రవ్యరాశి
ప్రశ్న 32.
ఏ పరిస్థితులలో ఫ్రాయిండ్లిష్ సమోష్ణరేఖ సమీకరణం క్రింది రేఖాపటాన్ని ప్రదర్శిస్తుంది?
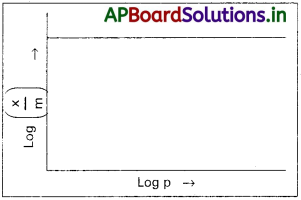
జవాబు:
పై గ్రాఫ్ నుండి అధిశోషణం ప్రక్రియ పీడనంపై ఆధారపడదు. అని తెలుస్తుంది.
ఇచ్చట \(\frac{1}{n}\) = 0, \(\frac{x}{m}\) = స్థిరాంకం
ప్రశ్న 33.
విజాతి ఉత్ప్రేరణంలో అధిశోషణం పాత్ర ఏమిటి?
జవాబు:
విజాతి ఉత్ప్రేరణంలో క్రియాజనక అణువులు ఘన పదార్థ ఉపరితలంపై అధిశోషణం జరుపుట ద్వారా ఉత్ప్రేరణ చర్య వలన చర్యరేటు పెరుగును.
ప్రశ్న 34.
KClO3 నుంచి O2 తయారీలో MnO2 పాత్ర ఏమిటి?
జవాబు:
![]()
పై చర్యలో MnO2, చర్యరేటును పెంచును. ఇది ఉత్ప్రేరకంగా పనిచేయును.
ప్రశ్న 35.
ఉత్ప్రేరణం ఘటనలో ‘ప్రమోటర్లు’ (ప్రవర్ధకాలు), ‘విష పదార్థాలు’ వీటిని నిర్వచించండి.
జవాబు:
ప్రమోటర్లు (ప్రవర్థకాలు) :
ఉత్ప్రేరకం యొక్క ఉత్తేజితత్వాన్ని పెంచే పదార్థాలను ప్రవర్థకాలు అంటారు.
విష పదార్థాలు :
ఉత్ప్రేరకం ఉత్తేజితత్వాన్ని తగ్గించే పదార్థాలను విషపదార్థాలు అంటారు.
![]()
ప్రశ్న 36.
సజాతి ఉత్ప్రేరణ అంటే ఏమిటి? ఇది విజాతి ఉత్ప్రేరణం నుంచి ఏ విధంగా భేదిస్తుంది?
జవాబు:
ఒక చర్యలో క్రియాజనకాలు, ఉత్ప్రేరకం అన్నీ ఒకే ప్రావస్థలో ఉన్నట్లైతే ఆ చర్యను సజాతి ఉత్ప్రేరణం అంటారు. క్రియాజనకాలు ఉత్ప్రేరకం, భిన్న ప్రావస్థలలో ఉండే ఉత్ప్రేరక చర్యను విజాతి ఉత్ప్రేరణం అంటారు.
ప్రశ్న 37.
సజాతి ఉత్ప్రేరణ చర్యలకు రెండు ఉదాహరణలు ఇవ్వండి.
జవాబు:
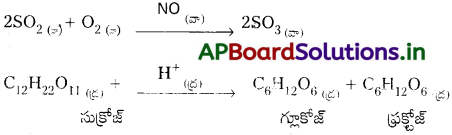
ప్రశ్న 38.
విజాతి ఉత్ప్రేరణ చర్యలకు రెండు ఉదాహరణలు ఇవ్వండి.
జవాబు:

ప్రశ్న 39.
విజాతి ఉత్ప్రేరణం ప్రదర్శించే వరణాత్మకతకు రెండు ఉదాహరణలు తెలపండి.
జవాబు:
ఈ క్రింది చర్యల ద్వారా విజాతి ఉత్ప్రేరణ వరణాత్మకత గురించి తెలుస్తుంది.
→ H2 మరియు CO లలో మొదలయి విభిన్న ఉత్ప్రేరకాల సమక్షంలో విభిన్న ఉత్పన్నాలు ఏర్పడతాయి.
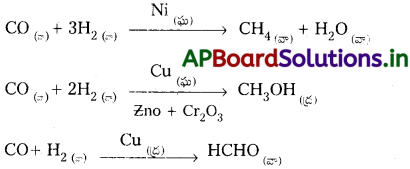
ఉత్ప్రేరక ప్రభావం సహజంగా వరణాత్మకమైనది.
ప్రశ్న 40.
జియోలైట్లను ఆకార వరణాత్మక ఉత్ప్రేరకాలు అని ఎందుకు అంటారు?
జవాబు:
ఉత్ప్రేరకంపై చోటుచేసుకొని ఉండే రంధ్రాల పరిమాణం ఆధారంగాను, క్రియజనకాల క్రియా జన్యాల అణువులు సాపేక్ష పరిమాణాల ఆధారంగాను జరిగే ఉత్ప్రేరక చర్యను ఆకార ఆధారిత వరణాత్మక ఉత్ప్రేరకం అంటారు. జియోలైట్లను తేనెపట్టు ఆకారంలోగల నిర్మాణం ఉండటం కారణంగా అవి ఆకార ఆధారిత వరణాత్మక ఉత్ప్రేరకాలుగా పనిచేస్తాయి.
ప్రశ్న 41.
ఆల్కహాల్లను గాసొలీన్ గా ప్రత్యక్షంగా మార్చే ఏ జియోలైట్ ఉత్ప్రేరకాన్ని ఉపయోగిస్తారు?
జవాబు:
పెట్రోలియం పరిశ్రమలో ఉపయోగించే ముఖ్యమైన జియోలైట్ ఉత్ప్రేరకం ZSM – 5 ఇది ఆల్కహాల్ల అనార్ద్రీకరణ చర్యకు గురిచేసే గాసోలిన్లుగా (పెట్రోల్) పిలిచే హైడ్రోకార్బన్ల మిశ్రమంగా మారుస్తుంది.
ప్రశ్న 42.
ఎంజైమ్లు అంటే ఏమిటి? మానవ శరీరంలో వీటి పాత్ర ఏమిటి?
జవాబు:
ప్రాణం గల మొక్కలు, జంతువులు ఉత్పత్తి చేసే సంక్లిష్ట నైట్రోజన్ కర్బన సమ్మేళనాలను ఎంజైమ్లు అంటారు.
- ఎంజైమ్లు జీవ రసాయనిక ఉత్ప్రేరకాలుగా పని చేస్తాయి.
- ఆయుఃప్రక్రియ కొనసాగడానికి దోహదం చేసే జంతువులు మొక్కలలో జరిగే చాలా రసాయన చర్యలను ఇవి ఉత్ప్రేరణం చేస్తాయి.
ప్రశ్న 43.
ఒక రసాయన దిగుబడిని ఉత్ప్రేరకం పెంచగలదా?
జవాబు:
ఒక రసాయన చర్య దిగుబడిని ఉత్ప్రేరకం పెంచదు. ఇది కేవలం చర్యవేగాన్ని పెంచుతుంది తద్వారా త్వరగా క్రియాజన్యం ఏర్పడేట్లు చేస్తుంది.
ప్రశ్న 44.
రెండు ఎంజైమ్ ఉత్ప్రేరణ చర్యలను తెలపండి. చర్యలు వ్రాయండి.
జవాబు:
చక్కెర విలోమ చర్య :
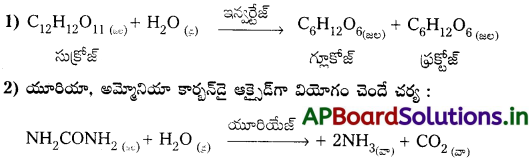
ప్రశ్న 45.
సోయాబీన్ల నుంచి లభించే ఎంజైమ్లు ఏవి?
జవాబు:
సోయాబీన్ ల నుంచి లభించే ఎంజైమ్లు యూరియేజ్
![]()
ప్రశ్న 46.
క్రింది వాటిలో ఉపయోగించే ఎంజైమ్లను తెలపండి.
ఎ) యూరియా, అమోనియా విఘటనం చెందడం
బి) ప్రోటీన్లు, పెప్టైడ్లుగా ఉదరంలో మారడం
జవాబు:
ఎ) యూరియా, అమ్మోనియాగా విఘటనం చెందటంలో ఉపయోగించే ఎంజైమ్ యూరియేజ్
బి) ఉదరంలో ప్రోటీన్లు పెప్టైడ్లుగా మార్చే ఎంజైమ్ పెప్సిన్
ప్రశ్న 47.
ఈస్ట్ నుంచి లభించే ఎంజైమ్లు ఏవి?
జవాబు:
ఈస్ట్ నుంచి లభించే ఎంజైమ్లు ఇన్వర్టేజ్, జైమేజ్ మరియు మాల్టేజ్
ప్రశ్న 48.
ఎంజైమ్లు అధిక క్రియాశీలతను ప్రదర్శించే ఉష్ణోగ్రత, pH ల పరిధులను తెలపండి.
జవాబు:
- ఎంజైమ్ క్రియాశీలతకు అనువైన ఉష్ణోగ్రత 298 – 310 K.
- pH విలువ 5 – 7 మధ్య ఎంజైమ్ల ఉత్ప్రేరకచర్య రేటు గరిష్టంగా ఉంటుంది.
ప్రశ్న 49.
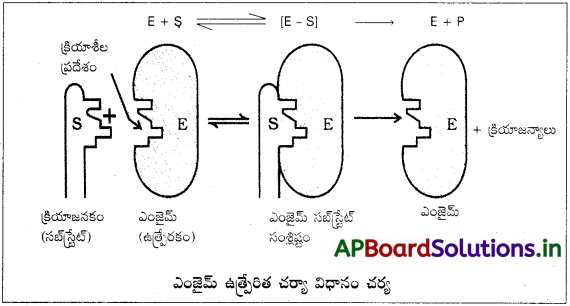
ఎంజైమ్ ఉత్ప్రేరణను పటం ద్వారా వివరించండి.
జవాబు:
ప్రశ్న 50.
పారిశ్రామిక ప్రాముఖ్యం గల రెండు విజాతి ఉత్ప్రేరణ చర్యలను పేర్కొని వాటిలోని ఉత్ప్రేరకాలను తెలపండి.
జవాబు:
i) హేబర్ పద్ధతి ద్వారా అమ్మోనియా తయారీ :
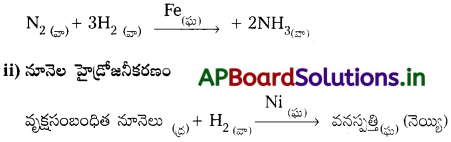
ప్రశ్న 51.
కొల్లాయిడ్ ద్రావణం అంటే ఏమిటి? ఇది నిజద్రావణం నుంచి విక్షిప్త కణం పరిమాణంలోను, సజాతి స్వభావంలోను ఏ విధంగా విభేదిస్తుంది?
జవాబు:
ఒక పదార్థంలో పెద్దసైజు కణాలుగా వేరొక పదార్థం విక్షేపణం చెంది ఏర్పరచిన విజాతి వ్యవస్థను కొల్లాయిడ్ ద్రావణం అంటారు.
- కొల్లాయిడల్ ద్రావణాలలో కణాల సైజు పరిమాణం 1 mµ – 1µ వరకు ఉంటాయి. నిజద్రావణాలలో కణాల సైజు < / mµ ఉంటాయి.
- కొల్లాయిడల్ ద్రావణం విజాతీయ ద్విగుణ వ్యవస్థ. నిజద్రావణం సజాతీయ ద్విగుణ వ్యవస్థ.
ప్రశ్న 52.
క్రింది కొల్లాయిడ్ వ్యవస్థలలో విక్షిప్త ప్రావస్థ విక్షేపణ యానకం వీటిని తెలపండి.
ఎ) పొగమంచు
బి) పొగ
సి) పాలు
జవాబు:
ఎ) పొగమంచు : విక్షిప్త ప్రావస్థ : ద్రవము
విక్షేపణ యానకం : వాయువు
(బి) పొగ : విక్షిప్త ప్రావస్థ : కార్బన్ కణాలు (ఘన)
విక్షేపణ యానకం : గాలి (వాయువు)
సి) పాలు : విక్షిప్త ప్రావస్థ : ద్రవరూప కొవ్వు
విక్షేపణ యానకం : నీరు
![]()
ప్రశ్న 53.
లయోధిలిక్, లయోఫోబిక్ సాల్లు అంటే ఏమిటి? ఒక్కొక్కదానికి ఒక్కొక్క ఉదాహరణ ఇవ్వండి.
జవాబు:
విక్షిప్త ప్రావస్థ(ద్రావితం) కణ పరిమాణం 1mµ – 1µ వరకు ఉండే ద్విగుణాత్మక విజాతి వ్యవస్థను కొల్లాయిడ్లు అంటారు.
కొల్లాయిడ్ల వర్గీకరణ :
విక్షిప్త ప్రావస్థ మరియు విక్షేపక యానకం మధ్యగల సంబంధం ఆధారంగా వర్గీకరణ జరిగింది.
ఎ) లయోఫిలిక్ కొల్లాయిడ్లు (ద్రవ ప్రియ కొల్లాయిడ్లు) :
వీటిలో విక్షేపక యానకంకూ, విక్షిప్త ప్రావస్థకీ మధ్య ఎక్కువ ఆపేక్ష ఉంటుంది.
ఉదా : స్టార్చ్ కొల్లాయిడ్ ద్రావణం లయోఫిలిక్.
బి) లయోఫోబిక్ కొల్లాయిడ్లు (ద్రవ విరోధి కొల్లాయిడ్లు) :
వీటిలో విక్షిప్త ప్రావస్థకూ, విక్షేపక యానకానికీ మధ్య ఆపేక్ష ఉండదు.
ఉదా : గోల్డ్ కొల్లాయిడ్ ద్రావణం లయోఫోబిక్.
ప్రశ్న 54.
క్రింది పదాలను సరయిన ఉదాహరణలతో వివరించండి.
ఎ) ఏరోసాల్ బి) హైడ్రోసాల్
జవాబు:
ఎ) ఏరోసాల్ :
ఏ కొల్లాయిడ్ ద్రావణంలో విక్షిప్త ప్రావస్థ ఘనపదార్థం విక్షేపణ యానకం గాలి (వాయువు) ఉంటుందో వాటిని ఎరోసాల్ అంటారు.
ఉదా : పొగ : విక్షిప్తప్రావస్థ : కార్బన్ కణాలు (ఘన)
విక్షేపణ యానకం : గాలి (వాయువు)
బి) హైడ్రోసాల్ :
ఏ కొల్లాయిడ్ ద్రావణంలో విక్షేపం యానకం నీరుగా ఉంటుందో వాటిని హైడ్రోసాల్ అంటారు.
ఉదా : పాలు : విక్షిప్తప్రావస్థ : ద్రవరూప క్రొవ్వు
విక్షేపణ యానకం : నీరు
ప్రశ్న 55.
లయోఫిలిక్ కొల్లాయిడ్లు, లయోఫోబిక్ కొల్లాయిడ్ల కంటే స్థిరంగా ఉంటాయి. కారణం తెలపండి.
జవాబు:
- లయోఫిలిక్ సాల్లు ఉత్రమణీయమైనవి. ఇవి స్కందనం జరుగవు. స్థిరంగా ఉంటాయి.
- లయోఫోబిక్ సాల్లు అనుత్రమణీయమైనవి. వీటికి విద్యుద్విశ్లేష్యాలను కలిపినపుడు అస్థిరంగా మారి స్కంధనం జరుగుతాయి. వీటిని స్థిరంగా మార్చుటకు లయోఫిలిక్ కొల్లాయిడ్లను కలుపవలెను.
ప్రశ్న 56.
ద్రవ, ఘపపదార్థంలో విక్షిప్తం అయి ఏర్పరచిన రెండు కొల్లాయిడ్ వ్యవస్థలకు ఉదాహరణలు ఇవ్వండి. ఈ కొల్లాయిడ్ ద్రావణం పేరు ఏమిటి?
జవాబు:
జున్ను వెన్న మరియు జెల్లీలు ద్రవ, ఘనపదార్థంలో నిక్షిప్తం అయి ఏర్పరిచిన కొల్లాయిడ్ వ్యవస్థలకు ఉదాహరణలు ఈ కొల్లాయిడ్ ద్రావణాల పేరు జెల్లు
ప్రశ్న 57.
బహుఅణుత, స్థూలఅణుత కొల్లాయిడ్ల మధ్య భేదం తెలపండి. ఒక్కొక్క దానిని ఒక్కొక్క ఉదారణ ఇవ్వండి.
జవాబు:
బహుఅణుత కొల్లాయిడ్లు :
అధిక సంఖ్యలో విక్షిప్త ప్రావస్థలోని పరమాణువులు లేదా లఘు అణువుల సముచ్చయం చెంది కొల్లాయిడ్ `సైజు జాతులను ఏర్పరుస్తాయి. ఇలా ఏర్పడిన జాతులను బహు అణుత కొల్లాయిడ్లు అంటారు.
ఉదా : సల్ఫర్సాల్
స్థూల (లేదా) బృహత్ అణుకొల్లాయిడ్లు :
అనువైన ద్రావణిలో బృహత్ అణువులను కరిగిస్తే కొల్లాయిడ్ కణాల పరిధిలో ఉండే కణాలు ఉన్న ద్రావణాలు ఏర్పడతాయి. ఈ వ్యవస్థలను బృహత్ అణు కొల్లాయిడ్లు అంటారు.
ఉదా : స్టార్చ్, సెల్యులోజ్
ప్రశ్న 58.
మిసెల్లు అంటే ఏమిటి? ఒక ఉదాహరణ ఇవ్వండి.
జవాబు:
కొన్ని పదార్థాలు అల్పగాఢతల వద్ద సాధారణ బలమైన విద్యుద్విశ్లేషకాలుగా ప్రవర్తించే పదార్థాలు. అయితే అధిక గాఢతల వద్ద కొల్లాయిడ్ల ప్రవర్తనను ప్రదర్శిస్తాయి. దీనికి కారణం సముచ్ఛములను ఏర్పరచడం ఈ విధంగా సముచ్ఛయం చెంది ఏర్పడిన కణాలను మిసెల్లు అంటారు.
ఉదా : సబ్బులు, డిటర్జంట్లు మిసెల్లను ఏర్పరుస్తాయి.
![]()
ప్రశ్న 59.
సాధారణ కొల్లాయిడ్ ద్రావణానికి, మిసెల్లకు గల భేదం ఏమిటి?
జవాబు:
- కొన్ని పదార్థాలు అల్పగాఢతల వద్ద సాధారణబలమైన విద్యుద్విశ్లేషకాలుగా ప్రవర్తించే పదార్థాలు, అయితే అధిక గాఢతల వద్ద కొల్లాయిడ్ల ప్రవర్తనను ప్రదర్శిస్తాయి. దీనికి కారణం సముచ్ఛములను ఏర్పరచడం ఈ విధంగా సముచ్ఛయం చెంది ఏర్పడిన కణాలను మిసెల్లు అంటారు.
- వీటినే సముచ్ఛయ కొల్లాయిడ్లు అంటారు.
- ఇవి లయోఫిలిక్, లయోఫోబిక్ భాగాలు కలిగి ఉంటాయి.
- మిసెల్లలో 100 లేదా అంతకంటే ఎక్కువ సంఖ్యలో సాధారణ అణువులు ఉంటాయి.
- కొల్లాయిడ్ ద్రావణం విలీనంలో ఈ కొల్లాయిడ్లు వ్యక్తిగత విద్యుద్విశ్లేష్యకాలుగా తిరిగి మారతాయి.
ప్రశ్న 60.
సహచరిత కొల్లాయిడ్లకు రెండు ఉదాహరణలు తెలపండి.
జవాబు:
ఉపరితల క్రియాశీలతగల కారకాలు అయిన సబ్బులు, సంశ్లేషిత డిటర్జంట్లు సహచరిత కొల్లాయిడ్లకు ఉదాహరణలు.
ప్రశ్న 61.
ఒకే పదార్థం కొల్లాయిడ్గాను, క్రిస్టలాయిడ్గాను ప్రవర్తించగలదా?
జవాబు:
మిసెల్లు కొల్లాయిడ్గానూ, క్రిస్టలాయిడ్లుగాను ప్రవర్తించగలవు. అల్పగాఢతల వద్ద సాధారణ బలీయమైన విద్యుద్విశ్లేష్యకాలుగా, అధికగాఢతల వద్ద కొల్లాయిడ్లుగా ప్రవర్తిస్తాయి.
ప్రశ్న 62.
లయోఫోబిక్ కొల్లాయిడ్లకు రెండు ఉదాహరణలు తెలపండి.
జవాబు:
లోహసాల్లు, లోహసల్ఫైడ్సాల్లు లయోఫోబిక్ కొల్లాయిడ్లకు ఉదాహరణలు గోల్డ్సెల్ ఒక లయోఫోబిక్సాల్.
ప్రశ్న 63.
క్రింది కొల్లాయిడ్ వ్యవస్థలకు ఉదాహరణలు తెలపండి.
ఎ) ఘనపదార్థంలో ద్రవం
బి) ఘనపదార్థంలో వాయువు
జవాబు:
ఎ) ఘనపదార్థంలో ద్రవం :
ఘనపదార్ధంలో ద్రవం రకమైన కొల్లాయిడ్ వ్యవస్థకు ఉదాహరణలు జున్ను, వెన్న, జెల్లీలు
బి) ఘనపదార్థంలో వాయువు :
ఘనపదార్ధంలో వాయువు రకమైన కొల్లాయిడ్ వ్యవస్థకు ఉదాహరణలు ప్యూమిస్ రాళ్లు, ఫోమ్బ్బరు.
ప్రశ్న 64.
లయోఫోబిక్ కొల్లాయిడ్లను ఏ పదార్థాలు ఏర్పరుస్తాయి?
జవాబు:
లోహసాల్లు, లోహసల్ఫైడ్సాల్లు లయోఫోబిక్ కొల్లాయిడ్లకు ఉదాహరణలు గోల్డ్సెల్ ఒక లయోఫోబిక్సాల్.
ప్రశ్న 65.
సందిగ్ధ మిసెల్ గాఢత (Tk), క్రాఫ్ట్ ఉష్ణోగ్రత (CMC) అంటే ఏమిటి?
జవాబు:
ఒక ప్రత్యేకమైన గాఢత కంటే అధిక గాఢతల వద్ద మాత్రమే మిసెల్ ఏర్పడుతుంది. ఈ గాఢతను సంధిగ్ధమిసెల్ గాఢత (CMC) అంటారు.
ఒక ప్రత్యేక ఉష్ణోగ్రత కంటే అధిక ఉష్ణోగ్రత వద్ద మాత్రమే మిసెల్ ఏర్పడతాయి. ఈ ఉష్ణోగ్రతను క్రాఫ్ట్ ఉష్ణోగ్రత (Tk) అంటారు.
ప్రశ్న 66.
లయోఫోబిక్ కొల్లాయిడ్లను ఎందుకు ఉత్రమణీయం కానివి అంటారు?
జవాబు:
లయోఫోబిక్ కొల్లాయిడ్లు స్థిరమైనవి కావు. వీటికి విద్యుద్విశ్లేష్యాలు కలిపినపుడు స్కంధనం (అవక్షేపాలు) జరగుతాయి. ఏర్పడిన అవక్షేపానికి విక్షేపణ యానకాన్ని కలిపి గిలకరిస్తే తిరిగి ఈ కొల్లాయిడ్ సాల్లు ఏర్పడవు. అందువల్ల వీటిని అనుత్రమణీయ సాల్లు అంటారు.
![]()
ప్రశ్న 67.
ఆర్సీనియస్ సల్ఫైడ్ సాల్ను ఎలా తయారు చేస్తారు?
జవాబు:
As2O3 మరియు H2S లను ధ్వంద్వవియోగ చర్య ద్వారా ఆర్సీనియస్ సల్ఫైడ్ సాల్ను తయారు చేస్తారు.
![]()
ప్రశ్న 68.
పెష్టీకరణం అంటే ఏమిటి?
జవాబు:
పెష్టీకరణం :
విక్షేపణ యానకంలో ఉన్న ఒక అవక్షేపానికి కొద్ది ప్రయాణంలో ఒక విద్యుద్విశ్లేష్యాన్ని కలిపి బాగా కుదపడం ద్వారా అవక్షేపాన్ని కొల్లాయిడల్ స్థితికి మార్చడాన్ని పెష్టీకరణం అంటారు.
ప్రశ్న 69.
డయాలిసిస్ అంటే ఏమిటి? డయాలిసిస్ ఎలా వేగపరుస్తారు?
జవాబు:
డయాలిసిస్ :
అనువైన పటలం లేదా పొరను ఉపయోగించి కరిగే స్థితిలో ఉండే పదార్థాలను కొల్లాయిడ్ ద్రావణం నుండి తొలగించే ప్రక్రియను డయాలిసిస్ అంటారు.
ప్రశ్న 70.
కొల్లోడియన్ ద్రావణం అంటే ఏమిటి?
జవాబు:
ఆల్కహాల్ – ఈథర్ 40% మిశ్రమంలో కరిగించిన నైట్రో సెల్యులోజ్న కొల్లోడియన్ ద్రావణం అంటారు.
ప్రశ్న 71.
సాధారణ వడపోత కాగితం నుంచి సూక్ష్మ వడపోత కాగితాన్ని ఎలా తయారుచేస్తారు?
జవాబు:
కొల్లోడియన్ ద్రావణంలో వడపోతలో ఉపయోగించే కాగితాన్ని నానబెట్టి, ఫార్మాల్డీహైడ్ సహాయంతో గట్టిపరచి చివరగా ఆరపెట్టి సూక్ష్మ నిర్గలన పటాలను తయారు చేస్తారు.
ప్రశ్న 72.
టిండాల్ ఫలితం అంటే ఏమిటి?
జవాబు:
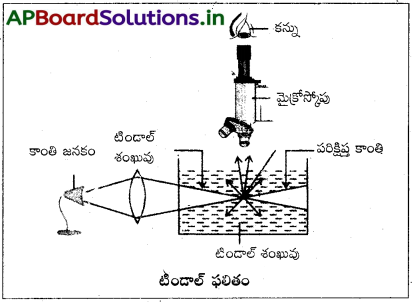
టిండాల్ ఫలితం :
“కాంతి, కొల్లాయిడ్ ద్రావణం ద్వారా ప్రయాణించినప్పుడు, కాంతి మార్గాన్ని మనం ఒక కాంతివంతమైన పుంజంగా చూడవచ్చు. ఈ దృగ్విషయాన్నే “టిండాల్ ఫలితం” అంటారు.
ఇది ఒక దృక్ ధర్మం.
కారణము :
కొల్లాయిడ్ ద్రావణం ద్వారా కాంతి ప్రసరించినప్పుడు ఆ కాంతి పెద్దసైజు కణాలు అయిన కొల్లాయిడ్ల విక్షిప్త, ప్రావస్థా కణాలలో పరిక్షేపణం చెందుతాయి.
- ఆకాశము నీలంగా ఉండటానికి టిండాల్ ప్రభావమే కారణము.
- నిజద్రావణాలు టిండాల్ ప్రభావాన్ని ప్రదర్శించవు.
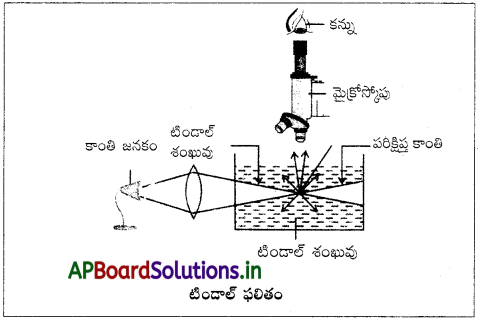
ప్రశ్న 73.
ఏ పరిస్థితులలో టిండాల్ ఫలితం కనిపిస్తుంది?
జవాబు:
ఈక్రింది నియమాలు పాటించినపుడే టిండాల్ ఫలితం గమనించగలము.
- కొల్లాయిడ్ కణాల వ్యాసం ఉపయోగించిన కాంతి కిరణం తరంగదైర్ఘ్యం కంటే చాలా తక్కువగా ఉండకూడదు.
- విక్షిప్త ప్రావస్థ, విక్షేపణ యానకం వీటి వక్రీభవన గుణకం విలువల మధ్య భేదం అధికంగా ఉండాలి. టిండాల్ ఫలితాన్ని నిజద్రావణాన్ని, కొల్లాయిడ్ ద్రావణాన్ని గుర్తించడానికి ఉపయోగిస్తారు.
ప్రశ్న 74.
కొల్లాయిడ్ ద్రావణాన్ని, నిజద్రావణాన్ని భేదపరచడానికి టిండాల్ ఫలితం ఉపయోగపడుతుందా? వివరించండి.
జవాబు:
‘కొల్లాయిడ్ ద్రావణం, నిజద్రావణంను భేదపరచడానికి ఉపయోగపడును.
సజాల బ్రావణం (నిజద్రావణం) ను చీకటిలో ఉంచి దానిగుండా కాంతి కిరణాన్ని ప్రసారం చేస్తే కాంతి కిరణం పోయే “దిశలోనే దానిని పరిశీలిస్తే ద్రావణం నిర్మలంగానే కనిపిస్తుంది. కాంతి కిరణం ప్రయాణించే దిశను లంబదిశలో ద్రావణాన్ని పరిశీలిస్తే ద్రావణం నలుపురంగులో కనిపిస్తుంది.
కొల్లాయిడ్ ద్రావణాలను కూడా ఇదే విధంగా కాంతికిరణ దిశలో పరిశీలించినట్లైతే అవి నిర్మలంగా లేదా అర్ధపారదర్శకంగా మసకగా కనిపిస్తుంది. కాంతి కిరణ ప్రయాణదిశకు లంబదిశలో పరిశీలించినట్లైతే కొల్లాయిడ్ ద్రావణాలు బలహీన లేదా బలమైన క్షీరదీప్తిరూపంలో కనిపిస్తాయి. కాంతికిరణం ప్రయాణించే మార్గం నీలిరంగు కాంతిలో కనిపిస్తుంది. దీనినే టిండాల్ ఫలితం అంటారు.
![]()
ప్రశ్న 75.
ఆకాశం నీలిరంగులో కనిపిస్తుంది. ఎందుకు?
జవాబు:
గాలిలో అవలంబనం చెంది ఉన్న ధూళి కణాలు నీటి ఆవిరి ద్వారా సౌరకాంతి పరిక్షేపణం చెంది నీలిరంగు కాంతి మన కంటిని చేరుతుంది. ఈ కారణంగా ఆకాశం నీలంగా కనిపిస్తుంది.
ప్రశ్న 76.
బ్రౌనియన్ చలనం అంటే ఏమిటి?
జవాబు:
బ్రౌనియన్ చలనం :
“కొల్లాయిడ్ కణాలు, విక్షేపణ యానకంలో నిరంతరం వేగంగా మరియు అస్తవ్యస్తంగా చలించడాన్ని “బ్రౌనియన్ చలనం” అంటారు. ఇది ఒక గతిజ ధర్మము.
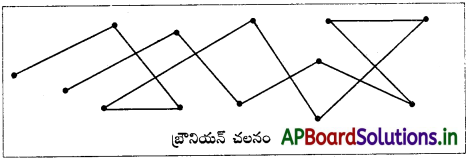
ఈ దృగ్విషయాన్ని “జిగ్మండీ” అను శాస్త్రవేత్త కనుగొన్నాడు.
కారణము :
విక్షేపణ యానక అణువులకు, కొల్లాయిడ్ కణాలకు మధ్య తుల్యము కాని అభిఘాతాల కారణంగా బ్రౌనియన్ చలనం ఉంటుంది.
ప్రశ్న 77.
కొల్లాయిడ్ ద్రావణంపై ఆవేశం ఉండటానికిగల కారణం ఏమిటి?
జవాబు:
కొల్లాయిడ్ కణాలు ఆవేశాన్ని సంతరించుకోవడానికి కారణం లోహాలు ఎలక్ట్రోడ్పై నిక్షిప్తం అయినపుడు ఆ లోహాలు ఎలక్ట్రాన్లను బంధించి ఉంచటం మరియు ద్రావణంలో ఉండే ఇతర అయాన్లను కొల్లాయిడ్ కణం అధిశోషించుకోవడం.
ప్రశ్న 78.
ఎలక్ట్రోకైనెటిక్ పొటెన్షియల్ లేదా జీటా పొటెన్షియల్ అంటే ఏమిటి?
జవాబు:
విరుద్ధ ఆవేశాలు గల స్థిర పటలం, విసరిత పటలం మధ్యగల పొటెన్షియల్ బేధాన్ని విద్యుత్ గతిక పొటెన్షియల్ (లేదా) జీటా -పొటెన్షియల్ అంటారు. ఇది ధన లేదా ఋణ విలువలో ఉంటుంది.
ప్రశ్న 79.
ధనావేశం, రుణావేశం గల ఆర్ద్ర ఫెర్రిక్ ఆక్సైడ్ కొల్లాయిడ్ ద్రావణాల ఫార్ములాలను వ్రాయండి.
జవాబు:
- ధనావేశం గల ఆర్ధఫెర్రిక్ కొల్లాయిడ్ ద్రావణ ఫార్ములా Fe2O3.xH2O/Fe+3
- ఋణావేశం గల ఆర్ధఫెర్రిక్ కొల్లాయిడ్ ద్రావణ ఫార్ములా Fe2O3.xH2O/OH–
ప్రశ్న 80.
ధనావేశ కొల్లాయిడ్ల స్కందనంలో Cl–, SO2-4, PO3-4 అయాన్ల స్కందన సామర్థ్య క్రమాన్ని తెలపండి
జవాబు:
ధనావేశ కొల్లాయిడ్ స్కందనంలో Cl–, SO2-4, PO3-4 అయాన్ల స్కందన సామర్థ్యక్రమం PO43- > SO42- > Cl–
ప్రశ్న 81.
Na+, Ba2+, Al3+, లలో ఏది రుణావేశ కొల్లాయిడ్ను సులభంగా స్కందనం చేస్తుంది? కారణం ఏమిటి?
జవాబు:
Na+, Ba2+, Al3+ లలో రుణావేశ కొల్లాయిడ్ను సులభంగా స్కంధనం చేసేది Al3+ అయాన్ ఆవేశం ఎక్కువగా ఉన్నచో స్కంధన సామర్ధ్యం అధికంగా ఉండును.
ప్రశ్న 82.
AgI కొల్లాయిడ్ ద్రావణాన్ని Ag+ అయాన్లు అధికంగా గల ద్రావణం నుంచి తయారుచేసినప్పుడు ధనావేశంగాను, I– అయాన్లు అధికంగా గల ద్రావణం నుంచి తయారుచేసినప్పుడు రుణావేశంగాను ఉంటుంది. వివరించండి.
జవాబు:
అధిక పరిమాణంలో తీసుకొన్న విలీన KI ద్రావణానికి, విలీన AgNO3 ద్రావణాన్ని కలిపితే, ఏర్పడిన AgI అవక్షేపం అధికపరిమాణంలోగల ఉభయ సామాన్య అయాన్ I– ను అధిశోషించుకొంటుంది. ఫలితంగా రుణావేశ AgI కొల్లాయిడ్ ద్రావణం ఏర్పడుతుంది. అధిక పరిమాణంలో తీసుకొన్న AgNO3 ఎలీన ద్రావణానికి, విలీన KI ద్రావణం కలిపినట్లైతే, ఏర్పడిన Agl అవక్షేపం, అధికపరిమాణంలోగల ఉభయ సామాన్య అయాన్ Ag+ ను అధిశోషించుకొటుంది. ఫలితంగా ధనావేశ AgI కొల్లాయిడ్ ద్రావణం ఏర్పడుతుంది. సాధారణంగా విక్షిప్త ప్రావస్థలో ఉండే ఒక అయానన్ను కొల్లాయిడ్ కణం అధిశోషించుకొంటుంది.

ప్రశ్న 83.
విద్యుదావేశిత కణచలనం (ఎలక్ట్రోఫోరెసిస్) అంటే ఏమిటి?
జవాబు:
అనువర్తిత emf ప్రభావంతో కొల్లాయిడ్ కణం చలనం చెందే ప్రక్రియను విద్యుదావేశితకణ చలనం (లేదా) ఎలక్ట్రోఫోరసిస్ అంటారు.
ప్రశ్న 84.
విద్యుత్ ద్రవాభిసరణం (ఎలక్ట్రోఆస్మాసిస్) అంటే ఏమిటి?
జవాబు:
కొల్లాయిడ్ కణాల చలనాన్ని అనువైన పద్ధతిలో ఆపగల్యీ విక్షేపణ యానకం వ్యతిరేక దిశలో ప్రయాణిస్తుంది. దీనిని విద్యుత్ ద్రవాభిసరణం అంటారు.
![]()
ప్రశ్న 85.
స్కందనం అంటే ఏమిటి?
జవాబు:
సాల్ కొల్లాయిడ్ కణాలు పాత్ర అడుగు భాగానికి చేరి స్థిరపడే ప్రక్రియను సాల్స్కందనం లేదా అవక్షేపణం లేదా ఫ్లాక్యులేషన్ అంటారు.
ప్రశ్న 86.
ప్లాక్యులేషన్ విలువను నిర్వచించండి.
జవాబు:
రెండు గంటల కాలవ్యవధిలో ఒక సాల్ను స్కందనం చేయడానికి అవసరమైన మిల్లీ మోల్ల విద్యుద్విశ్లేష్య కనిష్ఠ గాఢతను స్కంధన విలువ అంటారు.
ప్రశ్న 87.
హార్డీ-షూల్జ్ నియమం తెలపండి.
జవాబు:
సామాన్యంగా స్కందన అయాన్ వేలన్సీ పెరిగిన కొలది దాని స్కందన సామర్ధ్యం పెరుగును. దీనినే హార్డీ – షూల్జ్ నియమం అంటారు.
ప్రశ్న 88.
ఆర్ద్ర ఫెర్రిక్ క్లోరైడ్ కొల్లాయిడ్ ద్రావణానికి సోడియమ్ క్లోరైడ్ ద్రావణం కలిపితే స్కందనం జరుగుతుంది. వివరించండి.
జవాబు:
ఆర్ద్ర ఫెర్రిక్ క్లోరైడ్ కొల్లాయిడ్ ద్రావణానికి NaCl ద్రావణం కలిపితే స్కందనం జరుగుతుంది. ఇచ్చట కొల్లాయిడ్ కణాలమీది ఆవేశాలు పరస్పరం తటస్థపరచబడి అవక్షేపణం చెందుతాయి.
ప్రశ్న 89.
లయోఫోబిక్ కొల్లాయిడ్లను స్కందనం ఘటన నుంచి ఎలా పరిరక్షిస్తారు?
జవాబు:
లయోఫిలిక్ కొల్లాయిడు లయోఫోబిక్ కొల్లాయిడ్కు కలుపుట ద్వారా వాటి స్కందన ఘటన నుండి పరిరక్షిస్తారు.
ప్రశ్న 90.
పరిరక్షణ కొల్లాయిడ్ అంటే ఏమిటి?
జవాబు:
లయోఫిలిక్ కొల్లాయిడ్ను లయోఫోబిక్ కొల్లాయిడ్కు కలుపుట ద్వారా వాటి స్కందన ఘటన నుండి పరిరక్షిస్తారు.
→ లయోఫిల్లిక్ కొల్లాయిడ్లను పరిరక్షక కొల్లాయిడ్లు అంటారు.
ప్రశ్న 91.
ఎమల్షన్ అంటే ఏమిటి ? రెండు ఉదాహరణలు తెలపండి. [AP. Mar.’17]
జవాబు:
ఎమల్షన్ :
“ద్రవ విక్షేపక యానకంలో, సూక్ష్మ విభాజిత ద్రవబిందు కణాలు విక్షిప్తం చెంది ఏర్పరిచే వ్యవస్థే ఎమల్షన్”.
(లేదా)
విక్షిప్త ప్రావస్థ మరియు విక్షేపక యానకం రెండూ ద్రవాలే అయిన కొల్లాయిడ్ వ్యవస్థను ‘ఎమల్షన్’ అంటారు.
ఉదా : పాలు – ద్రవ క్రొవ్వు నీటిలో విక్షిప్తం చెంది ఉండే ఎమల్షన్.
ప్రశ్న 92.
ఎమల్షన్లను ఎలా వర్గీకరిస్తారు? ఒక్కొక్క రకానికి ఒక్కొక్క ఉదాహరణ ఇవ్వండి. [AP. Mar.’17]
(ఎ) నీటిలో తైలం (O / W) రకం ఎమల్షన్లు :
వీటిలో విక్షిప్త ప్రావస్థ : తైలం
విక్షేపక యానకం : నీరు
ఉదాహరణలు :
i) పాలు – నీటిలో ద్రవ కొవ్వు ఏర్పరచే ఎమల్షన్
ii) వానిషింగ్ క్రీమ్ : నీటిలో క్రొవ్వు
(బి) తైలంలో నీరు (W / O) రకం ఎమల్షన్లు
వీటిలో విక్షిప్త ప్రావస్థ : నీరు
విక్షేపక యానకం : తైలం
ఉదాహరణలు :
i) గట్టి గ్రీజులు : కందెన తైలాల్లో నీరు
ii) కోల్డ్ క్రీమ్ : క్రొవ్వులో నీరు
ప్రశ్న 93.
ఎమల్సీకరణ కారకం అంటే ఏమిటి?
జవాబు:
ఒక ఎమల్షన్ స్థిరంగా ఉండేందుకు దానికి చేర్చే మూడో పదార్థమే ఎమల్సీకరణ కారకము. ఉదా : సబ్బులు – నీటిలో కిరోసిన్ ఎమల్షనన్ను స్థిరపరుస్తారు.
![]()
ప్రశ్న 94.
డీఎమల్సీకరణం అంటే ఏమిటి? రెండు డీఎమల్సీఫయర్లను తెలపండి.
జవాబు:
ఒక ఎమల్షన్ దానిలోని అనుఘటక ద్రవాలుగా వేరు పడే ప్రక్రియను డీఎమల్సీకరణం అంటారు.
వేడిచేయడం, ఘనీభవించుట ద్వారా డీ ఎమల్సీకరణం చేయవచ్చు.
ప్రశ్న 95.
కృత్రిమ వర్షాన్ని ఎలా సృష్టిస్తారు?
జవాబు:
విద్యుదీకరణం చెందించిన ఇసుకరేణువులను లేదా మేఘాల విద్యుదావేశానికి విరుద్ధ విద్యుదావేశం గల సాల్ కణాలను విమానాల ద్వారా వాతావరణంలోకి పిచికారీ చేయడం ద్వారా కృత్రిమ వర్షాన్ని కురిపిస్తారు.
ప్రశ్న 96.
అప్పుడే జరిగిన చర్మం కోత నుంచి కారే రక్తాన్ని పటిక ద్వారా ఆపుతారు. కారణాలు తెలపండి.
జవాబు:
అప్పుడే జరిగిన చర్మం కోతనుండి కారే రక్తాన్ని పటిక ద్వారా ఆపుతారు. దీనికి కారణం రక్త స్రావాన్ని నిరోధించే (స్ట్రిప్టిక్) చర్య కలిగి ఉంటుంది.
ప్రశ్న 97.
నది సముద్రాన్ని కలిసే స్థానాల వద్ద డెల్టాలు ఏర్పడతాయి. ఎందువల్ల?
జవాబు:
నదీజలాలను బంకమట్టి కొల్లాయిడ్ ద్రావణాలుగా భావిస్తాం. సముద్రం నీటిలో చాలా విద్యుత్ విశ్లేష్యకాలు కరిగి ఉన్నాయి. కాబట్టి నదీజలం, సముద్రం నీటితో కలిసినప్పుడు సముద్రపు నీటిలోని విద్యుద్విశ్లేష్యకాలు బంకమట్టి కొల్లాయిడ్ ద్రావణాన్ని స్కందన ప్రక్రియకు గురి చేస్తాయి. ఫలితంగా నదీజలంలోని బంకమట్టి, డెల్టాలుగా ఏర్పడుతుంది.
ప్రశ్న 98.
కొల్లాయిడ్ ద్రావణాల రెండు ఉపయోగాలను తెలపండి.
జవాబు:
ఫోటోగ్రాఫిక్ ప్లేట్లు, ఫిల్మ్ లు :
గాజు పలకలపై లేదా సెల్యులాయిడ్ ఫిల్మ్ పై జిలటీన్లో కరిగించిన కాంతితో చర్య జరపగలిగే సిల్వర్ బ్రోమైడ్ ఎమల్షన్ను పూతగా పూసి ఫోటోగ్రాఫిక్ ఫిల్మ్ ను ప్లేట్లను తయారుచేస్తారు.
రబ్బరు :
మొక్కలు ఏర్పరచే రుణావేశ రబ్బరు కణాల కొల్లాయిడ్ ద్రావణాన్ని లాటెక్స్ (జిగురు పదార్థం) అంటారు. ఈ లాటెక్స్ నుంచి రబ్బరును స్కందనం ప్రక్రియ ద్వారా వేరుపరుస్తారు.
ప్రశ్న 99.
పొగలోని కొల్లాయిడ్ కణాల ద్వారా కలిగే గాలి కాలుష్యాన్ని ఎలా నివారిస్తారు? వివరించండి.
జవాబు:
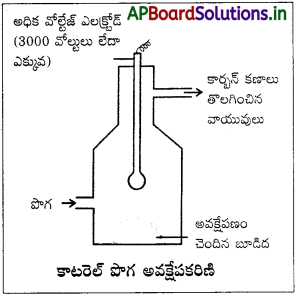
పొగ గొట్టాలనుంచి బహిర్గతం అయ్యే పొగను విద్యుత్ అవక్షేపణం చర్యకు గురిచేయడం :
కార్బన్, ఆర్సినిక్ సమ్మేళనాలు, ధూళి కణాలు మొదలైన ఘనస్థితిలో ఉండే కణాలు గాలిలో ఏర్పరచే కొల్లాయిడ్ ద్రావణమే పొగ, పొగగొట్టం నుంచి పొగ బయటకు వచ్చే ముందుగానే అవక్షేపకరిణి ద్వారా పంపుతారు. దీనిలో పొగ కణాల ఆవేశానికి విరుద్ధంగా ఉండే ఆవేశంగల ప్లేట్లు అమర్చి ఉంటాయి. కాబట్టి పొగలోని కణాలు వీటితో సంపర్కానికి వచ్చిన వెంటనే అవి వాటి ఆవేశాన్ని కోల్పోయి అవక్షేపణం చెందుతాయి. కాబట్టి గది నేలపై ఈ కణాలు స్థిరపడతాయి. ఈ అవక్షేపకరిణిని కాటరెల్ అవక్షేపకరిణి అంటారు.
ప్రశ్న 100.
ప్రకృతి వనరుల నుంచి వచ్చే నీటిని శుద్ధి చేయడానికి పటికను వాడతారు వివరించండి.
జవాబు:
ప్రకృతి వనరుల నుంచి లభ్యం అయిన నీటిలో సామాన్యంగా మలినాలు అవలంబనం చెంది ఉంటాయి. ఈ నీటికి పటికను కలిపినట్లైతే, అవలంబిత కణాలు స్కందన ప్రక్రియకు గురి అవుతాయి. ఆ నీరు త్రాగడానికి అనువుగా ఉంటుంది.
ప్రశ్న 101.
కొల్లాయిడ్ స్థితిలో ఉండే ఔషధాలు ఎందుకు అధిక క్రియాశీలత చూపుతాయి?
జవాబు:
చాలా ఔషధాలు స్వభావంలో కొల్లాయిడ్లుగానే ఉన్నాయి. ఉదాహరణకు కంటి లోషన్గా వాడే ఆర్జిరోల్ అనేది సిల్వర్సాలి. కలాజార్ అనే వ్యాధిని నయం చేయడానికి ఆంటిమొనీ కొల్లాయిడ్ వాడతారు. కొల్లాయిడల్ గోల్డ్ను కండరాంతర (intram iscular) ఇంజెక్షన్గా వాడతారు. ఉదర అస్వస్థతలకు, మిల్క్ ఆఫ్ మెగ్నీషియా’ అనే ఎమల్షన్ ఉపయోగిస్తారు. కొల్లాయిడ్ల రూపంలో ఉండే ఔషధాలు చాలా ప్రభావితంగా ఉంటాయి. ఎందుకంటే వీటి ఉపరితల వైశాల్యం అధికంగా ఉండటం కారణంగా ఇవి సులభంగా శరీరంలో జీర్ణించుకొంటాయి.
ప్రశ్న 102.
లాటెక్స్ నుంచి రబ్బరును ఎలా పొందుతారు?
జవాబు:
మొక్కలు ఏర్పరచే రుణావేశ. రబ్బరు కణాల కొల్లాయిడ్ ద్రావణాన్ని లాటెక్స్ (జిగురు పదార్థం) అంటాం. ఈ లాటెక్స్ నుంచి రబ్బరును స్కందనం ప్రక్రియ ద్వారా వేరుపరుస్తారు.
![]()
ప్రశ్న 103.
పాలు ఏ రకం ఎమల్షన్కు చెందినవి?
జవాబు:
పాలు నీటిలో తైలం (0/w) రకం ఎమల్షన్ :
ద్రవకొవ్వు నీటిలో విక్షిప్తం చెంది ఏర్పడిన కొల్లాయిడ్ ద్రావణమే “పాలు కొల్లాయిడ్”.
విక్షిప్త వ్యవస్థ : ద్రవ కొవ్వు (ద్రవం)
విక్షేపక యానకం : నీరు (ద్రావణం)
రకము : రెండు ద్రవాలే కాబట్టే ఇది ఒక “ఎమల్షన్”.
స్వల్ప సమాధాన ప్రశ్నలు
ప్రశ్న 1.
అధిశోషణం అంటే ఏమిటి? ఘనపదార్థాలపై వాయువులు ప్రదర్శించే అధిశోషణం చర్యా విధానాన్ని చర్చించండి.
జవాబు:
అధిశోషణం :
“ఒక పదార్థం వేరొక ద్రవం లేదా ఘన పదార్థం ఉపరితలంపై గాఢత చెందడాన్ని ‘అధిశోషణం’ అంటారు. ఇది ఒక ఉపరితల దృగ్విషయము.
ఉదా : i) CO2, SO2, Cl2 లాంటి వాయువులను ఉత్తేజిత బొగ్గు అధిశోషించుకుంటుంది.
ii) Pt లేక Ni లోహం, హైడ్రోజన్ వాయువుతో సంపర్కంలో ఉంటే ఆ వాయువును అధిశోషించుకుంటుంది.
ఘనపదార్థాలపై వాయువులు ప్రదర్శించే అధిశోషణం చర్యా విధానం :
పదార్థం ఉపరితలంపై చోటుచేసుకొని ఉన్న పదార్థ కణాలు అన్నీ ఒకే రసాయనిక వాతావరణంలో ఉండవు. అయితే పదార్థ అంతర్భాగంలోని కణాలు మాత్రం ఒకే వాతావరణంలో ఉంటాయి. అధిశోషకం అంతర్భాగంలోని కణాల మధ్య ఉండే బలాలు అన్నీ ఒకదానిని ఒకటి తుల్యం చేస్తాయి. అయితే ఉపరితలంపై ఉండే కణాల చుట్టూ అన్నివైపులా పరివేష్టితమై ఉండే పరమాణువులు, అణువులు ఈ కణాలకు చెందినవి కావు. కాబట్టి ఇవి తుల్యం కావు. అంటే అవశేష బలాలను పొంది ఉంటాయి. ఈ బలాలు, అధిశోషిత పదార్థ అణువులు అధిశోషకం ఉపరితలంపై సాంద్రీకృతం కావడానికి లేదా ఆకర్షితమవడానికి కారణంగా ఉన్నాయి. నిర్దేశిత ఉష్ణోగ్రత, పీడనం వద్ద ఏకాంక ద్రవ్యరాశి గల అధిశోషకం ఉపరితలం పెరుగుదలతో అధిశోషణం విస్తృతి కూడా పెరుగుతుంది.
అధిశోషణానికి సంబంధించిన వేరొక ముఖ్య అంశం అధిశోషణోష్టం. అధిశోషణం ప్రక్రియలో అధిశోషకం ఉపరితలంపై ఉండే అవశేష బలాల సంఖ్య తగ్గుతుంది. అంటే ఉపరితల శక్తి తగ్గుతుంది. ఇలా తగ్గిన శక్తి ఉష్ణరూపంలో వెలువడుతుంది. కాబట్టి అధిశోషణ పక్రియ ప్రధానంగా ఉష్ణమోచక చర్యగానే ఉంటుంది. అంటే అధిశోషణం ∆H విలువ రుణ విలువలో ఉంటుంది. అధిశోషణం ప్రక్రియ ఎంథాల్పీ తగ్గుదలను, ఎంట్రోపీ తగ్గుదలను కూడా ప్రదర్శించే చర్యగానే ఉంటుంది. నిర్దేశిత ఉష్ణోగ్రత, పీడనాల వద్ద ఒక చర్య అయత్నీకృతంగా ఉండాలి. అంటే ఉష్ణగతిక శాస్త్రీయ నిబంధన ప్రకారం చర్య గిబ్స్ శక్తి మార్పు ∆G రుణ విలువ ఉండాలి.
అంటే గిబ్స్ శక్తి తగ్గాలి. ∆G = ∆H – T∆S సమీకరణం ఆధారంగా ∆H కు అత్యధిక రుణ విలువ, -T∆S కు ధన విలువ ఉన్నట్లైతేనే ∆G అధిక రుణ విలువలో ఉండగలుగుతుంది. అధిశోషణ ప్రక్రియ అయత్నీకృత చర్య కాబట్టి పైన పేర్కొన్న రెండు కారణాంశాలు కలిసి ∆G కు రుణ విలువను సమకూరుస్తాయి. అధిశోషణం ప్రక్రియ పురోగమించిన కొద్దీ AH రుణ పరిమాణం తగ్గుతూ పోతుంది. చివరకు ∆H రుణ విలువ T∆S ధన విలువ సమానం అవుతాయి కాబట్టి ∆G విలువ “సున్నా” అవుతుంది. ఈ స్థితి వల్ల సమతాస్థితి ఏర్పడుతుంది.
ప్రశ్న 2.
అధిశోషణం రకాలు ఏమిటి? ఈ భిన్న రకాల అధిశోషణాల అభిలాక్షణిక ధర్మాలలో భేదాలను నాలుగింటిని తెలపండి. [AP & TS. Mar.’15]
జవాబు:
అధిశోషణం రెండు రకాలు.
1) భౌతిక అధిశోషణం (ఫిజి సార్షన్)
2) రసాయన అధిశోషణం (కెమి సార్షన్)
భౌతిక, రసాయన అధిశోషణాలను తులనం చేయడం :
| భౌతిక అధిశోషణం | రసాయన అధిశోషణం |
| 1. వాండర్వాల్ బలాల ద్వారా జరుగుతుంది. | 1. రసాయన బంధం ఏర్పడటం ద్వారా జరుగుతుంది. |
| 2. స్వభావంలో విశిష్టత కనబరచదు. | 2. స్వభావంలో అత్యధిక విశిష్టతను కనబరుస్తుంది. |
| 3. ద్విగత స్వభావం ఉంటుంది. | 3. అద్విగత స్వభావం ఉంటుంది. |
| 4. వాయువు స్వభావంపై ఆధారపడి ఉంటుంది. సులభంగా ద్రవాలుగా మారే వాయువులు సులభంగా అధిశోషణం చెందుతాయి. | 4. ఇది కూడా వాయువు స్వభావంపై ఆధారపడి ఉంటుంది. అధిశోషకంతో రసాయనిక చర్య జరిపే వాయువులు కెమిసారనన్ను ప్రదర్శిస్తాయి. |
| 5. అధిశోషణం ఎంథాల్పీ అల్పం (20 -40kJ మోల్-1). | 5. అధిశోషణం ఎంథాల్పీ అధికం 80–240kJ మోల్-1). |
| 6. అల్ప ఉష్ణోగ్రతలు అధిశోషణం ప్రక్రియను ప్రోత్సహిస్తాయి. ఉష్ణోగ్రత పెరుగుదలతో ఇది తగ్గుతుంది. | 6. అధిశోషణం అధిక ఉష్ణోగ్రతల వద్ద జరుగుతుంది. ఉష్ణోగ్రత పెరిగితే ఇది కూడా పెరుగుతుంది. |
| 7. దీని ఉత్తేజిత శక్తి విలువ నామమాత్రంగా ఉంటుంది. | 7. దీనికి కొన్ని సందర్భాలలో అధిక ఉత్తేజిత శక్తి అవసరమవుతుంది. |
| 8. ఉపరితల వైశాల్యంపై ఆధారపడి ఉంటుంది. ఉపరితల వైశాల్యం పెరిగితే అధిశోషణం పరిమాణం కూడా పెరుగుతుంది. | 8. ఇది కూడా ఉపరితల వైశాల్యంపై ఆధారపడి ఉంటుంది. దీనిలో కూడా ఉపరితల వైశాల్యం పెరిగితే, అధిశోషణం పరిమాణం పెరుగుతుంది. |
| 9. అధిక పీడనాల వద్ద అధిశోషకం ఉపరితలంపై బహు పొరలు ఏర్పడుతాయి. | 9. ఏకపొర మాత్రమే ఏర్పడుతుంది. |
ప్రశ్న 3.
క్రింది పదాలను గురించి నీవు ఏమి తెలుసుకున్నావు?
(ఎ) అధిశోషణం (బి) అభిశోషణం (సి) అధిశోషితం, అధిశోషకం
జవాబు:
(ఎ) అధిశోషణం :
“ఒక పదార్థం వేరొక ద్రవం లేదా ఘన పదార్థం ఉపరితలంపై గాఢత చెందడాన్ని ‘అధిశోషణం’ అంటారు. ఇది ఒక ఉపరితల దృగ్విషయము.
ఉదా :
i) CO2, SO2, Cl2 లాంటి వాయువులను ఉత్తేజిత బొగ్గు అధిశోషించుకుంటుంది.
ii) Pt లేక Ni లోహం, హైడ్రోజన్ వాయువుతో సంపర్కంలో ఉంటే ఆ వాయువును అధిశోషించుకుంటుంది.
(బి) అభిశోషణం :
“ఏదైనా ఒక పదార్థపు అణువులు, ఇతర పదార్థపు ఉపరితలంపై మరియు అంతర్భాగంలో కూడా ఏకరీతిగా వ్యాప్తి చెందడాన్ని ని ‘అబిశోషణం’ అంటారు.
ఇది ఒక ఆయతన దృగ్విషయం.
ఉదా : i) నీటిలో ముంచిన ‘స్పాంజ్’ నీటిని అభిశోషించుకుంటుంది.
ii) రంగు సిరాలో ఉంచిన సుద్దముక్క సిరాను అభిశోషించుకుంటుంది.
(సి) (i) అధిశోషితం :
ఒక పదార్థ ఉపరితలంపై సాంద్రీకృతం అయిన అణువును అధిశోషితం అంటారు.
(ii) అధిశోషకం :
ఏ పదార్థం ఉపరితలంపై అధిశోషణ ప్రక్రియ జరుగునో దానిని అధిశోషకం అంటారు.
ప్రశ్న 4.
ఘనపదార్థాల ఉపరితలాలపై వాయువుల అధిశోషణం సాధారణంగా ఎంట్రోపి తగ్గుదలతో జరుగుతుంది. అయితే అది అయత్నీకృత చర్యగానే ఉంటుంది. వివరించండి.
జవాబు:
అధిశోషణానికి సంబంధించిన వేరొక ముఖ్య అంశం అధిశోషణోష్ణం. అధిశోషణం ప్రక్రియలో అధిశోషకం ఉపరితలంపై ఉండే అవశేష బలాల సంఖ్య తగ్గుతుంది. అంటే ఉపరితల శక్తి తగ్గుతుంది. ఇలా తగ్గిన శక్తి ఉష్ణరూపంలో వెలువడుతుంది. కాబట్టి అధిశోషణ ప్రక్రియ ప్రధానంగా ఉష్ణమోచక చర్యగానే ఉంటుంది. అంటే అధిశోషణం ∆H విలువ రుణ విలువలో ఉంటుంది. అధిశోషణం ప్రక్రియ ఎంథాల్పీ తగ్గుదలను, ఎంట్రోపీ తగ్గుదలను కూడా ప్రదర్శించే చర్యగానే ఉంటుంది. నిర్దేశిత ఉష్ణోగ్రత, పీడనాల వద్ద ఒక చర్య అయత్నీకృతంగా ఉండాలి.
అంటే ఉష్ణగతిక శాస్త్రీయ నిబంధన ప్రకారం చర్య గిబ్స్ శక్తి మార్పు ∆G రుణ విలువ ఉండాలి. అంటే గిబ్స్ శక్తి తగ్గాలి. ∆G = ∆H – T∆S సమీకరణం ఆధారంగా ∆H కు అత్యధిక రుణ విలువ, -T∆S కు ధన విలువ ఉన్నట్లైతేనే ∆G అధిక రుణ విలువలో ఉండగలుగుతుంది. అధిశోషణ ప్రక్రియ అయత్నీకృత చర్య కాబట్టి పైన పేర్కొన్న రెండు కారణాంశాలు కలిసి ∆G కు రుణ విలువను సమకూరుస్తాయి. అధిశోషణం ప్రక్రియ పురోగమించిన కొద్దీ ∆H రుణ పరిమాణం తగ్గుతూ పోతుంది. చివరకు ∆H రుణ విలువ T∆S ధన విలువ సమానం అవుతాయి కాబట్టి ∆G విలువ “సున్నా” అవుతుంది. ఈ స్థితి వల్ల సమతాస్థితి ఏర్పడుతుంది.
![]()
ప్రశ్న 5.
ఫ్రాయిండ్లిష్ సమోష్ణరేఖ సమీకరణంలో k, n ల విలువలను ఎలా లెక్కిస్తారు?
జవాబు:
ప్రశ్న 6.
క్రింది వాటిపై అధిశోషణం పరిమాణం ఏ విధంగా ఆధారపడి ఉంది?
(ఎ) ఏకాంక ద్రవ్యరాశి గల అధిశోషకం ఉపరితల వైశాల్యం పెరుగుదల
(బి) వ్యవస్థ ఉష్ణోగ్రత పెరుగుదల
(సి) వాయువు పీడనం పెరుగుదల
జవాబు:
(ఎ) ఏకాంక ద్రవ్యరాశి గల అధిశోషకం ఉపరితల వైశాల్యం పెరుగుదల వలన అధిశోషణం పరిమాణం పెరుగును.
(బి) వ్యవస్థ ఉష్ణోగ్రత పెరుగుదల వలన అధిశోషణం పరిమాణం తగ్గును.
(సి) వాయువు పీడనం పెరుగుదల వలన అధిశోషణం పరిమాణం పెరుగును.
ప్రశ్న 7.
ఉత్ప్రేరణం అంటే ఏమిటి? ఉత్ప్రేరణాన్ని ఎలా వర్గీకరిస్తాం? ప్రతీ రకానికి ఒక ఉదాహరణ ఇవ్వండి. [AP. Mar.’16]
జవాబు:
ఉత్ప్రేరకం మరియు ఉత్ప్రేరణం :
రసాయన చర్యలో తాను వినియోగం చెందకుండా చర్యా వేగాన్ని పెంచే చర్యకు కలిపిన ఇతర పదార్థమే ఉత్ప్రేరకం (catalyst).
చర్యా మిశ్రమానికి బాహ్య పదార్థాన్ని కలిపి, చర్యా వేగాన్ని పెంచే ప్రక్రియను ఉత్ప్రేరణ (catalysis) అంటారు.
ఉత్ప్రేరణ వర్గీకరణ :
ఉత్ప్రేరకం మరియు క్రియాజనకాల భౌతిక స్థితుల (ప్రావస్థల) ఆధారంగా ఉత్ప్రేరణాన్ని రెండు రకాలుగా వర్గీకరించారు. అవి :
ఎ) సజాతి ఉత్ప్రేరణ :
ఒక ఉత్ప్రేరక రసాయన చర్యలో ఉత్ప్రేరకం మరియు క్రియాజనకాలు ఒకే భౌతిక ప్రావస్థలో ఉంటే దాన్ని సజాతి ఉత్ప్రేరణ అంటారు.
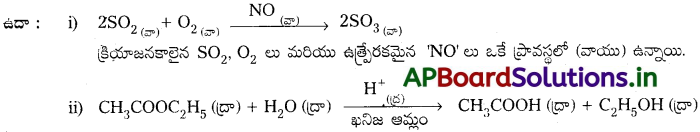
క్రియాజనకాలైన ఎస్టర్, H2O లు మరియు ఉత్ప్రేరకమైన ఆమ్లము ఒకే ప్రావస్థలో (ద్రవం) ఉన్నాయి.
బి) విజాతి ఉత్ప్రేరణ :
ఒక ఉత్ప్రేరక రసాయన చర్యలో ఉత్ప్రేరకం మరియు క్రియాజనకాలు భిన్న భౌతిక ప్రావస్థలలో ఉంటే దాన్ని విజాతి ఉత్ప్రేరణ అంటారు.
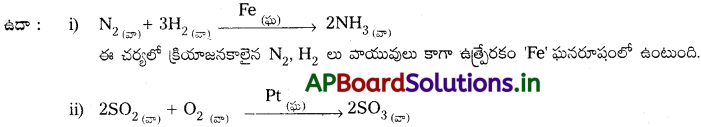
ఈ చర్యలో క్రియాజనకాలైన SO2, O2 లు వాయువులు కాగా ఉత్ప్రేరకం ‘Pt’ ఘన రూపంలో ఉంటుంది.
ప్రశ్న 8.
విజాతి ఉత్ప్రేరణానికి సంబంధించిన అధిశోషణ సిద్ధాంతం చర్యా విధానాన్ని చర్చించండి.
జవాబు:
అధిశోషణ సిద్ధాంతం విజాతి ఉత్ప్రేరణ చర్య విధానం వివరించినది.
చర్యా విధానం :
(i) ఉత్ప్రేరకం ఉపరితలం వద్దకు క్రియాజనకాల వ్యాపనం.
(ii) ఉత్ప్రేరకం ఉపరితలంపై క్రియాజనకాలు అధిశోషణం చెందడం.
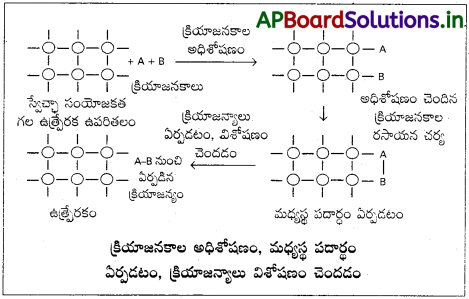
(iii) మధ్యస్థ పదార్థం ఏర్పడటం ద్వారా ఉత్ప్రేరకం ఉపరితలంపై రసాయన చర్య జరగడం.
(iv) ఉత్ప్రేరకం ఉపరితలం నుండి క్రియాజన్యాలు విశోషణం చెందడం ఫలితంగా తిరిగి మరికొంతమేర రసాయన చర్య జరగడానికి శుద్ధ ఉపరితలాన్ని సమకూర్చడం.
(v) ఉత్ప్రేరకం ఉపరితలం నుండి చర్యా క్రియాజన్యాలు వ్యాపనం చెందటం.
ప్రశ్న 9.
జియోలైట్లు జరిపే ఉత్ప్రేరణానికి సంబంధించిన కొన్ని లక్షణాలను చర్చించండి.
జవాబు:
జియోలైట్లు ప్రదర్శించే ఆకార ఆధారిత వరణాత్మకత :
ఉత్ప్రేరకంపై చోటు చేసుకొని ఉండే రంధ్రాల పరిమాణం ఆధారం గాను, క్రియాజనకాల క్రియాజన్యాల అణువుల సాపేక్ష పరిమాణాల ఆధారంగాను జరిగే ఉత్ప్రేరక చర్యను ఆకార ఆధారిత వరణాత్మక ఉత్ప్రేరణం అంటారు. జియోలైట్లకు తేనెపట్టు ఆకారంలోగల నిర్మాణం ఉండటం కారణంగా అవి ఆకార ఆధారిత వరణాత్మక ఉత్ప్రేరకాలుగా పని చేస్తాయి. సూక్ష్మరంధ్రాలు గల సచ్ఛిద్ర అల్యూమినోసిలికేట్లు జియోలైట్లు. ఇవి కొన్ని సిలికాన్ పరమాణువులు, అల్యూమినియమ్ పరమాణువులతో ప్రతిక్షేపితమై Al-O-Si త్రిమితీయ యూనిట్లు గల నిర్మాణంలో గల సిలికేట్లు. జియోలైట్లపై జరిగే చర్యలు క్రియాజనక, క్రియాజన్య అణువుల సైజు, ఆకారాల పైనా, జియోలైట్లలోని ఛిద్రాలు, డొల్లల ఆకారాల పైన ఆధారపడి ఉంటాయి. జియోలైట్లు ప్రకృతిలో లభ్యం అవుతాయి. కొన్నింటిని ఉత్ప్రేరక వరణాత్మకతను పొందే విధంగా సంశ్లేషిస్తున్నారు.
హైడ్రోకార్బన్ల విభంజనాన్ని, సదృశకరణాన్ని సాధించడానికి పెట్రోరసాయన పరిశ్రమలలో జియోలైట్లను విరివిగా ఉత్ప్రేరకాలుగా ఉపయోగిస్తున్నారు. పెట్రోలియమ్ పరిశ్రమలో ఉపయోగించే ఒక ముఖ్యమైన జియోలైట్ ఉత్ప్రేరకం ZSM – 5. ఇది ఆల్కహాల్లను అనార్థీకరణ చర్యకు గురిచేసి గాసోలిన్లుగా (పెట్రోల్) పిలిచే హైడ్రోకార్బన్ల మిశ్రమంగా మారుస్తుంది.
![]()
ప్రశ్న 10.
సరైన పటం సహాయంతో ఎంజైమ్ ఉత్ప్రేరణ చర్యా విధానాన్ని క్లుప్తంగా వివరించండి.
జవాబు:
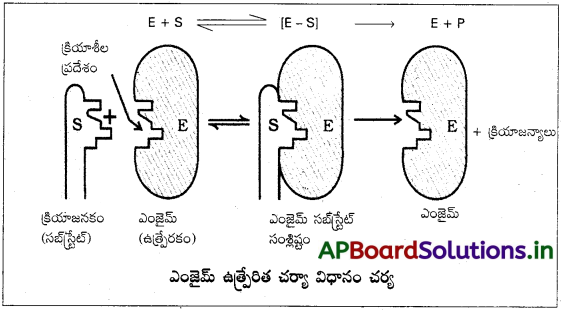
ఎంజైమ్ ఉత్ప్రేరిత చర్యా విధానం చర్య
ఎంజైమ్ ఉత్ప్రేరిత చర్యలు రెండు అంచెలలో జరుగును.
అంచె – 1 : ఎంజైమ్లో క్రియాజనకం బంధితమై ఉత్తేజిత సంక్లిష్టం (ES*) ఏర్పడుతుంది.
E + S → ES*
అంచె – 2 : ఈ ఉత్తేజిత సంక్లిష్టం క్రియాజన్యాలుగా వియోగం చెందుట.
ES* → E + P
ప్రశ్న 11.
ఎంజైమ్ల ఉత్ప్రేరణ క్రియాశీలతను ప్రభావితం చేసే అంశాలను చర్చించండి.
జవాబు:
ఎంజైమ్ల ఉత్ప్రేరణ క్రియాశీలతను ప్రభావితం చేసే అంశాలు :
అధిక చర్యాశీలత లేదా సామర్థ్యం, అధిక వరణాత్మక ధర్మం ఉండటం అనేది ఎంజైమ్ ఉత్ప్రేరణం ప్రత్యేకత. ఎంజైమ్ ఉత్ప్రేరకాలు కింది అభిలాక్షణిక ధర్మాలను ప్రదర్శిస్తాయి.
(i) అత్యధిక ఉత్ప్రేరణ సామర్థ్యం :
ఒక ఎంజైమ్ అణువు సుమారు ఒక మిలియన్ క్రియాజనక అణువులను ఒక నిమిషంలో పరివర్తన చర్యలకు గురిచేస్తుంది.
(ii) అత్యధిక వరణాత్మక గుణం :
ప్రతీ చర్యకు ఒక ప్రత్యేక ఎంజైమ్ ఉంటుంది. అంటే ఒక ఉత్ప్రేరకం, ఒక రకం, చర్యనే ఉత్ప్రేరణం చేస్తుంది. ఉదాహరణకు యూరియేజ్ ఎంజైమ్ యూరియా జలవిశ్లేషణ చర్యను మాత్రమే ఉత్ప్రేరణం చేస్తుంది. ఏ ఇతర ఎమైడ్ జలవిశ్లేషణ చర్యను ఉత్ప్రేరణం చెయ్యదు.
(iii) యుక్తతమ (optimum) ఉష్ణోగ్రత వద్ద మాత్రమే అధిక చర్యాశీలతను ప్రదర్శించడం :
యుక్తతమ ఉష్ణోగ్రత అనే ప్రత్యేక ఉష్ణోగ్రత వద్ద ఎంజైమ్ చర్యరేటు గరిష్ఠంగా ఉంటుంది. ఈ యుక్తతమ ఉష్ణోగ్రతకు రెండువైపులా గల ఉష్ణోగ్రతల వద్ద ఎంజైమ్ క్రియాశీలత తగ్గుతుంది. ఎంజైమ్ క్రియాశీలతకు అనువైన ఉష్ణోగ్రత వ్యాప్తి 298 – 310 Kగా ఉంటుంది. మానవ శరీర ఉష్ణోగ్రత 310 K ఎంజైమ్ ఉత్ప్రేరణ చర్యలకు అనువుగా ఉంటుంది.
(iv) యుక్తతమ pH వద్ద అత్యధిక చర్యాశీలతను ప్రదర్శించడం :
యుక్తతమ pH అనే ఒక ప్రత్యేక pH విలువ వద్ద మాత్రమే ఎంజైమ్ ఉత్ప్రేరక చర్యరేటు గరిష్ఠంగా ఉంటుంది. ఇది 5 – 7 pH ల మధ్య ఉంటుంది.
(v) ఉత్తేజకాలు, కో-ఎంజైమ్ల సమక్షంలో క్రియాశీలత పెరుగుదల :
కో-ఎంజైమ్లు అనే కొన్ని ఇతర పదార్థాల సమక్షంలో ఎంజైమ్ క్రియాశీలత పెరుగుతుంది. ఒక ఎంజైమ్తో సహా కొద్ది పరిమాణంలో ప్రోటీన్ కాని వేరొక పదార్థం (విటమిన్) కూడా ఉన్నట్లైతే, ఎంజైమ్ క్రియాశీలత గణనీయంగా పెరుగుతుంది.
Na+, Mn2+, Co2+, Cu2+ లాంటి లోహ అయాన్లు సాధారణంగా ఉత్తేజకాలుగా ఉంటాయి. ఈ లోహ అయాన్లు, ఎంజైమ్ అణువులతో బలహీనంగా బంధితమై, ఎంజైమ్ల క్రియాశీలతను పెంచుతాయి. సోడియమ్ క్లోరైడ్ అంటే Nat అయాన్ల ‘సమక్షంలో ఎమైలేజ్ క్రియాశీలత పెరుగుతుంది.
(vi) నిరోధకాలు, విషపదార్థాల ప్రభావం :
సాధారణ ఉత్ప్రేరకాల మాదిరిగానే ఇతర పదార్థాల సమక్షంలో ఎంజైమ్లు కూడా నిరోధకాలు లేదా విషపదార్థాలుగా పనిచేస్తాయి. ఎంజైమ్ ఉపరితలంపై చోటుచేసుకొని ఉండే క్రియాశీలత గల గ్రూపుతో ఈ నిరోధకాలు లేదా విషపదార్థాలు చర్యలో పాల్గొని ఎంజైమ్ల ఉత్ప్రేరణ క్రియాశీలతను తగ్గించడం లేదా పూర్తిగా నాశనం చేయడం చేస్తాయి. మన శరీరంలో చాలా ఔషధాలు ఎంజైమ్ నిరోధకాలుగా పనిచేసి వ్యాధిని నయం చేస్తాయి.
ప్రశ్న 12.
ఎంజైమ్ల ఉత్ప్రేరణ చర్యలు ఆరింటిని తెలపండి.
జవాబు:
చక్కెర విలోమ చర్య :
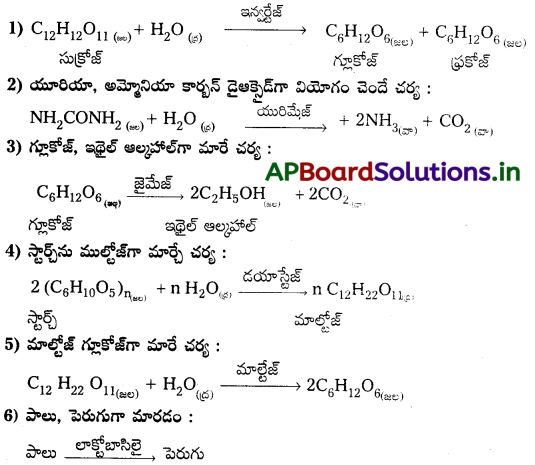
ప్రశ్న 13.
ఉత్ప్రేరకాల క్రియాశీలత, వరణాత్మకత అంటే ఏమిటి?
జవాబు:
క్రియాశీలత :
- ఉత్ప్రేరకం ఒక చర్యరేటు పెంచే సామర్థ్యం తెలిపేదే క్రియాశీలత.
- ఉత్ప్రేరకం క్రియాశీలత రసాయన అధిశోషణ బలంపై ఆధారపడును.
- ఉత్ప్రేరకం ఉపరితలంపై క్రియాజనకాలు బలంగా అధిశోషణం చెందినట్లైతేనే అవి క్రియాశీలతను ప్రదర్శిస్తాయి.
- ఆవర్తన పట్టికలో 5-11 గ్రూపు వరకు హైడ్రోజనీకరణ చర్యలో లోహాలకు ఉత్ప్రేరకం క్రియాశీలత క్రమంగా పెరుగుతుంది. 7-9 గ్రూపులకు ఈ క్రియాశీలత గరిష్టంగా ఉంటుంది.
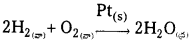
వరణాత్మకత :
ఒక రసాయన చర్యలో పాల్గొనే క్రియాజనకాలు ఆశించిన భిన్న క్రియాజన్యాలను ఏర్పరచే విధంగా చర్యను దిశాత్మకంగా చేయుటను వరణాత్మకత అంటారు.
ఈ క్రింది చర్యల ద్వారా విజాతి ఉత్ప్రేరణ వరణాత్మకత గురించి తెలుస్తుంది.
H2 మరియు CO లలో మొదలయి విభిన్న ఉత్ప్రేరకాల సమక్షంలో విభిన్న ఉత్పన్నాము ఏర్పడతాయి.
ఉత్ప్రేరక ప్రభావం సహజంగా వరణాత్మకమైనది.
![]()
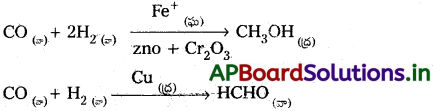
ఉత్ప్రేరక ప్రభావం సహజంగా వరణాత్మకమైనది.
దీనినిబట్టి ఒక ఉత్ప్రేరకం చర్య బలమైన వరణాత్మక స్వభావాన్ని ప్రదర్శిస్తుంది అని తెలుస్తుంది.
ప్రశ్న 14.
అనుఘకాల భౌతిక స్థితుల ఆధారంగా కొల్లాయిడ్లను ఎలా వర్గీకరిస్తారు?
జవాబు:
అనుఘటనాల భౌతిక స్థితుల ఆధారంగా కొల్లాయిడ్లను ఈ క్రింది విధంగా వర్గీకరించారు.
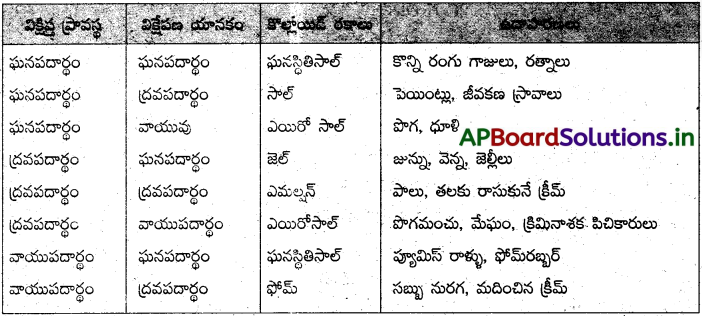
ప్రశ్న 15.
విక్షేపణ యానకం పరంగా కొల్లాయిడ్లను ఎలా వర్గీకరిస్తారు?
జవాబు:
విక్షేపణ యానకం ఆధారంగా కొల్లాయిడ్లను ఈ క్రింది విధంగా వర్గీకరించారు.
- విక్షేపణ యానకం గాలి (వాయువు) అయితే వాటిని ‘ఏరోసాల్లు అంటారు. ఉదా : పొగ.
- విక్షేపణ యానకం నీరు అయితే వాటిని హైడ్రోసాల్లు అంటారు. ఉదా : స్టార్చ్
- విక్షేపణ యానకం ఆల్కహాల్ అయితే వాటిని ఆల్కసాల్లు అంటారు.
![]()
ప్రశ్న 16.
విక్షిప్త ప్రావస్థ, విక్షేపణ యానకం వీటి మధ్య గల అన్యోన్య చర్యల ఆధారంగా కొల్లాయిడ్లను ఎలా వర్గీకరిస్తారు?
జవాబు:
విక్షిప్త ప్రావస్థ(ద్రావితం) కణ పరిమాణం 1mµ – lµ వరకు ఉండే ద్విగుణాత్మక విజాతి వ్యవస్థను కొల్లాయిడ్లు అంటారు.
కొల్లాయిడ్ల వర్గీకరణ :
విక్షిప్త ప్రావస్థ మరియు విక్షేపక యానకం మధ్యగల సంబంధం ఆధారంగా వర్గీకరణ జరిగింది.
ఎ) లయోఫిలిక్ కొల్లాయిడ్లు (ద్రవ ప్రియ కొల్లాయిడ్లు) :
వీటిలో విక్షేపక యానకంకూ,, విక్షిప్త ప్రావస్థకీ మధ్య ఎక్కువ ఆపేక్ష ఉంటుంది.
ఉదా : స్టార్చ్ కొల్లాయిడ్ ద్రావణం లయోఫిలిక్.
బి) లయోఫోబిక్ కొల్లాయిడ్లు (ద్రవ విరోధి కొల్లాయిడ్లు) :
వీటిలో విక్షిప్త ప్రావస్థకూ, విక్షేపక యానకానికీ మధ్య ఆపేక్ష ఉండదు.
ఉదా : గోల్డ్ కొల్లాయిడ్ ద్రావణం లయోఫోబిక్..
ప్రశ్న 17.
కొల్లాయిడ్సాల్, జెల్, ఎమల్షన్, ఫోమ్ వీటి మధ్య గల భేదాలను తెలపండి.
జవాబు:
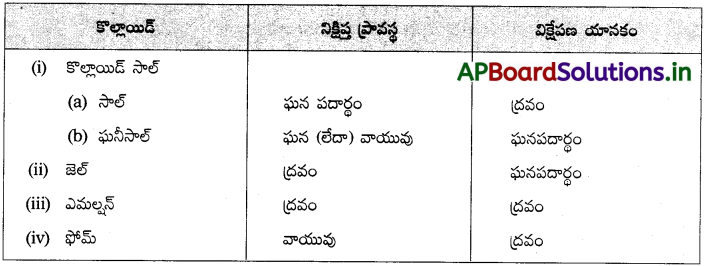
ప్రశ్న 18.
లయోఫిలిక్, లయోఫోబిక్ సాల్లు అంటే ఏమిటి? స్థిరత్వం, ఉత్రమణీయత ఆధారంగా పై రెండు పదాలను పోల్చండి.
జవాబు:
విక్షిప్త ప్రావస్థ(ద్రావితం) కణ పరిమాణం 1mµ – 1µ వరకు ఉండే ద్విగుణాత్మక విజాతి వ్యవస్థను కొల్లాయిడ్లు అంటారు.
కొల్లాయిడ్ల వర్గీకరణ :
విక్షిప్త ప్రావస్థ మరియు విక్షేపక యానకం మధ్యగల సంబంధం ఆధారంగా వర్గీకరణ జరిగింది.
ఎ) లయోఫిలిక్ కొల్లాయిడ్లు (ద్రవ ప్రియ కొల్లాయిడ్లు) :
వీటిలో విక్షేపక యానకంకూ, విక్షిప్త ప్రావస్థకీ మధ్య ఎక్కువ ఆపేక్ష ఉంటుంది.
ఉదా : స్టార్చ్ కొల్లాయిడ్ ద్రావణం లయోఫిలిక్.
బి) లయోఫోబిక్ కొల్లాయిడ్లు (ద్రవ విరోధి కొల్లాయిడ్లు) :
వీటిలో విక్షిప్త ప్రావస్థకూ, విక్షేపక యానకానికీ మధ్య ఆపేక్ష ఉండదు.
ఉదా : గోల్డ్ కొల్లాయిడ్ ద్రావణం లయోఫోబిక్.
- అయోఫిలిక్ సాల్లు ఉత్రమణీయమైనవి. ఇవి స్కందనం జరుగవు. స్థిరంగా ఉంటాయి.
- లయోఫోబిక్ సాల్లు అనుత్రమణీయమైనవి. వీటికి విద్యుద్విశ్లేష్యాలను కలిపినపుడు అస్థిరంగామారి స్కంధనం జరుగుతాయి. వీటిని స్థిరంగా మర్చుటకు లయోఫిలిక్ కొల్లాయిడ్లను కలుపవలెను.
ప్రశ్న 19.
లయోఫిలిక్, లయోఫోబిక్ భాగాలు గల అణువులు ఉన్న పదార్థం పేరు వ్రాయండి. దైనందిన జీవితంలో దాని ఉపయోగమేమిటి?
జవాబు:
- సముచ్ఛయం చెందిన కొల్లాయిడ్లు (లేదా) మిసెల్లు లయోఫిలిక్, లయోఫోబిక్ భాగాలు కలవి.
- సబ్బులు, సంశ్లేషక డిటర్జెంట్లు ఉదాహరణలు.
- సబ్బులు మురికిని తొలగించే ప్రక్రియలో సబ్బు అణువులు మిసెల్ను మురికి బిందువు వద్ద ఏర్పరుస్తారు.
ప్రశ్న 20.
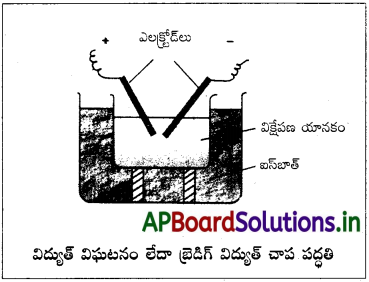
పటం సహాయంతో కొల్లాయిడ్లను తయారుచేసే బ్రెడిగ్ విద్యుత్ చాప పద్ధతిని వర్ణించండి.
జవాబు:
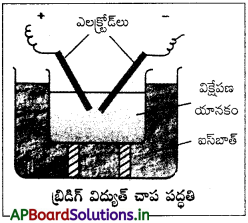
బ్రెడిగ్ విద్యుత్చాప పద్ధతి :
ఈ పద్ధతిలో విక్షేపణం (dispersion), సాంద్రీకరణం (condensation) రెండు ప్రక్రియలు ఇమిడి ఉన్నాయి. గోల్డ్, సిల్వర్, ప్లాటినమ్ మొదలైన లోహ కొల్లాయిడ్ సాల్లలను ఈ పద్ధతిలో తయారుచేస్తారు. ఈ పద్ధతిలో విక్షేపణ యానకంలో ముంచి ఉంచిన లోహ ఎలక్ట్రోడ్ల మధ్య విద్యుత్ చాపాన్ని అనువర్తిస్తారు. ఈ పద్ధతిలో అత్యధిక పరిమాణంలో వెలువడిన ఉష్ణం లోహబాష్పాలను ఏర్పరుస్తుంది. ఈ బాష్పాలు సాంద్రీకరణం చెంది కొల్లాయిడ్ల పరిమాణంలో కణాలను ఏర్పరుస్తాయి.
ప్రశ్న 21.
రసాయన పద్ధతులలో కొల్లాయిడ్లను తయారు చేసే నాలుగు పద్ధతులను రసాయన సమీకరణాలతో సహా తెలపండి.
జవాబు:
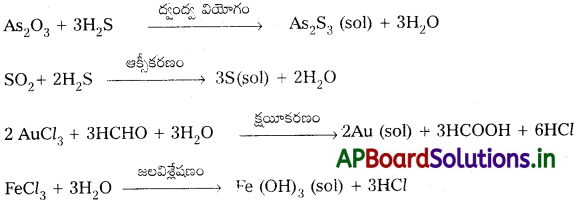
రసాయన పద్ధతులు :
క్రియాజన్య జాతులను ఏర్పరచే ద్వంద్వ వియోగం, ఆక్సీకరణం, క్షయకరణం, జలవిశ్లేషణం మొదలైన రసాయన చర్యల ఆధారంగా కొల్లాయిడ్లను తయారుచేస్తారు. క్రియాజన్య జాతులు సముచ్ఛయం చెంది, సాల్లను ఏర్పరుస్తాయి.
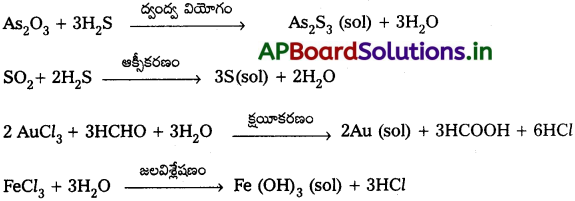
ప్రశ్న 22.
కొల్లాయిడ్ల శుద్ధి ప్రక్రియను పటం సహాయంతో డయాలిసిస్ దృగ్విషయం లేదా ఘటన ద్వారా వివరించండి.
జవాబు:
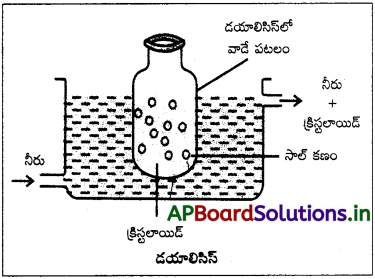
డయాలిసిస్ :
ఇది అనువైన పటలం లేదా పొరను ఉపయోగించి కరిగే (ద్రావణీయ) స్థితిలో ఉండే పదార్థాలను కొల్లాయిడ్ ద్రావణం నుంచి తొలగించే ప్రక్రియ. నిజ ద్రావణంలో ఉండే అయాన్లు, లఘు అణువులు జంతుపటలం (బ్లాడర్) లేదా పార్చిమెంట్ కాగితం లేదా సెల్లోఫేస్ రేకు ద్వారా పోగల్గుతాయి. కాని కొల్లాయిడ్ కణాలు వీటిగుండా పోలేవు కాబట్టి ఈ పొరలను ఉపయోగించి డయాలిసిస్ అంటారు. కొల్లాయిడ్ ద్రావణంతో నింపిన అనువైన పటలంతో పాత్రలో ముంచి ఉంచుతారు. అణువులు అయాన్లు పటలం ద్వారా వ్యాపనం చెంది పాత్రలోని నీటిలోకి పోతాయి. సంచిలో శుద్ధ కొల్లాయిడ్ ద్రావణం మిగిలిఉంటుంది.
ప్రశ్న 23.
రేఖాపటం సహాయంతో మిసెల్ ఏర్పడటాన్ని వివరించండి.
జవాబు:
మిసెల్ ఏర్పడే విధానం :
సబ్బు ద్రావణాన్ని ఉదాహరణగా తీసుకొందాం. భార కొవ్వు ఆమ్లాల సోడియమ్ లేదా పొటాషియమ్ లవణాన్ని సబ్బు అంటాం. దీనిని RCOO–Na+ (సోడియమ్ స్టియరేట్ CH3(CH2)16COO–Na+ అంటారు. ఇది చాలా బార్ సబ్బులలో ప్రధాన అనుఘటకంగా ఉంది). దీనిని నీటిలో కరిగిస్తే ఇది RCOO– గాను, Na+ గాను వియోజనం చెందుతుంది. RCOO– అయాన్ రెండు భాగాలు ఉన్నాయి. ఇవి పొడవైన హైడ్రోకార్బన్ గొలుసు R (దీనిని అధ్రువ భాగం లేదా ‘తోక’ అంటారు). ఇది హైడ్రోఫోబిక్ (నీటిని వికర్షించే భాగం), COO– ధ్రువ భాగం (ధ్రువ అయానిక లేదా ‘తల’ భాగం) ఇది హైడ్రోఫిలిక్ (నీటిని ఆకర్షించే భాగం).
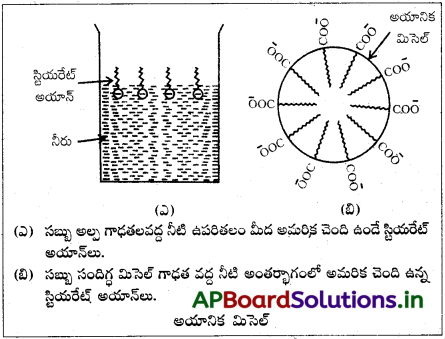
ఉపరితలంపై ఉండే RCOO– అయాన్లు COO– గ్రూపులు నీటిలోను హైడ్రోకార్బన్ గొలుసు (R) నీటికి దూరంగా ఉపరితలం వద్ద ఉంటాయి. అయితే సందిగ్ధ మిసెల్ గాఢత (CMC) వద్ద COOT అయాన్లు, ద్రావణం లోపలికి లాగబడతాయి. ఈ పరిస్థితులలో అవి సముచ్ఛయం చెంది గోళాకారంలోకి మారతాయి. హైడ్రోకార్బన్ గొలుసులు గోళం కేంద్రకం వైపుగా చొచ్చుకొని ఉంటాయి. COO– గ్రూపులు గోళం ఉపరితలంపై ఊర్ధ్వభాగం వైపుగా చోటుచేసుకొని ఉంటాయి. ఈ విధంగా ఏర్పడిన సముచ్ఛయాన్ని అయానిక్ మిసైల్ అంటారు. ఈ అణుపులలో సుమారు 100 సాధారణ అణువులు ఉంటాయి. ఇదే విధంగా సోడియమ్ లారిల్ సల్ఫేట్ CH3(CH2)11SO–4Na+ వంటి డిటర్జెంట్లలో -SO–4 పోలార్ గ్రూపుగా పొడవైన హైడ్రోకార్బన్ గొలుసుతో కూడా ఉంటుంది. కాబట్టి వీటి విషయంలో కూడా మిసెల్ ఏర్పాటు విధానం సబ్బులలో మాదిరి గానే ఉంటుంది.
![]()
ప్రశ్న 24.
ఎమల్సిఫికేషన్, మిసెల్ ఏర్పాటు వీటి ద్వారా సబ్బు జరిపే శుద్ధి ప్రక్రియ ఉంది. దీనిని గురించి తెలపండి.
జవాబు:
మురికి గుడ్డలపై ఉండే గ్రీజు, మురికి మొదలైన పదార్థాలు నీటిలో కరిగి మిసెల్ను ఏర్పరచటం అనే అంశం మీద ఈ శుభ్రపరిచే ప్రక్రియ ఆధారపడి ఉంటుంది. ఈ ప్రక్రియను గ్రీజు ఎమల్సిఫికేషన్ చర్య అంటారు. పొడుగాటి గొలుసులున్న. ఉన్నత ఫాటీ ఆమ్లం సోడియం లవణాలను సబ్బు అంటారు. సబ్బులోని ఆనయాన్లకూ, నీటికీ మధ్య ఉన్న బంధక బలం ఆధారంగానే ఈ శుభ్రపరచే ప్రక్రియ ఆధారపడి ఉంటుంది.
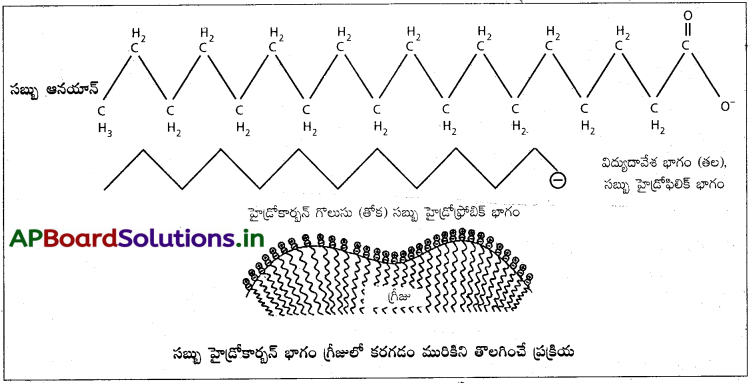
సబ్బు హైడ్రోకార్బన్ భాగం గ్రీజులో కరగడం మురికిని తొలగించే ప్రక్రియ సబ్బు ఆనయాన్లు సులభంగా మిసెల్లను ఏర్పరుస్తాయి. హైడ్రోకార్బన్ భాగాలు మిసెల్ అంతర్భాగంలోనికి చొచ్చుకుని పోతాయి. -COO– అయాన్లు మిసెల్ ఉపరీతలంపై చోటు చేసుకుంటాయి. ద్రవ హైడ్రో కార్బన్ గా ప్రవర్తించే గ్రీజు లేదా మురికి మిసెల్లోకి పోతుంది. సబ్బు ఆనయాన్ తోక భాగాలు గ్రీజులోకి చొచ్చుకుని ఉంటాయి. ధ్రువ సమూహాలు గ్రీజు ఉపరితలం నుంచి ‘వెలుపలికి చొచ్చుకునిపోయి మిసెల్ చుట్టు ఒక ధ్రువ స్వభావం ఉన్న పొరను ఏర్పరుస్తాయి. ‘ఎమల్సిఫికేషన్. చెందిన గ్రీజు మరకలను సబ్బు ద్రావణంతో తొలగించడం అవుతుంది.
ప్రశ్న 25.
బ్రౌనియన్ చలనం ఘటనను వివరించి, ఈ ఘటనానికి గల కారణాలను తెలపండి.
జవాబు:
బ్రౌనియన్ చలనం :
“కొల్లాయిడ్ కణాలు, విక్షేపణ యానకంలో నిరంతరం వేగంగా మరియు అస్తవ్యస్తంగా చలించడాన్ని “బ్రౌనియన్ చలనం” అంటారు. ఇది ఒక గతిజ ధర్మము.
ఈ దృగ్విషయాన్ని “జిగ్మండీ” అను శాస్త్రవేత్త కనుగొన్నాడు.
కారణము :
విక్షేపణ యానక అణువులకు, కొల్లాయిడ్ కణాలకు మధ్య తుల్యము కాని అభిఘాతాల కారణంగా బ్రౌనియన్ చలనం ఉంటుంది.
ప్రశ్న 26.
నాలుగు ధనావేశ కొల్లాయిడ్లను పేర్కొనండి.
జవాబు:
ధనావేశం గల కొల్లాయిడ్లు ఈ క్రింద ఇవ్వబడ్డాయి.
- హైడ్రేటెడ్ లోహ ఆక్సైడ్ సాల్లు. ఉదా : Al2O3.XH2O, CrO3.XH2O etc.
- క్షార అద్దకాలు. ఉదా : మిథిలీన్ బ్లూసాల్
- హిమోగ్లోబిన్ (రక్తం)
- ఆక్సైడ్లు. ఉదా : TiO2 సాల్
ప్రశ్న 27.
నాలుగు ఋణావేశ కొల్లాయిడ్లను పేర్కొనండి.
జవాబు:
ఋణావేశం గల కొల్లాయిడ్ లు ఈ క్రింద ఇవ్వబడ్డాయి.
- లోహసాల్లు. ఉదా : AU – సాల్.
- ఆమ్ల అద్దకాలు. ఉదా : ఇమోసిన్ సాల్.
- లోహ సల్ఫైడ్లు సాల్లు. ఉదా : ArS3, CdS సాల్లు.
- స్టార్చ్, గమ్ (జిగురులు) సాల్లు.
ప్రశ్న 28.
హెల్మ్ హోల్డ్జ్. పటల ద్వయం, జీటా పొటెన్షియల్ పదాలను వివరించండి. కొల్లాయిడ్ ద్రావణాలలో వీటి ప్రాముఖ్యం ఏమిటి?
జవాబు:
హెల్మ్ హోల్టేజ్ పటల ద్వయం :
కొల్లాయిడ్ కణం చుట్టూ విరుద్ధ ఆవేశాలు గల రెండు పటలాల సంయుగ్మాన్ని హెల్మ్ హోల్టేజ్ పటల ద్వయం అంటారు.
జీటా పొటెన్షియల్ :
విరుద్ధ ఆవేశాలు గల స్థిర పటలం, విసరిత పటలం మధ్యగల పొటెన్షియల్ బేధాన్ని విద్యుత్ గతిక ప్రొటెన్షియల్ (లేదా) జీటా పొటెన్షియల్ అంటారు. ఇది ధన లేదా ఋణ విలువలో ఉంటుంది.
పై దృగ్విషయముల నుండి కొల్లాయిడ్లలో ఘనరూప కణాలు ఒక రకమైన ఆవేశాన్ని కలిగిఉంటే ద్రవ యానకంలోని కణాలు వ్యతిరేక ఆవేశం కలిగిఉంటాయి అని తెలుస్తుంది.
ప్రశ్న 29.
ఎలక్ట్రోఫోరిసిస్ ఘటనను పటం సహాయంతో వివరించండి.
జవాబు:
ఎలక్ట్రోఫోరిసిస్ (లేదా) విద్యుదావేశిత కణ చలనం :
కొల్లాయిడ్ కణానికి విద్యుదావేశం ఉంది అనే వాస్తవాన్ని విద్యుదావేశిత కణచలనం ప్రయోగం నిర్ధారించింది. కొల్లాయిడ్ ద్రావణంలో రెండు ప్లాటినం ఎలక్ట్రోడ్లు ముంచి ఉంచి వాటి మధ్య విద్యుత్ పొటెన్షియల్ను ఆవర్తనం చేసినట్లైతే కొల్లాయిడ్ కణాలు రెండు ఎలక్ట్రోడ్లలో ఏదోఒక దానివైపుగా ప్రయాణిస్తాయి
అనువర్తిత emf ప్రభావంతో కొల్లాయిడ్ కణం చలనం చెందే ప్రక్రియను విద్యుదావేశితకణ చలనం (లేదా) ఎలక్ట్రోఫోరసిస్ అంటారు.
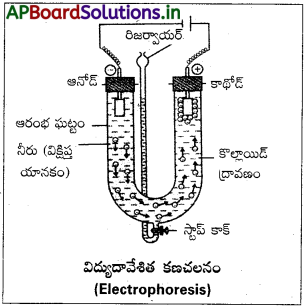
ధనావేశిత కణాలు కాథోడ్వైపు ఋణావేసిత కణాలు ఆనోడ్వైపు చలించబడతాయి.
![]()
ప్రశ్న 30.
క్రింది పదాలను వివరించండి.
(ఎ) ఎలక్ట్రోఫారిసిస్
(బి) స్కందనం
(సి) టిండాల్ ఫలితం
జవాబు:
(ఎ) ఎలక్ట్రోఫారిసిస్ :
కొల్లాయిడ్ ద్రావణంలో రెండు ప్లాటినం ఎలక్ట్రోడ్లు ముంచి ఉంచి వాటి మధ్య విద్యుత్ పొటెన్షియల్ను ఆవర్తనం చేసినట్లైతే కొల్లాయిడ్ కణాలు రెండు ఎలక్ట్రోడ్లలో ఏదోఒక దానివైపుగా ప్రయాణిస్తాయి. అనువర్తిత emf ప్రభావంతో కొల్లాయిడ్ కణం చలనం చెందే ప్రక్రియను విద్యుదావేశితకణ చలనం (లేదా) ఎలక్ట్రోఫోరసిస్ అంటారు.
(బి) స్కందనం :
సాల్ కొల్లాయిడ్ కణాలు- పాత్ర అడుగు భాగానికి చేరి స్థిరపడే ప్రక్రియను సాల్స్కంధనం లేదా అవక్షేపణం లేదా ఫ్లాక్యులేషన్ అంటారు.
(సి) టిండాల్ ఫలితం :
“కాంతి, కొల్లాయిడ్ ద్రావణం ద్వారా ప్రయాణించినప్పుడు, కాంతి మార్గాన్ని మనం ఒక కాంతివంతమైన పుంజంగా చూడవచ్చు. ఈ దృగ్విషయాన్నే “టిండాల్ ఫలితం” అంటారు.
ఇది ఒక దృక్ ధర్మం.
కారణము :
కొల్లాయిడ్ ద్రావణం ద్వారా కాంతి ప్రసరించినప్పుడు ఆ కాంతి పెద్దసైజు కణాలు అయిన కొల్లాయిడ్ల విక్షిప్త, ప్రావస్థా కణాలలో పరిక్షేపణం చెందుతాయి.
- ఆకాశము నీలంగా ఉండటానికి టిండాల్ ప్రభావమే కారణము.
- నిజద్రావణాలు టిండాల్ ప్రభావాన్ని ప్రదర్శించవు.
ప్రశ్న 31.
క్రింది వాటిలో కనిపించే ఘటనలను వివరించండి.
(ఎ) కొల్లాయిడ్ సాల్ గుండా కాంతిపుంజాన్ని పంపినప్పుడు
(బి) ఆర్ద్ర ఫెర్రిక్ ఆక్సైడ్కు NaCl విద్యుద్విశ్లేష్యకం కలిపినప్పుడు
(సి) కొల్లాయిడ్ ద్రావణం ద్వారా విద్యుత్ ప్రసారం జరిగినప్పుడు
జవాబు:
(ఎ) కొల్లాయిడాల్ గుండా కాంతిపుంజాన్ని పంపినప్పుడు టిండాల్ ఫలితం గమనించబడును.
టిండాల్ ఫలితం :
“కాంతి, కొల్లాయిడ్ ద్రావణం ద్వారా ప్రయాణించినప్పుడు, కాంతి మార్గాన్ని మనం ఒక కాంతివంతమైన పుంజంగా చూడవచ్చు. ఈ దృగ్విషయాన్నే “టిండాల్ ఫలితం” అంటారు.
ఇది ఒక దృక్ ధర్మం.
కారణము :
కొల్లాయిడ్ ద్రావణం ద్వారా కాంతి ప్రసరించినప్పుడు ఆ కాంతి పెద్దసైజు కణాలు అయిన కొల్లాయిడ్ల విక్షిప్త, ప్రావస్థా కణాలలో పరిక్షేపణం చెందుతాయి.
- ఆకాశము నీలంగా ఉండటానికి టిండాల్ ప్రభావమే కారణము.
- నిజద్రావణాలు టిండాల్ ప్రభావాన్ని ప్రదర్శించవు.

(బి) ఆర్ధ ఫెర్రిక్ క్లోరైడ్ కొల్లాయిడ్ ద్రావణానికి NaCI ద్రావణం కలిపితే స్కందనం జరుగుతుంది. ఇచ్చట కొల్లాయిడ్
కణాలమీది ఆవేశాలు పరస్పరం తటస్థపరచబడి అవక్షేపణం చెందుతాయి.
(సి) కొల్లాయిడ్ ద్రావణం ద్వారా విద్యుత్ ప్రసారం జరిగినపుడు ఎలక్ట్రోఫోరసిస్ జరుగును.
ఎలక్ట్రోఫారిసిస్ :
కొల్లాయిడ్ ద్రావణంలో రెండు ప్లాటినం ఎలక్ట్రోడ్లు ముంచి ఉంచి వాటి మధ్య విద్యుత్ పొటెన్షియల్ను ఆవర్తనం చేసినట్లైతే కొల్లాయిడ్ కణాలు రెండు ఎలక్ట్రోడ్లలో ఏదోఒక దానివైపుగా ప్రయాణిస్తాయి. అనువర్తిత emf ప్రభావంతో కొల్లాయిడ్ కణం చలనం చెందే ప్రక్రియను విద్యుదావేశితకణ చలనం (లేదా) ఎలక్ట్రోఫోరసిస్ అంటారు.
ప్రశ్న 32.
పటం సహాయంతో కాటరెల్ పొగ అవక్షేపకరణిని వర్ణించండి.
జవాబు:
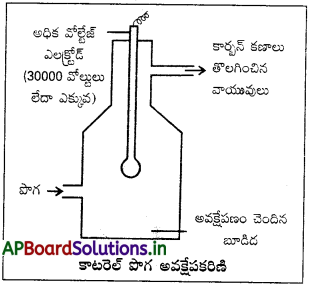
కాటరెల్ పొగ అవక్షేపకరణి :
కార్బన్, ఆర్సినిక్ సమ్మేళనాలు, ధూళి కణాలు మొదలైన ఘనస్థితిలో ఉండే కణాలు గాలిలో ఏర్పరచే కొల్లాయిడ్ ద్రావణమే పొగ, పొగగొట్టం నుంచి పొగ బయటకు వచ్చే ముందుగానే అవక్షేపకరిణి ద్వారా పంపుతారు. దీనిలో పొగ కణాల ఆవేశానికి విరుద్ధంగా ఉండే ఆవేశం గల ప్లేట్లు అమర్చి ఉంటాయి. కాబట్టి పొగలోని కణాలు వీటితో సంపర్కానికి వచ్చిన వెంటనే అవి వాటి ఆవేశాన్ని అవక్షేపణం చెందుతాయి. కాబట్టి గది నేలపై ఈ కణాలు స్థిరపడతాయి. ఈ అవక్షేపకరణిని కాటరెల్ అవక్షేపకరిణి అంటారు.
ప్రశ్న 33.
ఆర్ధ ఫెర్రిక్ క్లోరైడ్ సాల్న స్కందనం చేయడానికి NaCl, Na2SO4, Na3PO4 లలో ఏది అధిక ప్రభావం చూపుతుంది.? కారణం ఏమిటి?
జవాబు:
ఆర్ద్రఫెర్రిక్ క్లోరైడ్ సాల్న స్కందనం చేయడానికి NaCl, Na2SO4, Na3PO4 లలో Na3PO4 అధిక ప్రభావం చూపుతుంది.
- దీనిని హార్టీషూల్ట్ నియమం ద్వారా వివరించవచ్చు.
సామాన్యంగా స్కంధన అయాన్ వేలన్సీ పెరిగిన కొలది దాని స్కంధన సామర్థ్యం పెరుగును. దీనినే హార్డీ – షూల్జ్ నియమం అంటారు. - ఇవ్వబడిన లవణాలలోని ఆనయాన్ల స్కందన సామర్థ్య క్రమం PO4-3 > SO4-2 > ClO–.
ప్రశ్న 34.
ఒక లయోఫిలిక్ కొల్లాయిడ్, ఒక లయోఫోబిక్ కొల్లాయిడ్ను ఎలా పరిరక్షిస్తుంది?
జవాబు:
లయోఫిలిక్ కొల్లాయిడ్ను లయోఫోబిక్ కొల్లాయిడ్కు కలుపుట ద్వారా వాటి స్కందన ఘటన నుండి పరిరక్షిస్తారు.
లయోఫిలిక్ కొల్లాయిడ్లను పరిరక్షక కొల్లాయిడ్లు అంటారు.
లయోఫిలిక్ కొల్లాయిడ్ లయోఫోబిక్ కొల్లాయిడ్ చుట్టూ ఒక పరిరక్షక వలయాన్ని ఏర్పరచి స్కందన ప్రక్రియ జరగకుండా ఆపివేస్తుంది.
ప్రశ్న 35.
క్రిందివాటిలో కొల్లాయిడ్ల ఉపయోగం తెలపండి.
(ఎ) తాగేనీటిని శుద్ధి చేయడం
(బి) టానింగ్
(సి) ఔషధాలు
జవాబు:
(ఎ) తాగేనీటిని శుద్ధి చేయడం :
ప్రకృతి వనరుల నుంచి లభ్యం అయిన నీటిలో సామాన్యంగా మలినాలు అవలంబనం చెంది ఉంటాయి. ఈ నీటికి పటికను కలిపినట్లైతే, అవలంబిత కణాలు స్కందన ప్రక్రియకు గురి అవుతాయి. ఆ నీరు త్రాగడానికి అనువుగా ఉంటుంది.
(బి) టానింగ్ :
జంతు చర్మాలకు కొల్లాయిడ్ స్వభావం ఉంటుంది. ధనావేశం గల కణాలు గల చర్మాన్ని టానిన్లో నానబెట్టినట్లైతే టానిన్ లోని ఋణావేశ కొల్లాయిడ్ కణాలు చర్మంలోని ధనావేశ కణాలు పరస్పరం స్కందన ప్రక్రియకు గురవుతాయి. ఈ ప్రక్రియ ద్వారా చర్మం గట్టిపడుతుంది (తోలు). ఈ ప్రక్రియను టానింగ్ అంటారు. టానిన్కు బదులుగా క్రోమియమ్ను కూడా ఉపయోగిస్తారు.
(సి) ఔషధాలు :
చాలా ఔషధాలు స్వభావంలో కొల్లాయిడ్లుగానే ఉన్నాయి. ఉదాహరణకు కంటి లోషన్ గా వాడే ఆర్జిరోల్ అనేది సిల్వర్సాల్. కలాజార్ అనే వ్యాధిని నయం చేయడానికి ఆంటిమొనీ కొల్లాయిడ్ వాడతారు. కొల్లాయిడల్ గోల్డ్ను కండరాంతర (intramuscular) ఇంజెక్షన్గా వాడతారు. ఉదర అస్వస్థతలకు, మిల్క్ ఆఫ్ మెగ్నీషియా అనే ఎమల్షన్ ఉపయోగిస్తారు. కొల్లాయిడ్ రూపంలో ఉండే ఔషధాలు చాలా ప్రభావితంగా ఉంటాయి. ఎందుకంటే వీటి ఉపరితల వైశాల్యం అధికంగా ఉండటం కారణంగా ఇవి సులభంగా శరీరంలో జీర్ణించుకొంటాయి.
![]()
ప్రశ్న 36.
గోల్డ్ సంఖ్యను నిర్వచించండి.
జవాబు:
గోల్డ్ సంఖ్య – నిర్వచనము :
“1 మి.లీ. 10% NaCl ద్రావణాన్ని చేర్చడం ద్వారా, 10 మి.లీ. ప్రమాణ గోల్డ్సెల్ ద్రావణం స్కందనం చెందకుండా పరిరక్షించడానికి చేర్చే అనార్థ లయోఫిలిక్సాల్ కనీస ద్రవ్యరాశి (మిల్లీగ్రాములలో).”
గోల్డ్ సంఖ్య పరిమాణం తగ్గినకొద్దీ, దాని పరిరక్షక సామర్థ్యం అధికం.
కొన్ని పరిరక్షణ కొల్లాయిడ్ల గోల్డ్ సంఖ్యలు :
| పరిరక్షణ కొల్లాయిడ్ | గోల్డ్ సంఖ్య |
| జిలటిన్ | 0.005 – 0.01 |
| హీమోగ్లోబిన్ | 0.03 -0.07 |
| ఆల్బిమిన్ | 0.1 -0.2 |
| స్టార్చ్ | 25 |
ప్రశ్న 37.
ఎమల్షన్ను, ఎమల్సిఫయర్లు ఎలా స్థిరపరుస్తాయి? రెండు ఎమల్సిఫయర్లను తెలపండి.
జవాబు:
ఒక ఎమల్షన్ స్థిరంగా ఉండేందుకు దానికి చేర్చే మూడో పదార్థమే ఎమల్సీకరణ కారకము.
ఉదా : సబ్బులు – నీటిలో కిరోసిన్ ఎమల్షన్ ను స్థిరపరుస్తారు.
ఎమల్సీ కారకం విక్షిప్తం చెందిన కణాలు, విక్షేపణ యానకం కణాల మధ్య అంతర్ తల పొరగా ఏర్పడుతుంది. ఉదా : కేసీన్, సిలికా, సబ్బు.
దీర్ఘ సమాధాన ప్రశ్నలు
ప్రశ్న 1.
అభిశోషణం, అధిశోషణం, శోషణం పదాలను వివరించండి. భిన్నరకాల అధికశోషణాలను వివరించండి.
జవాబు:
అభిశోషణం :
“ఏదైనా ఒక పదార్థపు అణువులు, ఇతర పదార్థపు ఉపరితలంపై మరియు అంతర్భాగంలో కూడా ఏకరీతిగా వ్యాప్తి చెందడాన్ని ‘అభిశోషణం’ అంటారు.
ఇది ఒక ఆయతన దృగ్విషయం.
ఉదా :
i) నీటిలో ముంచిన ‘స్పాంజ్’ నీటిని అభిశోషించుకుంటుంది.
ii) రంగు. సిరాలో ఉంచిన సుద్దముక్క సిరాను అభిశోషించుకుంటుంది.
అధిశోషణం :
“ఒక పదార్థం వేరొక ద్రవం లేదా ఘన పదార్థం ఉపరితలంపై గాఢత చెందడాన్ని ‘అధిశోషణం’ అంటారు. ఇది ఒక ఉపరితల దృగ్విషయము.
ఉదా : i) CO2, SO2, Cl2 లాంటి వాయువులను ఉత్తేజిత బొగ్గు అధిశోషించుకుంటుంది.
ii) Pt లేక Ni లోహం, హైడ్రోజన్ వాయువుతో సంపర్కంలో ఉంటే ఆ వాయువును అధిశోషించుకుంటుంది.
భౌతిక అధిశోషణం :
అధిశోషణ ప్రక్రియలో అధిశోషితం, అధిశోషకం మధ్య వాండర్వాల్ బలాలు కలిగి ఉంటే ఆ అధిశోషణంను భౌతిక అధిశోషణం అంటారు.
ధర్మాలు :
- వాండర్వాల్ బలాల ద్వారా జరుగుతుంది.
- స్వభావంలో విశిష్టత కనబరచదు.
- ద్విగత- స్వభావం ఉంటుంది.
- వాయువు స్వభావంపై ఆధారపడి ఉంటుంది. సులభంగా ద్రవాలుగా మారే వాయువులు సులభంగా అధిశోషణం గురు చెందుతాయి.
- అధిశోషణం ఎంథాల్పీ అల్పం 20 – 40 KJ మోల్-1.
- అల్ప ఉష్ణోగ్రతలు అధిశోషణం ప్రక్రియను ప్రోత్సహిస్తాయి. ఉష్ణోగ్రత పెరుగుదలతో ఇది తగ్గుతుంది.
- దీని ఉత్తేజిత శక్తి విలువ నామమాత్రంగా ఉంటుంది.
- ఉపరితల వైశాల్యంపై ఆధారపడి ఉంటుంది. ఉపరితల వైశాల్యం పెరిగితే అధిశోషణం పరిమాణం కూడా పెరుగుతుంది.
- అధిక పీడనాల వద్ద అధిశోషకం ఉపరితలంపై బహు పొరలు ఏర్పడతాయి.
రసాయన అధిశోషణం :
అధిశోషణ ప్రక్రియలో అధిశోషితం, అధిశోషకం మధ్య రసాయన బలాలు (బంధాలు) లేదా వేలన్సీ బలాలు కలిగి ఉంటే ఆ అధిశోషణంను రసాయన అధిశోషణం అంటారు.
ధర్మాలు :
- రసాయన బంధం ఏర్పడటం ద్వారా జరుగుతుంది.
- స్వభావంలో అత్యధిక విశిష్టతను కనబరుస్తుంది.
- అద్విగత స్వభావం ఉంటుంది.
- ఇది కూడా వాయువు స్వభావంపై ఆధారపడి ఉంటుంది. అధిశోషకంతో రసాయనిక చర్య జరిపే వాయువులు కెమిసారనన్ను ప్రదర్శిస్తాయి.
- అధిశోషణం ఎంథాల్పీ అధికం (80 – 240 KJ మోల్-1).
- అధిశోషణం అధిక ఉష్ణోగ్రతల వద్ద జరుగుతుంది. ఉష్ణోగ్రత పెరిగితే ఇది కూడా పెరుగుతుంది.
- దీనికి కొన్ని సందర్భాలలో అధిక ఉత్తేజిత శక్తి అవసరమవుతుంది.
- ఇది కూడా ఉపరితల వైశాల్యంపై ఆధారపడి ఉంటుంది. దీనిలో కూడా ఉపరితల వైశాల్యం పెరిగితే, అధిశోషణం పరిమాణం పెరుగుతుంది.
- ఏకపొర మాత్రమే ఏర్పడుతుంది.
ప్రశ్న 2.
భౌతిక అధిశోషణం అభిలాక్షణిక లక్షణాలను చర్చించండి.
జవాబు:
భౌతిక అధిశోషణం :
అధిశోషణ ప్రక్రియలో అధిశోషితం, అధిశోషకం మధ్య వాండర్వాల్ బలాలు కలిగి ఉంటే ఆ అధిశోషణంను భౌతిక అధిశోషణం అంటారు.
ధర్మాలు :
- వాండర్వాల్ బలాల ద్వారా జరుగుతుంది.
- స్వభావంలో విశిష్టత కనబరచదు.
- ద్విగత స్వభావం ఉంటుంది.
- వాయువు స్వభావంపై ఆధారపడి ఉంటుంది. సులభంగా ద్రవాలుగా మారే వాయువులు సులభంగా అధిశోషణం చెందుతాయి.
- అధిశోషణం ఎంథాల్పీ అల్పం 20 – 40 KJ మోల్-1.
- అల్ప ఉష్ణోగ్రతలు అధిశోషణం ప్రక్రియను ప్రోత్సహిస్తాయి. ఉష్ణోగ్రత పెరుగుదలతో ఇది తగ్గుతుంది.
- దీని ఉత్తేజిత శక్తి విలువ నామమాత్రంగా ఉంటుంది.
- ఉపరితల వైశాల్యంపై ఆధారపడి ఉంటుంది. ఉపరితల వైశాల్యం పెరిగితే అధిశోషణం పరిమాణం కూడా పెరుగుతుంది.
- అధిక పీడనాల వద్ద అధిశోషకం ఉపరితలంపై బహు పొరలు ఏర్పడతాయి.
ప్రశ్న 3.
కెమిసాల్షన్ అభిలాక్షణిక ధర్మాలను చర్చించండి.
జవాబు:
i) అధిక విశిష్టత :
కెమిసారేషన్ అత్యధిక విశిష్టతతో కూడుకొని ఉండే ప్రక్రియ. అధిశోషితం, అధిశోషకం, వీటి మధ్య రసాయన బంధం ఏర్పడే అవకాశం ఉన్నప్పుడే ఈ రకం అధిశోషణం జరుగుతుంది. ఉదాహరణకు లోహాలపై లోహ ఆక్సైడ్ల ఏర్పాటు ద్వారా ఆక్సిజన్ వాయువు అధిశోషణం చెందుతుంది. పరివర్తన లోహాలపై లోహ హైడ్రైడ్లను ఏర్పరచడం ద్వారా హైడ్రోజన్ అధిశోషణం జరుగుతుంది.
ii) అద్విగత స్వభావం :
అధిశోషణం ప్రక్రియలో ఉపరితలానికి వాయువుకు మధ్య సమ్మేళనం ఏర్పడటం కారణంగా ఈ ప్రక్రియ అద్విగతంగా ఉంటుంది. కెమిసారేషన్ ప్రక్రియ కూడా ఉష్ణమోచక చర్య. అయితే అల్ప ఉష్ణోగ్రతలవద్ద ఈ చర్య మితవేగాలతో జరుగుతుంది. దీనికి కారణం ఈ ప్రక్రియ ఉత్తేజితశక్తి అధికం. ఉష్ణోగ్రతను పెంచితే, సామాన్య రసాయన చర్యల మాదిరిగానే అధిశోషణం పరిమాణం కూడా పెరుగుతుంది. అల్ప ఉష్ణోగ్రతలవద్ద జరిగిన ఫిజిసారేషన్ ప్రక్రియ అధిక ఉష్ణోగ్రతల వద్ద కెమిసార్ధాన్గా మారుతుంది. సాధారణంగా అధిక పీడనాలు కూడా కెమిసారన్ను ప్రోత్సహిస్తాయి.
iii) ఉపరితల వైశాల్యం :
భౌతిక అధిశోషణం మాదిరిగానే కెమిసార్షన్ కూడా ఉపరితల వైశాల్యం పెరిగితే అధిశోషణం పరిమాణం కూడా పెరుగుతుంది.
iv) అధిశోషణం ఎంథాల్పీ :
కెమిసారేషన్ ఎంథాల్పీ విలువ అధికం (80 – 240 kJ మోల్-1). ఎందుకంటే దీనిలో రసాయన బంధం ఏర్పడుతుంది.
స్థిర ఉష్ణోగ్రత వద్ద పీడనం మార్పుతో అధిశోషకంపై అధిశోషణం చెందే వాయువు పరిమాణంలో కలిగే మార్పుని అధిశోషణ సమోష్ణరేఖ అనే వక్రం ద్వారా వ్యక్తం చేయవచ్చు.
![]()
ప్రశ్న 4.
ఫిజిసాల్షన్, కెమిసార్షిన్ దృగ్విషయాలను లేదా ఘటనలను తులనం చేయండి. భేదపరచండి.
జవాబు:
భౌతిక అధిశోషణం :
అధిశోషణ ప్రక్రియలో అధిశోషితం, అధిశోషకం మధ్య వాండర్ వాల్ బలాలు కలిగి ఉంటే ఆ అధిశోషణంను భౌతిక అధిశోషణం అంటారు.
ధర్మాలు :
- వాండర్ వాల్ బలాల ద్వారా జరుగుతుంది.
- స్వభావంలో విశిష్టత కనబరచదు.
- ద్విగత స్వభావం ఉంటుంది.
- వాయువు స్వభావంపై ఆధారపడి ఉంటుంది. సులభంగా ద్రవాలుగా మారే వాయువులు సులభంగా అధిశోషణం చెందుతాయి.
- అధిశోషణం ఎంథాల్పీ అల్పం 20 – 40 KJ మోల్-1.
- అల్ప ఉష్ణోగ్రతలు అధిశోషణం ప్రక్రియను ప్రోత్సహిస్తాయి. ఉష్ణోగ్రత పెరుగుదలతో ఇది తగ్గుతుంది.
- దీని ఉత్తేజిత శక్తి విలువ నామమాత్రంగా ఉంటుంది.
- ఉపరితల వైశాల్యంపై ఆధారపడి ఉంటుంది. ఉపరితల వైశాల్యం పెరిగితే అధిశోషణం పరిమాణం కూడా పెరుగుతుంది.
- అధిక పీడనాల వద్ద అధిశోషకం ఉపరితలంపై బహు పొరలు ఏర్పడతాయి.
రసాయన అధిశోషణం :
అధిశోషణ ప్రక్రియలో అధిశోషితం, అధిశోషకం మధ్య రసాయన బలాలు (బంధాలు) లేదా వేలన్సీ బలాలు కలిగి ఉంటే ఆ అధిశోషణంను రసాయన అధిశోషణం అంటారు.
ధర్మాలు :
- రసాయన బంధం ఏర్పడటం ద్వారా జరుగుతుంది.
- స్వభావంలో అత్యధిక విశిష్టతను కనబరుస్తుంది.
- అద్విగత స్వభావం ఉంటుంది.
- ఇది కూడా వాయువు స్వభావంపై ఆధారపడి ఉంటుంది. అధిశోషకంతో రసాయనిక చర్య జరిపే వాయువులు కెమిసారనన్ను ప్రదర్శిస్తాయి.
- అధిశోషణం ఎంథాల్పీ అధికం (80 – 240 KJ మోల్-1).
- అధిశోషణం అధిక ఉష్ణోగ్రతల వద్ద జరుగుతుంది. ఉష్ణోగ్రత పెరిగితే ఇది కూడా పెరుగుతుంది.
- దీనికి కొన్ని సందర్భాలలో అధిక ఉత్తేజిత శక్తి అవసరమవుతుంది.
- ఇది కూడా ఉపరితల వైశాల్యంపై ఆధారపడి ఉంటుంది. దీనిలో కూడా ఉపరితల వైశాల్యం పెరిగితే, అధిశోషణం పరిమాణం పెరుగుతుంది.
ప్రశ్న 5.
అధిశోషణం సమోష్ణరేఖ అంటే ఏమిటి? ఫ్రాయిండ్లిష్ అధిశోషణ సమోష్ణరేఖ ద్వారా ఘనపదార్థాలపై వాయువుల అధిశోషణాన్ని వివరించండి.
జవాబు:
అధిశోషణ సమోష్ణగ్రతా రేఖలు :
స్థిర ఉష్ణోగ్రత వద్ద ఏకాంక ద్రవ్యరాశిగల ఘనస్థితిలోని అధిశోషకంపై అధిశోషణం చెందే వాయువు పరిమాణానికి, వాయువు పీడనానికి మధ్యగల అనుభావిక సంబంధాన్ని తెలిపే రేఖలను అధిశోషణ సమోష్ణరేఖలు అంటారు.
ఫ్రాయిండ్లిష్ అధిశోషణ సమోష్ణరేఖ సమీకరణం
ప్రశ్న 6.
అధిశోషణం అనువర్తనాలను గురించి వివరంగా తెలపండి.
జవాబు:
(i) అధిక శూన్యస్థితిని ఏర్పరచడం :
ఒక పాత్రలో అధిక శూన్య స్థితిని పొందడానికి ఆ పాత్రలోని గాలిని నిర్వాత పంపు ‘ద్వారా తొలగిస్తారు. ఈ ప్రక్రియలో. పాత్రలో ఇంకా మిగిలి ఉన్న కొద్దిపాటి గాలిని, బొగ్గును ఉపయోగించి అధిశోషణ ప్రక్రియ ద్వారా తొలగిస్తారు.
(ii) వాయు ముసుగు (gas mask) :
బొగ్గు గనులలో పనిచేసే కార్మికులు గాలిని పీల్చుకొనేటప్పుడు గాలిలోని విషవాయువులను అధిశోషించుకోవడానికి వాడే సాధనాన్ని వాయు ముసుగు అంటారు. ఇది ఉత్తేజపరిచిన బొగ్గు లేదా ఇతర అధిశోషకాల మిశ్రమంతో నిండి ఉంటుంది.
(iii) తేమను నియంత్రణ చేయడం :
నివాస గదులలో ఉండే తేమను తొలగించి, గాలిలోని తేమను నియంత్రణ చేయడానికి సిలికాజెల్ అల్యూమినాజెల్లను అధిశోషకాలుగా ఉపయోగిస్తారు.
(iv) మలిన రంగు ద్రావణాల నుంచి రంగు మలినాలను తొలగించడం :
మలిన రంగు ద్రావణాల రంగుకు కారణమైన రంగు మలినాలను, ద్రావణాల నుంచి జాంతవ బొగ్గు ద్వారా తొలగిస్తారు.
(v) విజాతి ఉత్ప్రేరణం :
ఘనస్థితిలో ఉండే ఉత్ప్రేరకాల ఉపరితలాలపై చర్యలోని క్రియాజనకాలు అధిశోషణం చెందడం ద్వారా చర్యావేగం పెరుగుతుంది. ఘనస్థితి ఉత్ప్రేరకాల వాడకాన్ని పారిశ్రామిక ప్రాముఖ్యం ఉన్న చాలా వాయుస్థితి చర్యలలో మనం గమనిస్తాం. హేబర్ పద్ధతిలో అమోనియా సంశ్లేషణలలో ఐరన్ ను, స్పర్శ (కాంటాక్ట్) పద్ధతిలో H2SO4 తయారీలో V2O6 ను, తైలాలను హైడ్రోజనీకరణం చేసే (వనస్పతి) చర్యలలో సూక్ష్మవిభాజిత Niను ఉత్ప్రేరకాలుగా ఉపయోగించే చర్యలు విజాతి ఉత్ప్రేరణ చర్యలకు ఉదాహరణలు.
(vi) జడ వాయువులను వాటి మిశ్రమం నుంచి వేరుపరచడం :
బొగ్గుపై వాయువుల అధిశోషణం సామర్థ్యం లేదా అవధి భిన్న వాయువులకు భిన్నంగా ఉంటుంది. కొబ్బరి బొగ్గుపై భిన్న జడవాయువుల అధిశోషణం అవధి భిన్న ఉష్ణోగ్రతల వద్ద భిన్నంగా ఉండటం ఆధారంగా, వ్యక్తిగత జడవాయువులను వాటి మిశ్రమం నుంచి భిన్న ఉష్ణోగ్రతల వద్ద జరిపే అధిశోషణ ప్రక్రియ ద్వారా వేరుపరుస్తారు.
(vii) వ్యాధులను నయం చేయడం :
క్రిముల ద్వారా కలిగే వ్యాధులను నయం చేయడానికి వాడే చాలా ఔషధాలు ఈ . క్రిములపై అధిశోషణం చెంది వాటి చంపుతాయి.
(viii) నురుగు ప్లవన ప్రక్రియ :
అల్ప నాణ్యత గల సల్ఫైడ్ ఖనిజాల నుంచి సిలికా లేదా ఇతర మట్టి మలినాలను పైన్ నూనెను నురుగు కారకాలను వాడి తొలగించి, ఖనిజాన్ని గాఢతపరిచే విధానంలో అధిశోషణం ప్రక్రియ చోటుచేసుకొంటుంది.
(ix) అధిశోషణ సూచికలు :
సిల్వలర్ హాలైడ్ల వంటి కొన్ని అవక్షేపాలు, వాటి ఉపరితలాలపై ఇయోసిన్, ఫ్లోరసీన్ లాంటి కొన్ని రంజనాలను అధిశోషణ చెందించుకొని, అభిలాక్షణిక రంగు మార్పును కలిగించుకుంటాయి. దీని ఆధారంగా అర్జెంటోమెట్రిక్ టైట్రేషన్లలో అంతిమ బిందువును రంజన పదార్థాల ద్వారా నిర్ణయిస్తారు.
(x) క్రొమొటోగ్రాఫిక్ విశ్లేషణం :
విశ్లేషణ పద్ధతులలోను, పారిశ్రామిక పద్ధతులలోను, అధిశోషణ దృగ్విషయం ఆధారంగా రూపొందించబడిన క్రొమొటోగ్రాఫిక్ పద్ధతులను విస్తారంగా ఉపయోగిస్తారు.
ప్రశ్న 7.
ఉత్ప్రేరణం అంటే ఏమిటి? ఉత్ప్రేరణాన్ని ఎలా వర్గీకరిస్తాం? ఉదాహరణలు ఇవ్వండి.
జవాబు:
ఉత్ప్రేరకం మరియు ఉత్ప్రేరణం :
రసాయన చర్యలో తాను వినియోగం చెందకుండా చర్యా వేగాన్ని పెంచే చర్యకు కలిపిన ఇతర పదార్థమే ఉత్ప్రేరకం (catalyst).
చర్యా మిశ్రమానికి బాహ్య పదార్థాన్ని కలిపి, చర్యా వేగాన్ని పెంచే ప్రక్రియను ఉత్ప్రేరణ (catalysis) అంటారు.
ఉత్ప్రేరణ వర్గీకరణ :
ఉత్ప్రేరకం మరియు క్రియాజనకాల భౌతిక స్థితుల (ప్రావస్థల ఆధారంగా ఉత్ప్రేరణాన్ని రెండు. రకాలుగా వర్గీకరించారు. అవి :
ఎ) సజాతి ఉత్ప్రేరణ :
ఒక ఉత్ప్రేరక రసాయన చర్యలో ఉత్ప్రేరకం మరియు క్రియాజనకాలు ఒకే భౌతిక ప్రావస్థలో ఉంటే దాన్ని సజాతి ఉత్ప్రేరణ అంటారు.
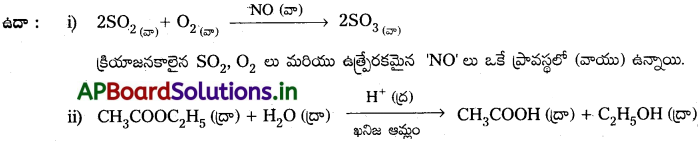
క్రియాజనకాలైన ఎస్టర్, H2O లు మరియు ఉత్ప్రేరకమైన ఆమ్లము ఒకే ప్రావస్థలో (ద్రవం) ఉన్నాయి.
బి) విజాతి ఉత్ప్రేరణ :
ఒక ఉత్ప్రేరక రసాయన చర్యలో ఉత్ప్రేరకం మరియు క్రియాజనకాలు భిన్న భౌతిక ప్రావస్థలలో ఉంటే దాన్ని విజాతి ఉత్ప్రేరణ అంటారు.
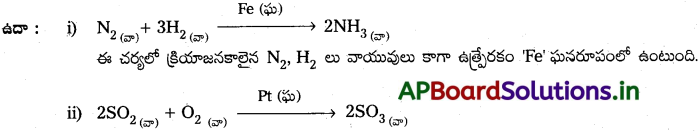
ఈ చర్యలో క్రియాజనకాలైన SO2, O2 లు వాయువులు కాగా ఉత్ప్రేరకం ‘Pt’ ఘన రూపంలో ఉంటుంది.
![]()
ప్రశ్న 8.
విజాతి ఉత్ప్రేరణం చర్యా విధానాన్ని చర్చించండి.
జవాబు:
అధిశోషణ సిద్ధాంతం విజాతి ఉత్ప్రేరణ చర్య విధానం వివరించినది.
చర్యా విధానం :
(i) ఉత్ప్రేరకం ఉపరితలం వద్దకు క్రియాజనకాల వ్యాపనం.
(ii) ఉత్ప్రేరకం ఉపరితలంపై క్రియాజనకాలు అధిశోషణం చెందడం.

(iii) మధ్యస్థ పదార్థం ఏర్పడటం ద్వారా ఉత్ప్రేరకం ఉపరితలంపై రసాయన చర్య జరగడం.
(iv) ఉత్ప్రేరకం ఉపరితలం నుండి క్రియాజన్యాలు విశోషణం చెందడం ఫలితంగా, తిరిగి మరికొంతమేర రసాయన చర్య జరగడానికి శుద్ధ ఉపరితలాన్ని సమకూర్చడం.
(v) ఉత్ప్రేరకం ‘ఉపరితలం నుండి చర్య క్రియాజన్యాలు వ్యాపనం చెందటం.
ప్రశ్న 9.
ఎంజైమ్లు అంటే ఏమిటి? ఎంజైమ్ ఉత్ప్రేరణాన్ని వివరణ, ఉదాహరణలతో సహా చర్చించండి.
జవాబు:
ప్రాణం గల మొక్కలు, జంతువులు ఉత్పత్తి చేసే సంక్లిష్ట నైట్రోజన్ కర్బన సమ్మేళనాలను ఎంజైమ్లు అంటారు.
- ఎంజైమ్లు జీవ రసాయనిక ఉత్ప్రేరకాలుగా పని చేస్తాయి.
- ఆయుఃప్రక్రియ కొనసాగడానికి దోహదం చేసే జంతువులు మొక్కలలో జరిగే చాలా రసాయన చర్యలను ఇవి ‘ఉత్ప్రేరణం చేస్తాయి.
అధిక చర్యాశీలత లేదా సామర్థ్యం, అధిక వరణాత్మక ధర్మం ఉండటం అనేది ఎంజైమ్ ఉత్ప్రేరణం ప్రత్యేకత. ఎంజైమ్ ఉత్ప్రేరకాలు క్రింది అభిలాక్షణిక ధర్మాలను ప్రదర్శిస్తాయి.
(i) అత్యధిక ఉత్ప్రేరణ సామర్థ్యం :
ఒక ఎంజైమ్ అణువు సుమారు ఒక మిలియన్ క్రియాజనక అణువులను ఒక నిమిషంలో పరివర్తన చర్యలకు గురిచేస్తుంది.
(ii) అత్యధిక వరణాత్మక గుణం :
ప్రతీ చర్యకు ఒక ప్రత్యేక ఎంజైమ్ ఉంటుంది. అంటే ఒక ఉత్ప్రేరకం, ఒక రకం, చర్యనే ఉత్ప్రేరణం చేస్తుంది. ఉదాహరణకు యూరియేజ్ ఎంజైమ్ యూరియా జలవిశ్లేషణ చర్యను మాత్రమే ఉత్ప్రేరణం చేస్తుంది. ఏ ఇతర ఎమైడ్ జలవిశ్లేషణ చర్యను ఉత్ప్రేరణం చెయ్యదు.
(iii) యుక్తతమ (optimum) ఉష్ణోగ్రత వద్ద మాత్రమే అధిక చర్యాశీలతను ప్రదర్శించడం :
యుక్తతమ ఉష్ణోగ్రత అనే ప్రత్యేక ఉష్ణోగ్రత వద్ద ఎంజైమ్ చర్యరేటు గరిష్ఠంగా ఉంటుంది. ఈ యుక్తతమ ఉష్ణోగ్రతకు రెండువైపులా గల ఉష్ణోగ్రతల వద్ద “ఎంజైమ్ క్రియాశీలత తగ్గుతుంది. ఎంజైమ్ క్రియాశీలతకు అనువైన ఉష్ణోగ్రత వ్యాప్తి 298 – 310 K.గా ఉంటుంది. మానవ శరీర ఉష్ణోగ్రత 310 K ఎంజైమ్ ఉత్ప్రేరణ చర్యలకు అనువుగా ఉంటుంది.
(iv) యుక్తతమ pH వద్ద అత్యధిక చర్యాశీలతను ప్రదర్శించడం :
యుక్తతమ pH అనే ఒక ప్రత్యేక pH విలువ వద్ద మాత్రమే ఎంజైమ్ ఉత్ప్రేరక చర్యరేటు గరిష్ఠంగా ఉంటుంది. ఇది 5 – 7 pH ల మధ్య ఉంటుంది.
(v) ఉత్తేజకాలు, కో-ఎంజైమ్ల సమక్షంలో క్రియాశీలత పెరుగుదల :
కో-ఎంజైమ్లు అనే కొన్ని ఇతర పదార్థాల సమక్షంలో ఎంజైమ్ క్రియాశీలత పెరుగుతుంది. ఒక ఎంజైమ్తో సహా కొద్ది పరిమాణంలో ప్రోటీన్ కాని వేరొక పదార్థం (విటమిన్) కూడా ఉన్నట్లైతే, ఎంజైమ్ క్రియాశీలత గణనీయంగా పెరుగుతుంది.
Na+, Mn2+, Co2+, Cu2+ లాంటి లోహ అయాన్లు సాధారణంగా ఉత్తేజకాలుగా ఉంటాయి. ఈ లోహ అయాన్లు, ఎంజైమ్ అణువులతో బలహీనంగా బంధితమై, ఎంజైమ్ల క్రియాశీలతను పెంచుతాయి. సోడియమ్ క్లోరైడ్ అంటే Na+ అయాన్ల సమక్షంలో ఎమైలేజ్ క్రియాశీలత పెరుగుతుంది.
(vi) నిరోధకాలు, విషపదార్థాల ప్రభావం :
సాధారణ ఉత్ప్రేరకాల మాదిరిగానే ఇతర పదార్థాల సమక్షంలో ఎంజైమ్లు కూడా నిరోధకాలు లేదా విషపదార్థాలుగా పనిచేస్తాయి. ఎంజైమ్ ఉపరితలంపై చోటుచేసుకొని ఉండే క్రియాశీలత గల గ్రూపుతో ఈ నిరోధకాలు లేదా విషపదార్థాలు చర్యలో పాల్గొని ఎంజైమ్ల ఉత్ప్రేరణ క్రియాశీలతను తగ్గించడం లేదా పూర్తిగా నాశనం చేయడం చేస్తాయి. మన శరీరంలో చాలా ఔషధాలు ఎంజైమ్ నిరోధకాలుగా పనిచేసి వ్యాధిని నయం చేస్తాయి.

ఎంజైమ్ల ఉత్ప్రేరిత చర్యలు రెండు అంచెలలో జరుగును.
అంచె – 1 : ఎంజైమ్ క్రియాజనకం బంధితమై ఉత్తేజిత సంక్లిష్టం (ES*) ఏర్పడుతుంది.
E+ S → ES*
అంచె – 2 : ఈ ఉత్తేజిత సంక్లిష్టం క్రియాజన్యాలుగా వియోగం చెందుట.
ES* → E+ P
చక్కెర విలోమ చర్య :
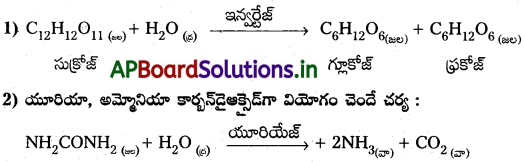
ప్రశ్న 10.
కొల్లాయిడ్ ద్రావణాలు అంటే ఏమిటి? వీటిని ఎలా వర్గీకరిస్తారు? ఉదాహరణలు ఇవ్వండి.
జవాబు:
ఒక పదార్థంలో పెద్దసైజు కణాలుగా వేరొక పదార్థం విక్షేపణం చెంది ఏర్పరచిన విజాతి వ్యవస్థను కొల్లాయిడ్ ద్రావణం అంటారు.
విక్షేపణ యానకం ఆధారంగా కొల్లాయిడ్లను ఈ క్రింది విధంగా వర్గీకరించారు.
- విక్షేపణ యానకం గాలి (వాయువు) అయితే వాటిని ఏరోసాల్లు అంటారు. ఉదా : పొగ.
- విక్షేపణ యానకం నీరు అయితే వాటిని హైడ్రోసాల్లు అంటారు. ఉదా : స్టార్చ్
- విక్షేపణ యానకం ఆల్కహాల్ అయితే వాటిని ఆల్కసాల్లు అంటారు.
విక్షిప్త ప్రావస్థ(ద్రావితం) కణ పరిమాణం 1mµ – 1µ వరకు ఉండే ద్విగుణాత్మక విజాతి వ్యవస్థను కొల్లాయిడ్లు అంటారు.
కొల్లాయిడ్ల వర్గీకరణ :
విక్షిప్త ప్రావస్థ మరియు విక్షేపక యానకం మధ్యగల సంబంధం ఆధారంగా వర్గీకరణ జరిగింది.
ఎ) లయోఫిలిక్ కొల్లాయిడ్లు (ద్రవ ప్రియ కొల్లాయిడ్ లు) :
వీటిలో విక్షేపక యానకంకూ, విక్షిప్త ప్రావస్థకీ మధ్య ఎక్కువ ఆపేక్ష ఉంటుంది.
ఉదా : స్టార్చ్ కొల్లాయిడ్ ద్రావణం లయోఫిలిక్.
బి) లయోఫోబిక్ కొల్లాయిడ్లు (ద్రవ విరోధి కొల్లాయిడ్లు) :
వీటిలో విక్షిప్త ప్రావస్థకూ, విక్షేపక యానకానికీ మధ్య ఆపేక్ష ఉండదు.
ఉదా : గోల్డ్ కొల్లాయిడ్ ద్రావణం లయోఫోబిక్.
ప్రశ్న 11.
విక్షిప్త ప్రావస్థ, విక్షేపణ యానకం వీటి మధ్యగల అన్యోన్య చర్యల ఆధారంగా కొల్లాయిడ్లను ఎలా వర్గీకరిస్తారు ? ప్రతీ రకానికి ఒక ముఖ్య ఉదాహరణ ఇవ్వండి. సాల్ను నిల్వ ఉంచడానికి ఏ రకం సాల్కు స్థిరీకరణ కారకం చేర్చాలి?
జవాబు:
- సముచ్ఛయం చెందిన కొల్లాయిడ్లు (లేదా) మిసెల్లు లయోఫిలిక్, లయోఫోబిక్ భాగాలు కలవి.
- సబ్బులు, సంశ్లేషక డిటర్జెంట్లు ఉదాహరణలు.
- సబ్బులు మురికిని తొలగించే ప్రక్రియలో సబ్బు అణువులు మిసెల్ను మురికి బిందువు వద్ద ఏర్పరుస్తారు.
ప్రశ్న 12.
మిసెల్లు అంటే ఏమిటి? మిసెల్లు ఏర్పడే విధానాన్ని తెలిపి, సబ్బు ప్రదర్శించే శుద్ధి ప్రక్రియను చర్చించండి.
జవాబు:
కొన్ని పదార్థాలు అల్పగాఢతల వద్ద సాధారణ బలమైన విద్యుద్విశ్లేషకాలుగా ప్రవర్తించే పదార్థాలు. అయితే అధిక గాఢతల వద్ద కొల్లాయిడ్ల ప్రవర్తనను ప్రదర్శిస్తాయి. దీనికి కారణం సముచ్ఛములను ఏర్పరచడం ఈ విధంగా సముచ్ఛయం చెంది ఏర్పడిన కణాలను మిసెల్లు అంటారు.
ఉదా : సబ్బులు, డిటర్జంట్లు మిసెల్లను ఏర్పరుస్తాయి.
మిసెల్ ఏర్పడే విధానం :
సబ్బు ద్రావణాన్ని ఉదాహరణగా తీసుకొందాం. భార కొవ్వు ఆమ్లాల సోడియమ్ లేదా పొటాషియమ్ లవణాన్ని సబ్బు అంటాం. దీనిని RCOO–Na+ (సోడియమ్ స్టియరేట్ CH3(CH)16COO–Na+ అంటారు. ఇది చాలా బార్ సబ్బులలో ప్రధాన అనుఘటకంగా ఉంది). దీనిని నీటిలో కరిగిస్తే ఇది RCOO– గాను, Na+ గాను వియోజనం చెందుతుంది. RCOO– అయాన్లో రెండు భాగాలు ఉన్నాయి. ఇవి పొడవైన హైడ్రోకార్బన్ గొలుసు R (దీనిని అధ్రువ భాగం లేదా ‘తోక’ అంటారు). ఇది హైడ్రోఫోబిక్ (నీటిని వికర్షించే భాగం), COO ధ్రువ భాగం (ధ్రువ అయానిక లేదా ‘తల’ భాగం) ఇది హైడ్రోఫిలిక్ (నీటిని ఆకర్షించే భాగం).
ఉపరితలంపై ఉండే RCOO– అయాన్లు COO– గ్రూపులు నీటిలోను హైడ్రోకార్బన్ గొలుసు (R) నీటికి దూరంగా ఉపరితలం వద్ద ఉంటాయి. అయితే సందిగ్ధ మిసెల్ గాఢత (CMC) వద్ద COO– అయాన్లు, ద్రావణం లోపలికి లాగబడతాయి.

ఈ పరిస్థితులలో అవి సముచ్ఛయం చెంది గోళాకారంలోకి మారతాయి. హైడ్రోకార్బన్ గొలుసులు గోళం కేంద్రకం వైపుగా చొచ్చుకొని ఉంటాయి. COO– గ్రూపులు గోళం ఉపరితలంపై ఊర్ధ్వభాగం వైపుగా చోటుచేసుకొని ఉంటాయి. ఈ విధంగా ఏర్పడిన సముచ్ఛయాన్ని అయానిక్ మిసైల్ అంటారు. ఈ అణువులలో సుమారు 100 సాధారణ అణువులు ఉంటాయి. ఇదేవిధంగా సోడియమ్ లారిల్ సల్ఫేట్ CH3(CH2)11 SO–4 Na+ వంటి డిటర్జెంట్లలో – SO–4 పోలార్ గ్రూపుగా పొడవైన హైడ్రోకార్బన్ గొలుసుతో కూడా ఉంటుంది. కాబట్టి వీటి విషయంలో కూడా మిసెల్ ఏర్పాటు విధానం సబ్బులలో మాదిరిగానే ఉంటుంది.
![]()
ప్రశ్న 13.
కొల్లాయిడ్ల తయారీని, అవసరమైనచోట పటాల సహాయంతో వర్ణించండి.
జవాబు:
బ్రెడిగ్ విద్యుత్చాప పద్ధతి :
ఈ పద్ధతిలో విక్షేపణం (dispersion), సాంద్రీకరణం (condensation) రెండు ప్రక్రియలు ఇమిడి ఉన్నాయి. గోల్డ్, సిల్వర్, ప్లాటినమ్ మొదలైన లోహ కొల్లాయిడ్ సాల్లను ఈ పద్ధతిలో తయారుచేస్తారు. ఈ పద్ధతిలో విక్షేపణ యానకంలో ముంచి ఉంచిన లోహ ఎలక్ట్రోడ్ల మధ్య విద్యుత్ చాపాన్ని అనువర్తిస్తారు. ఈ పద్ధతిలో అత్యధిక పరిమాణంలో వెలువడిన ఉష్ణం లోహబాష్పాలను ఏర్పరుస్తుంది. ఈ బాష్పాలు సాంద్రీకరణం చెంది కొల్లాయిడ్ల పరిమాణంలో కణాలను ఏర్పరుస్తాయి.
రసాయన పద్ధతులు :
క్రియాజన్య జాతులను ఏర్పరచే ద్వంద్వ వియోగం, ఆక్సీకరణం, క్షయకరణం, జలవిశ్లేషణం మొదలైన రసాయన చర్యల ఆధారంగా కొల్లాయిడ్లను తయారుచేస్తారు. క్రియాజన్య జాతులు సముచ్ఛయం చెంది, సాల్లను ఏర్పరుస్తాయి.
పెష్టీకరణం :
విక్షేపణ యానకంలో ఉన్న ఒక అవక్షేపానికి కొద్ది ప్రయాణంలో ఒక విద్యుద్విశ్లేష్యాన్ని కలిపి బాగా కుదపడం ద్వారా అవక్షేపాన్ని కొల్లాయిడల్ స్థితికి మార్చడాన్ని పెష్టీకరణం అంటారు.
![]()
ప్రశ్న 14.
ఎమల్షన్లు అంటే ఏమిటి? వీటిని ఎలా వర్గీకరిస్తారు? ఎమల్షన్ల అనువర్తనాలను తెలపండి. [TS. Mar.’16]
జవాబు:
ఎమల్షన్ :
“ద్రవ విక్షేపక యానకంలో, సూక్ష్మ విభాజిత ద్రవబిందు కణాలు విక్షిప్తం చెంది ఏర్పరిచే వ్యవస్థే ఎమల్షన్”.
(లేదా)
విక్షిప్త ప్రావస్థ మరియు విక్షేపక యానకం రెండూ ద్రవాలే అయిన కొల్లాయిడ్ వ్యవస్థను ‘ఎమల్షన్’ అంటారు.
ఉదా : పాలు – ద్రవ క్రొవ్వు నీటిలో విక్షిప్తం చెంది ఉండే ఎమల్షన్.
(ఎ) నీటిలో తైలం (O / W) రకం ఎమల్షన్లు :
వీటిలో విక్షిప్త ప్రావస్థ : నీరు
విక్షేపక యానకం : తైలం
ఉదాహరణలు :
i) పాలు – నీటిలో ద్రవ కొవ్వు ఏర్పరచే ఎమల్షన్
ii) వానిషింగ్ క్రీమ్ – నీటిలో క్రొవ్వు
(బి) తైలంలో నీరు (W / O) రకం ఎమల్షన్లు :
వీటిలో విక్షిప్త ప్రావస్థ : నీరు
విక్షేపక యానకం : తైలం
ఉదాహరణలు : i) గట్టి గ్రీజులు – కందెన తైలాల్లో నీరు
ii) కోల్డ్ క్రీమ్ – క్రొవ్వులో నీరు
ఎమల్షన్ల అనువర్తనాలు :
- తైలాల వంటి మందుల తయారీలో ఉపయోగిస్తారు.
- బట్టలను శుభ్రపరుచుటలో ఉపయోగిస్తారు.
- కొవ్వులను కరిగించుటలో ఉపయోగిస్తారు.
- లోషన్లు, క్రీములు, ఆయింట్మెంట్ల తయారీలో ఉపయోగిస్తారు.
- ప్లవన క్రియ ద్వారా లోహాలను శుద్ధిచేయుటలో ఉపయోగిస్తారు.
- నూనె బావులలో నీరు తైలం ఎమల్షన్లను వియోగం చేయుటలో ఉపయోగిస్తాయి.
పాఠ్యాంశ ప్రశ్నలు Intext Questions
ప్రశ్న 1.
కెమిసాన్ రెండు అభిలాక్షణిక ధర్మాలను తెలపండి.
జవాబు:
అనువర్తిత emf ప్రభావంతో కొల్లాయిడ్ కణం చలనం చెందే ప్రక్రిను విద్యుదావేశితకణ చలనం (లేదా) ఎలక్ట్రోఫోరసిన్ అంటారు. సాల్ కొల్లాయిడ్ కణాలు పాత్ర అడుగు భాగానికి చేరి స్థిరపడే ప్రక్రియను సాల్స్కంధనం లేదా అవక్షేపణం లేదా ఫ్లాక్యులేషన్ అంటారు.
ప్రశ్న 2.
ఉష్ణోగ్రత పెరుగుదలతో ఫిజిసార్షన్ అవధి ఎందుకు తగ్గిపోతుంది?
జవాబు:
ఫిజిసాల్షన్ ఒక ఉష్ణమోచక చర్య. ఉష్ణోగ్రత పెంచితే చర్య తిరోగమిస్తుంది. అందువలన పిజిసాల్షన్ తగ్గును.
ప్రశ్న 3.
సూక్ష్మవిభాజిత స్థితిలో ఉండే పదార్థాలు, సూక్ష్మవిభాజిత స్థితిలో లేని స్ఫటిక రూపంలో ఉండే ఈ పదార్థాల కంటే ఎందుకు అధిక అధిశోషణ సామర్థ్యం కనబరుస్తాయి?
జవాబు:
సూక్ష్మ విభాజిత స్థితిలో ఉండు పదార్థాలకు ఉపరితల వైశాల్యం అధికం కావున అధిశోషణ సామర్థ్యం అధికంగా ఉంటుంది.
ప్రశ్న 4.
NiO ఉత్ప్రేరకం సమక్షంలో మీథేన్ ను నీటి ఆవిరితో చర్య జరిపించి హేబర్ పద్ధతిలో వాడే హైడ్రోజను తయారుచేస్తారు. ఈ ప్రక్రియను నీటిఆవిరి పునరుద్ధరణ చర్య అంటారు. అమోనియాను హేబర్ పద్ధతిలో తయారు చేసినప్పుడు ఈ నీటి ఆవిరి పునరుద్ధరణ చర్యలో CO ను ఎందుకు తొలగిస్తారు?
జవాబు:
కార్బన్మోనాక్సైడ్ (CO) విషపూరితమైనది. ఇది ఉత్ప్రేరకం Fe యొక్క మరియు ప్రవర్థకం Mo యొక్క ఉత్తేజితత్వాన్ని తగ్గిస్తుంది. అందువలన COను తొలగించవచ్చు.
ప్రశ్న 5.
ఆరంభ దశలో ఎస్టర్ జలవిశ్లేషణ చర్య నెమ్మదిగా జరిగి, కొంత చర్యాకాలం తరువాత వేగంగా జరుగుతుంది. ఎందుకు?
జవాబు:
ఎస్టర్ జలవిశ్లేషణ రసాయన చర్య

చర్యలో ఏర్పడిన కార్బాక్సిలిక్ ఆమ్లం H+ లను విడుదల చేస్తుంది. ఇవి స్వయం ఉత్ప్రేరణ చర్య జరుపుతాయి. అందువలన కొంత చర్యాకాలం తరువాత చర్య వేగంగా జరుగుతుంది.
ప్రశ్న 6.
అధిశోషణం ఉత్ప్రేరణ ప్రక్రియలో విశోషణం పాత్ర ఏమిటి?
జవాబు:
విశోషణం వలన ఉత్ప్రేరకం ఉపరితలంపై ఉన్న క్రియాజన్యాలు విడిపోయి మరలా ఉత్ప్రేరకం క్రియాజనకాలను ఉపరితలంపై అధిశోషించుటకు కారణం అవుతుంది.
ప్రశ్న 7.
హార్డీ-షూల్జ్ నియమానికి నీవు ఎటువంటి మార్పులను సూచిస్తావు?
జవాబు:
సమాన మోలార్ నిష్పత్తులలో ఉన్న రెండు వ్యతిరేక ఆవేశాలు గల సాల్లను కలిపినపుడు అవి పరస్పరం తటస్థీకరింపబడి రెండు స్కందన ప్రక్రియకు గురిఅవుతాయి.
![]()
ప్రశ్న 8.
భారాత్మక విశ్లేషణ పద్ధతిలో అవక్షేపాన్ని తడి లేకుండా చేసి, తూచే ముందుగా దానిని క్షాళన ద్రవంతో ఎందుకు ప్రక్షాళనం చేస్తావు?
జవాబు:
కణాల ఉపరితలంపై కొన్ని క్రియాజనక అయాన్లు అంటుకొని ఉంటాయి. వీటిని తొలగించుటకు నీటితో అవక్షేపాన్ని శుభ్రం చేస్తారు.